通过海水晾晒可得粗盐,粗盐中除NaCl外,还含有 、
、 、
、 以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、
以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、 溶液、
溶液、 溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
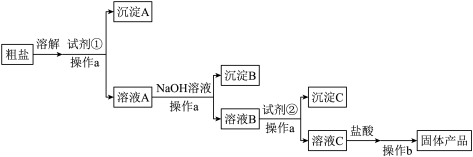
请回答:
(1)操作a名称是_______ 。
(2)试剂①是_______ 溶液(填化学式)。
(3)加入NaOH后,得到的主要沉淀B是_______ 。
(4)加入试剂②后,发生反应的离子方程式有_______ 。
(5)如果加入试剂②后直接加盐酸,产生的后果是_______ (用离子方程式表示)。
 、
、 、
、 以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、
以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、 溶液、
溶液、 溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
请回答:
(1)操作a名称是
(2)试剂①是
(3)加入NaOH后,得到的主要沉淀B是
(4)加入试剂②后,发生反应的离子方程式有
(5)如果加入试剂②后直接加盐酸,产生的后果是
更新时间:2022-11-01 11:31:06
|
相似题推荐
【推荐1】NiCl2是一种重要催化剂。某科研小组以废弃催化剂(含Ni2+、Cu2+、Fe3+、Ca2+、Mg2+等)为原料,按如图流程回收NiCl2·6H2O晶体,回答下列问题。
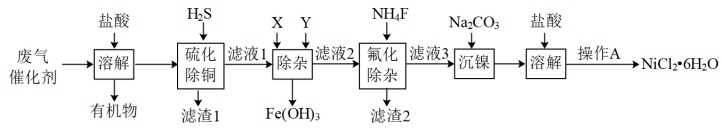
已知:Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9
(1)滤渣1的成分主要是_______ 。
(2)若X为Cl2,则其发生的离子方程式是_______ 。若用H2O2代替Cl2,试剂Y的使用量会减少,原因是_______ 。
(3)氟化除杂时要保证完全除去Ca2+和Mg2+(离子浓度≤10-5mol/L),滤液3中c(F-)不小于_______ mol/L。
(4)实际生产中,产生的滤渣均需进行洗涤,并将洗涤液与滤液合并,此操作的目的是_______ 。操作A为_______ 、冷却结晶、过滤、洗涤。
(5)将所得NiCl2·6H2O与SOCl2混合加热可制备无水 NiCl2并得到两种酸性气体,反应的化学方程式为_______ 。

已知:Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9
(1)滤渣1的成分主要是
(2)若X为Cl2,则其发生的离子方程式是
(3)氟化除杂时要保证完全除去Ca2+和Mg2+(离子浓度≤10-5mol/L),滤液3中c(F-)不小于
(4)实际生产中,产生的滤渣均需进行洗涤,并将洗涤液与滤液合并,此操作的目的是
(5)将所得NiCl2·6H2O与SOCl2混合加热可制备无水 NiCl2并得到两种酸性气体,反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室通常用MnO2与浓盐酸反应制取氯气。现用下列有关装置先制取干燥、纯净的氯气,后进行有关性质实验。试根据下列有关装置回答有关问题。
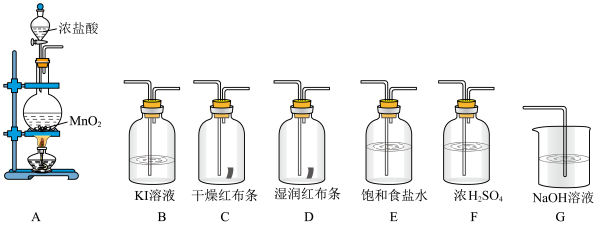
(1)上述装置中各仪器从左至右的连接顺序为___________ ,A接___________接___________接___________接___________接___________接G。
(2)E装置的作用是___________ ,D中的现象为___________ ,B中的现象为___________ 。
(3)写出相关反应的离子方程式:A中___________ ,G中___________ 。
(4)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)___________ 。

(1)上述装置中各仪器从左至右的连接顺序为
(2)E装置的作用是
(3)写出相关反应的离子方程式:A中
(4)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】学习小组探究碳酸钠和碳酸氢钠性质
(1)分别取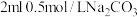 和
和
如图:Ⅰ中浅红色褪去,且立即产生大量气泡;Ⅱ中开始无气泡,溶液颜色由红色变为浅红色,最后出现大量气泡.
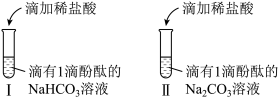
①浓度相同时,碱性
________  (填“>”或“<”)。
(填“>”或“<”)。
②Ⅱ的反应过程出现 的证据是
的证据是___________ ,其离子反应的方程式________________ 。
(2)用 固体配制
固体配制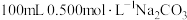 溶液。
溶液。
①用到的玻璃仪器有:量筒、烧杯、玻璃棒、胶头滴管和_____________ 。
②计算需要 固体的质量是
固体的质量是_________ g。
③下列情况中,会使所配溶液浓度偏高的是___________ (填字母)。
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(3)我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献.下图为联合制碱法的主要过程(部分物质已略去)。
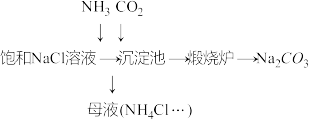
已知:ⅰ. 极易溶于水并生成碱,与酸反应生成盐,如
极易溶于水并生成碱,与酸反应生成盐,如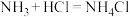 。
。
ⅱ.有关物质的溶解度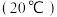
沉淀池中主要沉淀物________ (化学式),发生反应的化学方程式为_______________ 。
(1)分别取
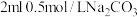 和
和
如图:Ⅰ中浅红色褪去,且立即产生大量气泡;Ⅱ中开始无气泡,溶液颜色由红色变为浅红色,最后出现大量气泡.

①浓度相同时,碱性

 (填“>”或“<”)。
(填“>”或“<”)。②Ⅱ的反应过程出现
 的证据是
的证据是(2)用
 固体配制
固体配制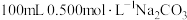 溶液。
溶液。①用到的玻璃仪器有:量筒、烧杯、玻璃棒、胶头滴管和
②计算需要
 固体的质量是
固体的质量是③下列情况中,会使所配溶液浓度偏高的是
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(3)我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献.下图为联合制碱法的主要过程(部分物质已略去)。
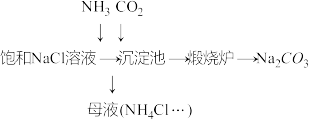
已知:ⅰ.
 极易溶于水并生成碱,与酸反应生成盐,如
极易溶于水并生成碱,与酸反应生成盐,如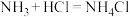 。
。ⅱ.有关物质的溶解度
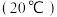
| 物质 |  |  |  |  |
| 溶解度/g | 36.0 | 21.7 | 9.6 | 37.2 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】碱式碳酸镁[MgCO3 Mg(OH)2]是一种重要的无机化工产品,在现代社会中具有广泛的应用。白云石[主要成分为CaMg(CO3)2]碳化法制备碱式碳酸镁的流程如图所示:
Mg(OH)2]是一种重要的无机化工产品,在现代社会中具有广泛的应用。白云石[主要成分为CaMg(CO3)2]碳化法制备碱式碳酸镁的流程如图所示:
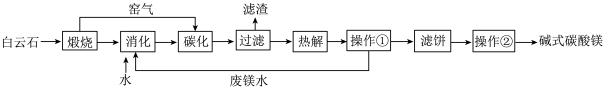
已知:①“碳化”时发生的反应为Mg(OH)2+Ca(OH)2+3CO2=Mg(HCO3)2+CaCO3↓+H2O;
②滤饼的主要成分为MgCO3 Mg(OH)2,还含有少量Mg(HCO3)2。
Mg(OH)2,还含有少量Mg(HCO3)2。
回答下列问题:
(1)“煅烧”时发生反应的化学方程式为___________ ,为了加快“煅烧”速率,可以采取的措施有___________ (写出一种)。
(2)“消化”过程需要加水、搅拌并保持60℃消化1 h,得到精灰乳,若往精灰乳中通入氯气,其中Ca(OH)2悬浊液与氯气发生反应的化学方程式为___________ 。
(3)操作①为___________ ,操作②包含___________ 、___________ ;碱式碳酸镁属于___________ (填标号)。
a.混合物 b.碱 c.盐 d.氧化物
(4)采用上述流程制得的碱式碳酸镁常含一定量结晶水,化学式为MgCO3·Mg(OH)2·xH2O。称取10.0 g样品,进行热重分析,并绘制出如图所示热重曲线示意图。则T℃时所得固体的化学式为___________ ,计算x=___________ 。

 Mg(OH)2]是一种重要的无机化工产品,在现代社会中具有广泛的应用。白云石[主要成分为CaMg(CO3)2]碳化法制备碱式碳酸镁的流程如图所示:
Mg(OH)2]是一种重要的无机化工产品,在现代社会中具有广泛的应用。白云石[主要成分为CaMg(CO3)2]碳化法制备碱式碳酸镁的流程如图所示:
已知:①“碳化”时发生的反应为Mg(OH)2+Ca(OH)2+3CO2=Mg(HCO3)2+CaCO3↓+H2O;
②滤饼的主要成分为MgCO3
 Mg(OH)2,还含有少量Mg(HCO3)2。
Mg(OH)2,还含有少量Mg(HCO3)2。回答下列问题:
(1)“煅烧”时发生反应的化学方程式为
(2)“消化”过程需要加水、搅拌并保持60℃消化1 h,得到精灰乳,若往精灰乳中通入氯气,其中Ca(OH)2悬浊液与氯气发生反应的化学方程式为
(3)操作①为
a.混合物 b.碱 c.盐 d.氧化物
(4)采用上述流程制得的碱式碳酸镁常含一定量结晶水,化学式为MgCO3·Mg(OH)2·xH2O。称取10.0 g样品,进行热重分析,并绘制出如图所示热重曲线示意图。则T℃时所得固体的化学式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】镁及其化合物在生产生活中有重要的作用。以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:
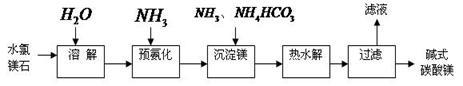
(1)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为___________ 。指出该物质在工农业生产中的一种用途:___________ 。
(2)写出预氨化时发生的主要反应的离子方程式:_________________________ 。
(3)沉淀镁时反应的温度不宜过高,原因是___________________________ 。
(4)设计一个实验,确定产品碱式碳酸镁aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量;②高温分解;③_______________ ;④______________ ;⑤称量MgO。
18.2g产品完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:
a=________ ;b =________ ;c =________ 。
(5)从水氯镁石中可以提取无水氯化镁,电解熔融态的无水氯化镁可以得到金属镁。有同学认为:电解熔融的MgO也可制金属镁,在实际生产中可简化生产步骤,体现生产的简约性和经济性原则。你同意该同学的想法吗?为什么?你的观点是______________________ 。理由是_________________________________________________________________ 。

(1)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为
(2)写出预氨化时发生的主要反应的离子方程式:
(3)沉淀镁时反应的温度不宜过高,原因是
(4)设计一个实验,确定产品碱式碳酸镁aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量;②高温分解;③
18.2g产品完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:
a=
(5)从水氯镁石中可以提取无水氯化镁,电解熔融态的无水氯化镁可以得到金属镁。有同学认为:电解熔融的MgO也可制金属镁,在实际生产中可简化生产步骤,体现生产的简约性和经济性原则。你同意该同学的想法吗?为什么?你的观点是
您最近一年使用:0次
【推荐3】MgSO4·7H2O医药上用作泻剂。工业上用氯碱工业中的一次盐泥为原料生产。已知一次盐泥中含有镁、钙、铁、铝、锰的硅酸盐和碳酸盐等成分。主要工艺如下:
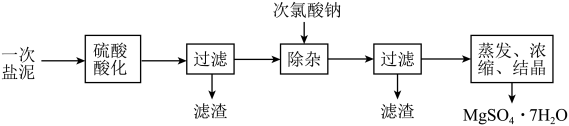
(1)用硫酸调整溶液pH到1~2,硫酸的作用是________________________ 。
(2)加次氯酸钠溶液至pH=5~6并加热煮沸约5~10分钟,滤渣中主要含MnO2和另两种沉淀,另两种沉淀是___________________ (写化学式)。其中次氯酸钠溶液将MnSO4转化为MnO2的离子方程式为:____________________ 。
(3)若除杂后过滤,发现滤液发黄,需采取的措施是__________________ 。
(4)过滤后晶体常用丙酮代替蒸馏水洗涤的目的是______________________ 。
(5)晶体中结晶水含量的测定:准确称取0.20g MgSO4·7H2O样品,放入已干燥至恒重的瓷坩埚,置于马弗炉中,在200℃脱水1小时。为准确确定脱水后的质量,还需要经过的操作有:冷却(干燥器中)至室温→_______________________ 。
(6)硫酸根离子质量分数的测定:准确称取自制的样品0.50g,用200mL水溶液,加入2mol·L-1HCl溶液5mL,将溶液加热至沸,在不断搅拌下逐滴加入5~6mL0.5mol·L-1BaCl2溶液,充分沉淀后,得沉淀0.466g,则样品中w(SO )=
)=____________ 。

(1)用硫酸调整溶液pH到1~2,硫酸的作用是
(2)加次氯酸钠溶液至pH=5~6并加热煮沸约5~10分钟,滤渣中主要含MnO2和另两种沉淀,另两种沉淀是
(3)若除杂后过滤,发现滤液发黄,需采取的措施是
(4)过滤后晶体常用丙酮代替蒸馏水洗涤的目的是
(5)晶体中结晶水含量的测定:准确称取0.20g MgSO4·7H2O样品,放入已干燥至恒重的瓷坩埚,置于马弗炉中,在200℃脱水1小时。为准确确定脱水后的质量,还需要经过的操作有:冷却(干燥器中)至室温→
(6)硫酸根离子质量分数的测定:准确称取自制的样品0.50g,用200mL水溶液,加入2mol·L-1HCl溶液5mL,将溶液加热至沸,在不断搅拌下逐滴加入5~6mL0.5mol·L-1BaCl2溶液,充分沉淀后,得沉淀0.466g,则样品中w(SO
 )=
)=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】已知某化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。某校化学研究性学习小组通过查阅资料,设计了如下图所示的方法以该含镍废催化剂为原料来制备NiSO4·7H2O。
25℃时部分阳离子以氢氧化物形式沉淀时的pH如下:
回答下列问题:
(1)操作a、c中需使用的仪器除铁架台(带铁圈)、酒精灯、烧杯、玻璃棒外还需要的主要仪器为________ 。
(2)“碱浸”的目的是除去________ 。
(3)“酸浸”时所加入的酸是________ (填化学式)。酸浸后,经操作a分离出固体①后,溶液中可能含有的金属离子是________ 。
(4)操作b为调节溶液的pH,你认为pH的最佳调控范围是________ 。
(5)“调pH为2~3”的目的是________ 。
(6)产品晶体中有时会混有少量绿矾(FeSO4·7H2O),其原因可能是________ 。
(7)NiSO4在强碱溶液中用次氯酸钠氧化,可以制得碱性镍镉电池电极材料—NiOOH。该反应的离子方程式___________ 。
(8)一般认为残留在溶液中的离子浓度小于1×10-5 mol/L时,沉淀已经完全。请利用上表中数据估算Fe(OH)2的溶度积________ 和可逆反应Fe2++2H2O 2H++Fe(OH)2在25℃时的平衡常数
2H++Fe(OH)2在25℃时的平衡常数________ 。

25℃时部分阳离子以氢氧化物形式沉淀时的pH如下:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀pH | 3.4 | 1.8 | 7.5 | 7.1 |
| 完全沉淀pH | 5.2 | 3.2 | 9.7 | 9.2 |
(1)操作a、c中需使用的仪器除铁架台(带铁圈)、酒精灯、烧杯、玻璃棒外还需要的主要仪器为
(2)“碱浸”的目的是除去
(3)“酸浸”时所加入的酸是
(4)操作b为调节溶液的pH,你认为pH的最佳调控范围是
(5)“调pH为2~3”的目的是
(6)产品晶体中有时会混有少量绿矾(FeSO4·7H2O),其原因可能是
(7)NiSO4在强碱溶液中用次氯酸钠氧化,可以制得碱性镍镉电池电极材料—NiOOH。该反应的离子方程式
(8)一般认为残留在溶液中的离子浓度小于1×10-5 mol/L时,沉淀已经完全。请利用上表中数据估算Fe(OH)2的溶度积
 2H++Fe(OH)2在25℃时的平衡常数
2H++Fe(OH)2在25℃时的平衡常数
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
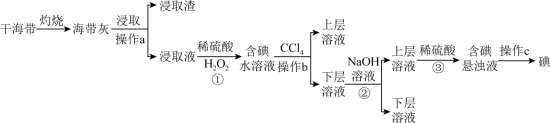
【推荐2】浩瀚的海洋里蕴藏着丰富的化学资源,从海带中提取碘单质的工艺流程如图。回答下列问题:_______ (填仪器名称)中,用酒精灯充分加热灰化。
(2)浸取液中碘主要以 存在,写出①发生反应的离子方程式
存在,写出①发生反应的离子方程式_______ ,实验步骤①后若检验溶液中碘单质的存在,具体方法是_______ 。
(3)向含有 的水溶液中加入
的水溶液中加入 振荡静置后的实验现象
振荡静置后的实验现象_______ 。
(4)步骤②中加入浓 溶液发生反应的化学方程式为
溶液发生反应的化学方程式为_______ ,步骤③反应中氧化剂与还原剂物质的量之比为_______ 。
(5)步骤②③是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为_______ 法。
(6)操作c的名称为_______ 。
(2)浸取液中碘主要以
 存在,写出①发生反应的离子方程式
存在,写出①发生反应的离子方程式(3)向含有
 的水溶液中加入
的水溶液中加入 振荡静置后的实验现象
振荡静置后的实验现象(4)步骤②中加入浓
 溶液发生反应的化学方程式为
溶液发生反应的化学方程式为(5)步骤②③是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为
(6)操作c的名称为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物,该电池放电过程产生MnOOH,回收处理该废电池可以得到多种化工原料,有关数据如表所示:
溶解度/(g/100g水)
某些氢氧化物的Ksp
(1)该电池的正极反应式为____ 。
(2)电池工作时产生了x库伦电量,理论上消耗锌____ g(已知转移1mol电子所产生的电量为96500库伦)。
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,两者可以通过____ 分离回收;滤渣的主要成分是MnO2、C和MnOOH,欲从中得到较纯的MnO2,最简便的方法是____ 。
(4)用废电池的锌皮制备ZnSO4•7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是:加稀H2SO4和H2O2溶解,铁变为____ (填粒子符号),加碱调节pH使铁刚好完全沉淀;继续加碱调节pH为____ 时,锌开始沉淀(假定Zn2+浓度为0.1mol/L)。若上述过程不加H2O2的后果是____ 。
溶解度/(g/100g水)
| 0℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ | |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
(2)电池工作时产生了x库伦电量,理论上消耗锌
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,两者可以通过
(4)用废电池的锌皮制备ZnSO4•7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是:加稀H2SO4和H2O2溶解,铁变为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
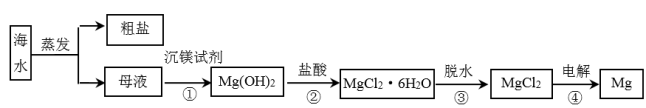
【推荐1】镁及其合金是一种用途很广的金属材料,目前世界上生产的镁有60%来自海水。一种从海水的母液中提取金属镁的工艺流程如下:_______ 。
a.氢氧化钙 b.氨水 c.氢氧化铜
(2)加入沉镁试剂后,能够分离得到Mg(OH)2沉淀的方法是_______ 。
(3)步骤②发生的化学反应方程式是_______ 。
(4)某海水中镁的含量为1.2g·L-1,则1L海水理论上可制得MgCl2的质量是_______ g。
a.氢氧化钙 b.氨水 c.氢氧化铜
(2)加入沉镁试剂后,能够分离得到Mg(OH)2沉淀的方法是
(3)步骤②发生的化学反应方程式是
(4)某海水中镁的含量为1.2g·L-1,则1L海水理论上可制得MgCl2的质量是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】某学习小组用含有少量杂质(主要为 )的粗盐制取较纯净的
)的粗盐制取较纯净的 ,实验前他们设计了如图所示的实验方案。
,实验前他们设计了如图所示的实验方案。
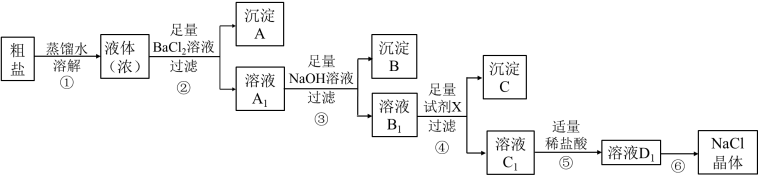
请回答:
(1)步骤②中除去的杂质离子是_______ 。
(2)试剂X是_______ ;用离子方程式表示其作用_______ 、_______ 。
(3)写出步骤⑤中发生反应的离子方程式_______ 、_______ 。
(4)步骤⑥的操作是_______ 。
 )的粗盐制取较纯净的
)的粗盐制取较纯净的 ,实验前他们设计了如图所示的实验方案。
,实验前他们设计了如图所示的实验方案。
请回答:
(1)步骤②中除去的杂质离子是
(2)试剂X是
(3)写出步骤⑤中发生反应的离子方程式
(4)步骤⑥的操作是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】 是一种常见的氧化剂,工业上利用软锰矿
是一种常见的氧化剂,工业上利用软锰矿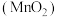 制备高锰酸钾的流程如下,在实验室中模拟该流程制备
制备高锰酸钾的流程如下,在实验室中模拟该流程制备 ,并对产物纯度进行测定。
,并对产物纯度进行测定。
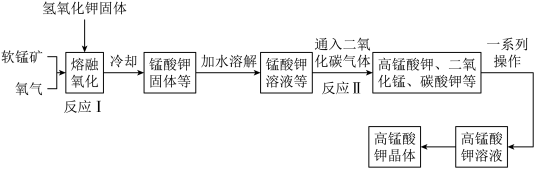
回答下列问题:
(1)反应Ⅰ需要的温度约为400℃,应选择的加热仪器为_______ 。
A酒精灯 B.电磁炉 C.电吹风
(2)加水溶解步骤必须要用到的玻璃仪器有_______。
(3)若要除去 、
、 溶液中的
溶液中的 ,应进行操作
,应进行操作_______ (填操作名称)。
(4)由 溶液获的
溶液获的 晶体的一系列操作为:蒸发浓缩至饱和、
晶体的一系列操作为:蒸发浓缩至饱和、_______ 、过滤、洗涤、干燥(填操作名称)。
(5)研究表明,反应Ⅰ分两步进行:
第一步反应生成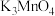 ,反应方程式为
,反应方程式为_______ 。
第二步反应方程式为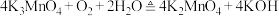
(6)写出反应Ⅱ的离子方程式_______ 。
(7)所得产品中只含有杂质 ,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为_______ %(保留两位小数)。
 是一种常见的氧化剂,工业上利用软锰矿
是一种常见的氧化剂,工业上利用软锰矿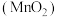 制备高锰酸钾的流程如下,在实验室中模拟该流程制备
制备高锰酸钾的流程如下,在实验室中模拟该流程制备 ,并对产物纯度进行测定。
,并对产物纯度进行测定。
回答下列问题:
(1)反应Ⅰ需要的温度约为400℃,应选择的加热仪器为
A酒精灯 B.电磁炉 C.电吹风
(2)加水溶解步骤必须要用到的玻璃仪器有_______。
| A.烧杯 | B.玻璃棒 | C.量筒 | D.酒精灯 |
 、
、 溶液中的
溶液中的 ,应进行操作
,应进行操作(4)由
 溶液获的
溶液获的 晶体的一系列操作为:蒸发浓缩至饱和、
晶体的一系列操作为:蒸发浓缩至饱和、(5)研究表明,反应Ⅰ分两步进行:
第一步反应生成
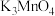 ,反应方程式为
,反应方程式为第二步反应方程式为
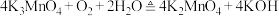
(6)写出反应Ⅱ的离子方程式
(7)所得产品中只含有杂质
 ,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
您最近一年使用:0次



