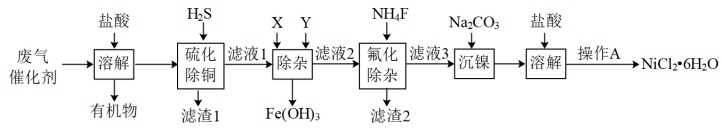
NiCl2是一种重要催化剂。某科研小组以废弃催化剂(含Ni2+、Cu2+、Fe3+、Ca2+、Mg2+等)为原料,按如图流程回收NiCl2·6H2O晶体,回答下列问题。
已知:Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9
(1)滤渣1的成分主要是_______ 。
(2)若X为Cl2,则其发生的离子方程式是_______ 。若用H2O2代替Cl2,试剂Y的使用量会减少,原因是_______ 。
(3)氟化除杂时要保证完全除去Ca2+和Mg2+(离子浓度≤10-5mol/L),滤液3中c(F-)不小于_______ mol/L。
(4)实际生产中,产生的滤渣均需进行洗涤,并将洗涤液与滤液合并,此操作的目的是_______ 。操作A为_______ 、冷却结晶、过滤、洗涤。
(5)将所得NiCl2·6H2O与SOCl2混合加热可制备无水 NiCl2并得到两种酸性气体,反应的化学方程式为_______ 。

已知:Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9
(1)滤渣1的成分主要是
(2)若X为Cl2,则其发生的离子方程式是
(3)氟化除杂时要保证完全除去Ca2+和Mg2+(离子浓度≤10-5mol/L),滤液3中c(F-)不小于
(4)实际生产中,产生的滤渣均需进行洗涤,并将洗涤液与滤液合并,此操作的目的是
(5)将所得NiCl2·6H2O与SOCl2混合加热可制备无水 NiCl2并得到两种酸性气体,反应的化学方程式为
2022·陕西西安·三模 查看更多[5]
陕西省西安中学2021-2022学年高三下学期第三次模拟考试理科综合化学试题(已下线)秘籍17 工艺流程的条件控制与计算-备战2022年高考化学抢分秘籍(全国通用)(已下线)专项15 工艺流程综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)湖南省湘潭市第一中学2023届高三上学期第五次月考化学试题四川省泸州市泸县第五中学2022-2023学年高二下学期4月月考化学试题
更新时间:2022-04-07 20:23:24
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某地环保部门取一定量某工厂所排酸性废水试样分成甲、乙、丙、丁四份,进行如图所示探究。

已知:废水试样中除H+外可能含有下表中的离子:
请回答下列问题:
(1)离子X是________________ (填化学式,下同),离子Y是________________ 。
(2)表中不能确定是否存在的阴离子是________ ,能证明该阴离子是否存在的简单实验操作为____________________________________________________________________________ 。
(3)写出废水试样中滴加淀粉KI溶液所发生反应的离子方程式:_____________________ 。

已知:废水试样中除H+外可能含有下表中的离子:
| 阳离子 | Na+、Mg2+、X |
| 阴离子 | Cl-、SO 、Y、NO 、Y、NO |
(1)离子X是
(2)表中不能确定是否存在的阴离子是
(3)写出废水试样中滴加淀粉KI溶液所发生反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】聚合硫酸铁是一种新型高效净水剂。以黄铁矿(主要成分:FeS2,铁的化合价为+2价)烧渣(主要成分为Fe2O3、FeO、SiO2等)为原料制取聚合硫酸铁(铁的化合价为+3价)的实验步骤如下:

回答下列问题:
(1)用98%的浓硫酸配制28%的稀硫酸,需要的玻璃仪器除玻璃棒外,还需要________ (填写仪器名称)。
(2)“煅烧”过程发生反应的氧化产物是___________________________ ;SO2氧化为SO3是工业生产硫酸的重要反应,写出该反应的化学方程式_______________________ 。
(3)写出“酸浸”过程中发生反应的离子方程式___________________________ 。
(4)“氧化”过程中先产生无色气体,最终变成红棕色气体,写出加入NaNO3产生无色气体反应的离子方程式______________________________ ,若用H2O2代替NaNO3达到相同氧化效果,消耗H2O2和NaNO3的物质的量之比___________ 。
(5)为确定产品是否合格,需测定聚合硫酸铁中Fe3+和SO42-的物质的量之比,测定时需要的试剂为___________ (填写序号)。
a. FeSO4 b. BaCl2 c. NaOH d. NaCl

回答下列问题:
(1)用98%的浓硫酸配制28%的稀硫酸,需要的玻璃仪器除玻璃棒外,还需要
(2)“煅烧”过程发生反应的氧化产物是
(3)写出“酸浸”过程中发生反应的离子方程式
(4)“氧化”过程中先产生无色气体,最终变成红棕色气体,写出加入NaNO3产生无色气体反应的离子方程式
(5)为确定产品是否合格,需测定聚合硫酸铁中Fe3+和SO42-的物质的量之比,测定时需要的试剂为
a. FeSO4 b. BaCl2 c. NaOH d. NaCl
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】SO2广泛用于医药、硫酸工业等领域,回收废气中的SO2可用如下方法。
(1)方法Ⅰ的过程如下。
① 制备Al2(SO4)x(OH)y。向Al2(SO4)3溶液中加入CaO粉末,调pH至3.6。 CaO的作用是______
② 吸收:Al2(SO4)x(OH)y吸收SO2后的产物是______ (写化学式)。
③ 解吸:加热②中产物,产生SO2,Al2(SO4)x(OH)y再生。
(2)方法Ⅱ中,在Fe2+催化下,SO2、O2和H2O生成H2SO4的化学方程式是______ 。
(3)方法Ⅱ中,Fe2+的催化过程可表示如下:
ⅰ:2Fe2++O2+SO2=2Fe3++SO42-
ⅱ:……
① 写出ⅱ的离子方程式:______ 。
② 下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向FeCl2溶液滴入KSCN,无变化
b.向FeCl2溶液通入少量SO2,滴入KSCN,颜色变红。
c.取b中溶液,______ 。
(4)方法Ⅱ中,催化氧化后,采用滴定法测定废气中残留SO2的含量。将V L(已换算为标准状况)废气中的SO2用1%的H2O2完全吸收,吸收液用如图所示装置滴定,共消耗a mL c mol/L NaOH标准液。

①H2O2氧化SO2的化学方程式______ 。
② 废气中残留SO2的体积分数为______ 。
| 方法Ⅰ | 用碱式硫酸铝Al2(SO4)x(OH)y溶液吸收富集SO2 |
| 方法Ⅱ | 在Fe2+或Fe3+催化下,用空气(O2)将SO2氧化为H2SO4 |
① 制备Al2(SO4)x(OH)y。向Al2(SO4)3溶液中加入CaO粉末,调pH至3.6。 CaO的作用是
② 吸收:Al2(SO4)x(OH)y吸收SO2后的产物是
③ 解吸:加热②中产物,产生SO2,Al2(SO4)x(OH)y再生。
(2)方法Ⅱ中,在Fe2+催化下,SO2、O2和H2O生成H2SO4的化学方程式是
(3)方法Ⅱ中,Fe2+的催化过程可表示如下:
ⅰ:2Fe2++O2+SO2=2Fe3++SO42-
ⅱ:……
① 写出ⅱ的离子方程式:
② 下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向FeCl2溶液滴入KSCN,无变化
b.向FeCl2溶液通入少量SO2,滴入KSCN,颜色变红。
c.取b中溶液,
(4)方法Ⅱ中,催化氧化后,采用滴定法测定废气中残留SO2的含量。将V L(已换算为标准状况)废气中的SO2用1%的H2O2完全吸收,吸收液用如图所示装置滴定,共消耗a mL c mol/L NaOH标准液。

①H2O2氧化SO2的化学方程式
② 废气中残留SO2的体积分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】硫酸锰是一种应用广泛的化工产品。以某工业废锰渣(含 及少
及少 )为原料制备硫酸锰晶体
)为原料制备硫酸锰晶体 ,其工艺流程如下:
,其工艺流程如下:

回答下列问题:
(1)为加快酸浸速率和效率可采取的措施有_______ (写出两条即可)。
(2)实验室进行过滤操作用到的玻璃仪器有_______ 、_______ 、_______ ;滤渣1为 和
和_______ (填化学式)。
(3)反应Ⅰ中氧化剂和还原剂的物质的量之比为_______ ;反应Ⅱ的离子方程式为_______ 。
(4)从 溶液中得到
溶液中得到 晶体的操作为
晶体的操作为_______ 。
(5)检验滤渣2是否完全沉淀的方法是_______ 。
 及少
及少 )为原料制备硫酸锰晶体
)为原料制备硫酸锰晶体 ,其工艺流程如下:
,其工艺流程如下:
回答下列问题:
(1)为加快酸浸速率和效率可采取的措施有
(2)实验室进行过滤操作用到的玻璃仪器有
 和
和(3)反应Ⅰ中氧化剂和还原剂的物质的量之比为
(4)从
 溶液中得到
溶液中得到 晶体的操作为
晶体的操作为(5)检验滤渣2是否完全沉淀的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】三氧化钨(WO3)常川于制备特种介金、防火材料和防腐涂层。现利用白钨精矿(含80% CaWO4及少量比Fe、Zn 和Mg等的氧化物)生产WO3。设计了如图工艺流程:
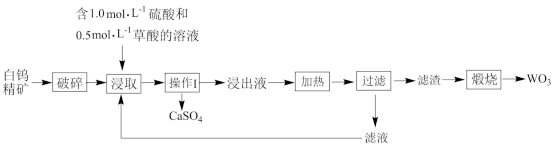
已知:①浸出液中钨(W)以[WO3C2O4.H2O]2-形式存在。
②钨酸(H2WO4)难溶于水。
③Ksp(CaSO4)=4.9×10-5; Ksp(CaC2O4)=2.3×10-9;Ka1(H2C2O4)=5.6×10-2、 Ka2(H2C2O4)=1.6×10-4。
回答下列问题:
(1)“破碎”的目的是_______ ;“破碎”后的白钨精矿粒径约为50μm,往其中加入浸取液后形成的分散系属于_______
(2)操作1的名称为_______ 。
(3)浸出液中含量最大的阳离子是_______ ;[WO3C2O4.H2O]2-中W元素的化合价为_______
(4)“加热”时发生反应的离子方程式为_______ ;煅烧”时发生反应的化学方程式为_______ 。
(5)本工艺中能循环使用的物质是_______
(6)通过计算说明“浸取”过程形成CaSO4而不能形成CaC2O4,的原因:_______

已知:①浸出液中钨(W)以[WO3C2O4.H2O]2-形式存在。
②钨酸(H2WO4)难溶于水。
③Ksp(CaSO4)=4.9×10-5; Ksp(CaC2O4)=2.3×10-9;Ka1(H2C2O4)=5.6×10-2、 Ka2(H2C2O4)=1.6×10-4。
回答下列问题:
(1)“破碎”的目的是
(2)操作1的名称为
(3)浸出液中含量最大的阳离子是
(4)“加热”时发生反应的离子方程式为
(5)本工艺中能循环使用的物质是
(6)通过计算说明“浸取”过程形成CaSO4而不能形成CaC2O4,的原因:
您最近一年使用:0次
【推荐3】Co2O3主要用作颜料、釉料及磁性材料,利用一种钴矿石(主要成分为Co2O3,含少量Fe2O3、SiO2及铝、镁、钙等金属元素的氧化物)制取Co2O3的工艺流程如图所示。

部分阳离子以氢氧化物形式沉淀时溶液pH
回答下列问题:
(1)“溶浸”过程中,可以加快反应速率和提高原料利用率的方法是_______ (写出一种即可),加入Na2SO3的作用是_______ 。
(2)“氧化”过程中金属离子与NaClO3反应的离子方程式为_______ ,由此推测还原性:Fe2+_______ Co2+(填“>”或“<”)。
(3)滤渣2的主要成分为_______ (写化学式),检验铁元素的离子已被完全沉淀的实验操作及现象;取少量待测液于试管中,_______ 。
(4)已知某温度下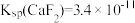 ,
,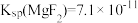 。该温度下,“沉淀除杂”时加入足量的NaF溶液可将Ca2+、Mg2+沉淀除去,若所得滤液中
。该温度下,“沉淀除杂”时加入足量的NaF溶液可将Ca2+、Mg2+沉淀除去,若所得滤液中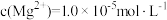 ,则滤液中c(Ca2+)为
,则滤液中c(Ca2+)为_______ (保留2位有效数字)。
(5) 在空气中充分煅烧,除得到产品外还产生了CO2,则反应中
在空气中充分煅烧,除得到产品外还产生了CO2,则反应中 与O2的化学计量数之比为
与O2的化学计量数之比为_______ 。

部分阳离子以氢氧化物形式沉淀时溶液pH
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 |
(1)“溶浸”过程中,可以加快反应速率和提高原料利用率的方法是
(2)“氧化”过程中金属离子与NaClO3反应的离子方程式为
(3)滤渣2的主要成分为
(4)已知某温度下
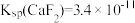 ,
,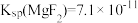 。该温度下,“沉淀除杂”时加入足量的NaF溶液可将Ca2+、Mg2+沉淀除去,若所得滤液中
。该温度下,“沉淀除杂”时加入足量的NaF溶液可将Ca2+、Mg2+沉淀除去,若所得滤液中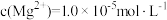 ,则滤液中c(Ca2+)为
,则滤液中c(Ca2+)为(5)
 在空气中充分煅烧,除得到产品外还产生了CO2,则反应中
在空气中充分煅烧,除得到产品外还产生了CO2,则反应中 与O2的化学计量数之比为
与O2的化学计量数之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
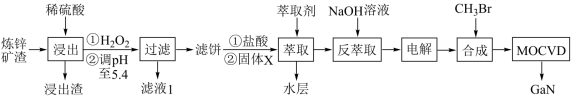
【推荐1】金属镓有“电子工业脊梁”的美誉,广泛应用于电子、航空航天、光学等领域。综合利用炼锌矿渣[主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4]获得3种金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。
②MOCVD是一种金属有机物化学气相淀积技术。
③常温下,浸出液中各离子形成氢氧化物沉淀的pH见下表。
④金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见下表。
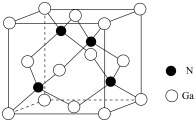
(1)GaN作为第三代半导体材料,具有耐高温、耐高电压等特性,GaN属于___________ 晶体;GaN晶体的一种立方晶胞如图所示,Ga的配位数为___________ 。___________ 。
(3)萃取前加入固体X的目的是___________ 。
(4)电解过程包括电解反萃取液制粗镓和粗镓精炼两个步骤。精炼时,以粗镓为阳极,纯镓为阴极,NaOH水溶液为电解质溶液。通电时,粗镓溶解以___________ (填离子符号)形式进入电解质溶液,并在阴极放电析出高纯镓,则阴极的电极反应方程式为___________ 。精炼时,若外电路通过0.25 mol e-时,阴极得到3.5 g的镓。则该电解装置的电解效率η=___________ (η=生成目标产物转移的电子数/转移的电子总数)。
(5)GaN可采用MOCVD(金属有机物化学气相淀积)技术制得:以合成的三甲基镓[Ga(CH3)3]为原料,使其与NH3发生反应得到GaN,该过程的化学方程式为___________ 。
②MOCVD是一种金属有机物化学气相淀积技术。
③常温下,浸出液中各离子形成氢氧化物沉淀的pH见下表。
| 金属离子 |  |  |  |  |
| 开始沉淀pH | 8.0 | 1.7 | 5.5 | 3.0 |
| 沉淀完全pH | 9.6 | 3.2 | 8.0 | 4.9 |
| 金属离子 |  |  |  |  |
| 萃取率(%) | 0 | 99 | 0 | 97~98.5 |
(1)GaN作为第三代半导体材料,具有耐高温、耐高电压等特性,GaN属于
(3)萃取前加入固体X的目的是
(4)电解过程包括电解反萃取液制粗镓和粗镓精炼两个步骤。精炼时,以粗镓为阳极,纯镓为阴极,NaOH水溶液为电解质溶液。通电时,粗镓溶解以
(5)GaN可采用MOCVD(金属有机物化学气相淀积)技术制得:以合成的三甲基镓[Ga(CH3)3]为原料,使其与NH3发生反应得到GaN,该过程的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】晶须是由高纯度单晶生长而成的微纳米级的短纤维,工业应用的晶须主要是在人工控制条件下合成。
碳酸镁晶须(MgCO3·nH2O,n = 1~5的整数)广泛应用于冶金、耐火材料及化工产品等领域。制取碳酸镁晶须的步骤如图:
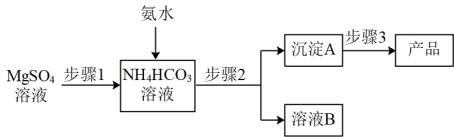
完成下列填空:
(1)步骤1必须将反应的温度控制在50℃,较好的加热方法是_______________________ ;氨水、硫酸镁、碳酸氢铵三者反应,除生成MgCO3·nH2O沉淀外,同时生成的产物还有______________________________________ 。
(2)步骤2是__________ 、洗涤,检验沉淀A已洗涤干净的方法是_____________________ 。
为测定碳酸镁晶须产品中n的值,某兴趣小组设计了如下装置,并进行了三次实验。(不考虑稀盐酸的挥发性)
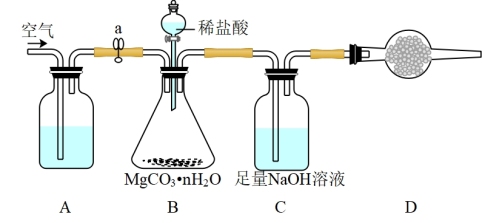
(3)装置A中盛放的溶液是_____________ 。装置D中盛放的固体是___________________ ,其作用是_________________________________ 。
(4)若三次实验测得每1.000g碳酸镁晶须产生的CO2平均值为a mol,则n值为__________________ (用含a的代数式表达)。
(5)下列选项中,会造成实验结果偏大的是____________ 。 (选填序号)
①实验开始,未先通空气,即称量装置C; ②B中反应结束后,没有继续通空气;
③缺少装置A; ④缺少装置D;
⑤装置B中稀盐酸的滴加速率过快; ⑥装置C中的NaOH溶液浓度过大。
碳酸镁晶须(MgCO3·nH2O,n = 1~5的整数)广泛应用于冶金、耐火材料及化工产品等领域。制取碳酸镁晶须的步骤如图:

完成下列填空:
(1)步骤1必须将反应的温度控制在50℃,较好的加热方法是
(2)步骤2是
为测定碳酸镁晶须产品中n的值,某兴趣小组设计了如下装置,并进行了三次实验。(不考虑稀盐酸的挥发性)

(3)装置A中盛放的溶液是
(4)若三次实验测得每1.000g碳酸镁晶须产生的CO2平均值为a mol,则n值为
(5)下列选项中,会造成实验结果偏大的是
①实验开始,未先通空气,即称量装置C; ②B中反应结束后,没有继续通空气;
③缺少装置A; ④缺少装置D;
⑤装置B中稀盐酸的滴加速率过快; ⑥装置C中的NaOH溶液浓度过大。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺如下:

[注:Al(OH)3和Cu(OH)2开始分解的温度分别为 450 ℃和 80 ℃]
(1)写出在空气中熔炼时发生反应的化学方程式:___________ 。
(2)滤渣 B 的组成是___________ ;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量则会引起的反应的离子方程式为___________ 。
(3)煅烧过程最后一步反应是CuO与Al2O3反应得到CuAlO2,该反应的另一种产物的化学式是___________ 。
(4)若银铜合金中铜的质量分数为64 %,理论上5.0 kg废料中的铜可完全转化为___________ kg CuAlO2。
(5)CuSO4溶液也可用于制备胆矾,主要操作步骤是___________ 、___________ 、过滤、洗涤和干燥。

[注:Al(OH)3和Cu(OH)2开始分解的温度分别为 450 ℃和 80 ℃]
(1)写出在空气中熔炼时发生反应的化学方程式:
(2)滤渣 B 的组成是
(3)煅烧过程最后一步反应是CuO与Al2O3反应得到CuAlO2,该反应的另一种产物的化学式是
(4)若银铜合金中铜的质量分数为64 %,理论上5.0 kg废料中的铜可完全转化为
(5)CuSO4溶液也可用于制备胆矾,主要操作步骤是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备 KClO3和 NaClO。回答下列问题:

(1)实验中制备氯气的离子方程式是______ 。
(2)c 中化学反应的离子方程式是______ ,采用冰水浴冷却的 目的是 ______ 。
(3)d 的作用是______ ,可选用试剂 ______ (填标号)。
A Na2S B NaCl C Ca(OH)2 D H2SO4
(4)已知 ClO2是更高效的消毒剂和漂白剂。若 Cl2和 ClO2作消毒剂后自身都转化为 Cl-,那么 ClO2的消毒效率(以单位质量得到电子数表示)是 Cl2的______ 倍。(保留小数点后两位)

(1)实验中制备氯气的离子方程式是
(2)c 中化学反应的离子方程式是
(3)d 的作用是
A Na2S B NaCl C Ca(OH)2 D H2SO4
(4)已知 ClO2是更高效的消毒剂和漂白剂。若 Cl2和 ClO2作消毒剂后自身都转化为 Cl-,那么 ClO2的消毒效率(以单位质量得到电子数表示)是 Cl2的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】 是重要的化学试剂,遇高温分解,与酸发生反应。实验室可通过如图所示装置制备
是重要的化学试剂,遇高温分解,与酸发生反应。实验室可通过如图所示装置制备 。
。

回答下列问题:
(1)仪器A的名称为_______ 。
(2)下列关于装置B的作用叙述正确的是_______ (填标号)
a.通过观察气泡可控制 气流速率
气流速率
b.防止发生倒吸
c.通过长颈漏斗液面升降判断B后面装置是否堵塞
(3)C中生成产品的化学反应方程式为_______ 。
(4)为保证硫代硫酸钠的产率和纯度,实验中通入的 不能过量,原因是
不能过量,原因是_______ 。
(5)为测定所得产品纯度,取m g所得产品溶于蒸馏水中配制成250mL溶液,取25.00mL置于锥形瓶中,加入2滴淀粉试剂,用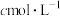 碘的标准溶液滴定,消耗标准液V mL。已知:
碘的标准溶液滴定,消耗标准液V mL。已知: 。
。
①滴定终点现象为_______ 。
②产品纯度为_______ (用m、c、V表示)。
(6)下列装置和试剂能代替E的是_______ (填标号)。
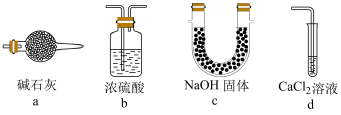
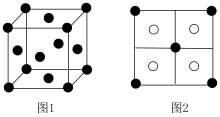
(7)硫化铜是一种难溶固体,晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,晶胞侧视图如图2所示。则与
所构成的四面体中心,晶胞侧视图如图2所示。则与 距离最近的
距离最近的 数目为
数目为_______ 。
 是重要的化学试剂,遇高温分解,与酸发生反应。实验室可通过如图所示装置制备
是重要的化学试剂,遇高温分解,与酸发生反应。实验室可通过如图所示装置制备 。
。
回答下列问题:
(1)仪器A的名称为
(2)下列关于装置B的作用叙述正确的是
a.通过观察气泡可控制
 气流速率
气流速率b.防止发生倒吸
c.通过长颈漏斗液面升降判断B后面装置是否堵塞
(3)C中生成产品的化学反应方程式为
(4)为保证硫代硫酸钠的产率和纯度,实验中通入的
 不能过量,原因是
不能过量,原因是(5)为测定所得产品纯度,取m g所得产品溶于蒸馏水中配制成250mL溶液,取25.00mL置于锥形瓶中,加入2滴淀粉试剂,用
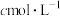 碘的标准溶液滴定,消耗标准液V mL。已知:
碘的标准溶液滴定,消耗标准液V mL。已知: 。
。①滴定终点现象为
②产品纯度为
(6)下列装置和试剂能代替E的是

(7)硫化铜是一种难溶固体,晶胞中
 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,晶胞侧视图如图2所示。则与
所构成的四面体中心,晶胞侧视图如图2所示。则与 距离最近的
距离最近的 数目为
数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钒主要用于钢铁工业,钒钢用于国防尖端工业。钒钛磁铁矿精矿中主要有用物相为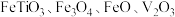 ,主要杂质为
,主要杂质为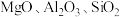 和
和 ,用钒钛磁铁矿精矿制备五氧化二钒的流程如图所示:
,用钒钛磁铁矿精矿制备五氧化二钒的流程如图所示:
(1) 中V的化合价为
中V的化合价为____________ 价;基态V原子的价层电子排布式为______________ 。
(2)在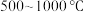 进行钠化焙烧时,钒转化为水溶性的偏钒酸钠
进行钠化焙烧时,钒转化为水溶性的偏钒酸钠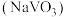 ,写出“焙烧”时生成偏钒酸钠的化学方程式:
,写出“焙烧”时生成偏钒酸钠的化学方程式:______________ 。
(3)常温下,在钒液中加入 和
和 溶液,通过两者的比例不同,调节适当的
溶液,通过两者的比例不同,调节适当的 值进行沉钒,“沉钒”过程中不涉及氧化还原反应,“沉钒”时发生反应的离子方程式为
值进行沉钒,“沉钒”过程中不涉及氧化还原反应,“沉钒”时发生反应的离子方程式为_______________ ;结合图中信息,获得偏钒酸铵晶体的最佳温度和 为
为_______________ 。 ,则晶胞中距离A点最远的白球的坐标参数为
,则晶胞中距离A点最远的白球的坐标参数为_______________ ;若晶胞的棱长为 ,设阿伏加德罗常数的数值为
,设阿伏加德罗常数的数值为 ,则该氮化钛的密度为
,则该氮化钛的密度为________________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。 发生还原反应生成
发生还原反应生成 ,写出该电池正极的电极反应式:
,写出该电池正极的电极反应式:________________ 。
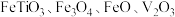 ,主要杂质为
,主要杂质为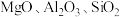 和
和 ,用钒钛磁铁矿精矿制备五氧化二钒的流程如图所示:
,用钒钛磁铁矿精矿制备五氧化二钒的流程如图所示: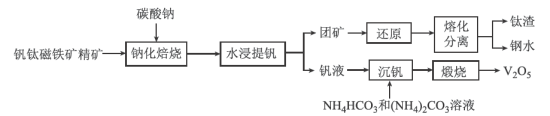
(1)
 中V的化合价为
中V的化合价为(2)在
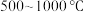 进行钠化焙烧时,钒转化为水溶性的偏钒酸钠
进行钠化焙烧时,钒转化为水溶性的偏钒酸钠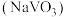 ,写出“焙烧”时生成偏钒酸钠的化学方程式:
,写出“焙烧”时生成偏钒酸钠的化学方程式:(3)常温下,在钒液中加入
 和
和 溶液,通过两者的比例不同,调节适当的
溶液,通过两者的比例不同,调节适当的 值进行沉钒,“沉钒”过程中不涉及氧化还原反应,“沉钒”时发生反应的离子方程式为
值进行沉钒,“沉钒”过程中不涉及氧化还原反应,“沉钒”时发生反应的离子方程式为 为
为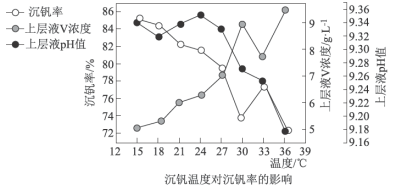
 ,则晶胞中距离A点最远的白球的坐标参数为
,则晶胞中距离A点最远的白球的坐标参数为 ,设阿伏加德罗常数的数值为
,设阿伏加德罗常数的数值为 ,则该氮化钛的密度为
,则该氮化钛的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。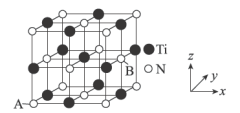
 发生还原反应生成
发生还原反应生成 ,写出该电池正极的电极反应式:
,写出该电池正极的电极反应式:
您最近一年使用:0次



