钒主要用于钢铁工业,钒钢用于国防尖端工业。钒钛磁铁矿精矿中主要有用物相为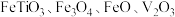 ,主要杂质为
,主要杂质为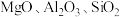 和
和 ,用钒钛磁铁矿精矿制备五氧化二钒的流程如图所示:
,用钒钛磁铁矿精矿制备五氧化二钒的流程如图所示:
(1) 中V的化合价为
中V的化合价为____________ 价;基态V原子的价层电子排布式为______________ 。
(2)在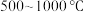 进行钠化焙烧时,钒转化为水溶性的偏钒酸钠
进行钠化焙烧时,钒转化为水溶性的偏钒酸钠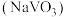 ,写出“焙烧”时生成偏钒酸钠的化学方程式:
,写出“焙烧”时生成偏钒酸钠的化学方程式:______________ 。
(3)常温下,在钒液中加入 和
和 溶液,通过两者的比例不同,调节适当的
溶液,通过两者的比例不同,调节适当的 值进行沉钒,“沉钒”过程中不涉及氧化还原反应,“沉钒”时发生反应的离子方程式为
值进行沉钒,“沉钒”过程中不涉及氧化还原反应,“沉钒”时发生反应的离子方程式为_______________ ;结合图中信息,获得偏钒酸铵晶体的最佳温度和 为
为_______________ 。 ,则晶胞中距离A点最远的白球的坐标参数为
,则晶胞中距离A点最远的白球的坐标参数为_______________ ;若晶胞的棱长为 ,设阿伏加德罗常数的数值为
,设阿伏加德罗常数的数值为 ,则该氮化钛的密度为
,则该氮化钛的密度为________________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。 发生还原反应生成
发生还原反应生成 ,写出该电池正极的电极反应式:
,写出该电池正极的电极反应式:________________ 。
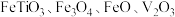 ,主要杂质为
,主要杂质为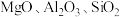 和
和 ,用钒钛磁铁矿精矿制备五氧化二钒的流程如图所示:
,用钒钛磁铁矿精矿制备五氧化二钒的流程如图所示: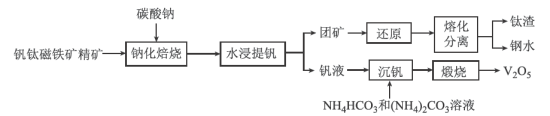
(1)
 中V的化合价为
中V的化合价为(2)在
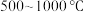 进行钠化焙烧时,钒转化为水溶性的偏钒酸钠
进行钠化焙烧时,钒转化为水溶性的偏钒酸钠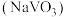 ,写出“焙烧”时生成偏钒酸钠的化学方程式:
,写出“焙烧”时生成偏钒酸钠的化学方程式:(3)常温下,在钒液中加入
 和
和 溶液,通过两者的比例不同,调节适当的
溶液,通过两者的比例不同,调节适当的 值进行沉钒,“沉钒”过程中不涉及氧化还原反应,“沉钒”时发生反应的离子方程式为
值进行沉钒,“沉钒”过程中不涉及氧化还原反应,“沉钒”时发生反应的离子方程式为 为
为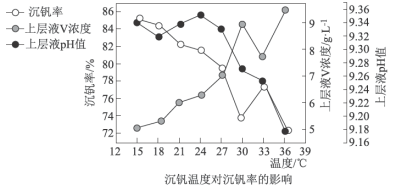
 ,则晶胞中距离A点最远的白球的坐标参数为
,则晶胞中距离A点最远的白球的坐标参数为 ,设阿伏加德罗常数的数值为
,设阿伏加德罗常数的数值为 ,则该氮化钛的密度为
,则该氮化钛的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。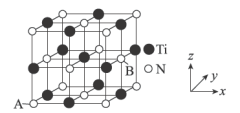
 发生还原反应生成
发生还原反应生成 ,写出该电池正极的电极反应式:
,写出该电池正极的电极反应式:
更新时间:2024-05-24 22:54:08
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】(1)锂空气电池比传统的锂离子电池拥有更强的蓄电能力,是传统锂离子电池容量的10倍,其工作原理示意图如图所示。
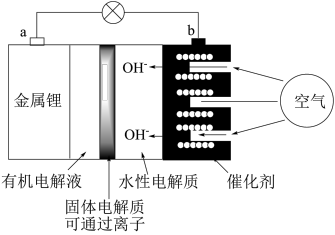
放电时,b电极为电源的极_______ ,电极反应式为_______ 。
(2)汽车尾气中 、
、 在一定条件下可发生反应
在一定条件下可发生反应 ,定温度下,向容积固定的
,定温度下,向容积固定的 密闭容器中充入一定量的
密闭容器中充入一定量的 和
和 ,
, 的物质的量随时间的变化曲线如图所示。
的物质的量随时间的变化曲线如图所示。
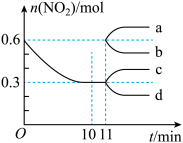
① 内该反应的平均速率
内该反应的平均速率
_______ ,从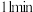 起其他条件不变,压缩容器的容积变为
起其他条件不变,压缩容器的容积变为 ,则
,则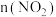 的变化曲线可能为图中的
的变化曲线可能为图中的_______ (填字母)。
②恒温恒容条件下,不能说明该反应已经达到平衡状态的是_______ (填序号)。
a.容器内混合气体颜色不再变化 b.容器内的压强保持不变 c.容器内混合气体密度保持不变

放电时,b电极为电源的极
(2)汽车尾气中
 、
、 在一定条件下可发生反应
在一定条件下可发生反应 ,定温度下,向容积固定的
,定温度下,向容积固定的 密闭容器中充入一定量的
密闭容器中充入一定量的 和
和 ,
, 的物质的量随时间的变化曲线如图所示。
的物质的量随时间的变化曲线如图所示。
①
 内该反应的平均速率
内该反应的平均速率
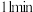 起其他条件不变,压缩容器的容积变为
起其他条件不变,压缩容器的容积变为 ,则
,则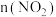 的变化曲线可能为图中的
的变化曲线可能为图中的②恒温恒容条件下,不能说明该反应已经达到平衡状态的是
a.容器内混合气体颜色不再变化 b.容器内的压强保持不变 c.容器内混合气体密度保持不变
您最近一年使用:0次
【推荐2】利用甲醇(CH3OH)制备一些高附加值产品,是目前研究的热点。
(1)甲醇和水蒸气经催化重整可制得氢气,反应主要过程如下:
反应I. CH3OH(g)+H2O(g) 3H2(g)+CO2(g) ΔH1
3H2(g)+CO2(g) ΔH1
反应II. H2(g)+CO2(g) H2O(g)+CO(g) ΔH2=a kJ·mol-1
H2O(g)+CO(g) ΔH2=a kJ·mol-1
反应III. CH3OH(g) 2H2(g)+CO(g) ΔH3=b kJ·mol-1
2H2(g)+CO(g) ΔH3=b kJ·mol-1
①ΔH1=_______ kJ·mol-1。
②工业上采用CaO吸附增强制氢的方法,可以有效提高反应I氢气的产率,如图,请分析加入CaO提高氢气产率的原因:_______ 。

(2)将CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应: CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如图。
CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如图。
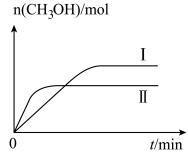
①曲线I、II对应的平衡常数大小关系为KⅠ_______ (填“>”“=”或“<”)KⅡ。
②一定温度下,在容积为1 L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
若甲中平衡后气体的压强为开始的0.8倍,则乙容器起始时反应速率v正_______ (填“>”“<”或“=”)v逆。
③一定温度下,此反应在恒压容器中进行,不能判断该反应达到化学平衡状态的依据是_______ 。
a.容器中压强不变
b.H2的体积分数不变
c.c(H2)=3c(CH3OH)
d.容器中密度不变
e.2个C=O断裂的同时有3个H—H生成
(3)已知电离常数HCN:Ka=4.9×10-10,H2CO3:Ka1=4.3×10-7,Ka2=5.6×10-11,则向KCN溶液中通入少量CO2时的离子方程式为_______ 。
(4)利用人工光合作用,借助太阳能使CO2和H2O转化为HCOOH,如图所示,在催化剂b表面发生的电极反应为_______ 。

(1)甲醇和水蒸气经催化重整可制得氢气,反应主要过程如下:
反应I. CH3OH(g)+H2O(g)
 3H2(g)+CO2(g) ΔH1
3H2(g)+CO2(g) ΔH1反应II. H2(g)+CO2(g)
 H2O(g)+CO(g) ΔH2=a kJ·mol-1
H2O(g)+CO(g) ΔH2=a kJ·mol-1反应III. CH3OH(g)
 2H2(g)+CO(g) ΔH3=b kJ·mol-1
2H2(g)+CO(g) ΔH3=b kJ·mol-1①ΔH1=
②工业上采用CaO吸附增强制氢的方法,可以有效提高反应I氢气的产率,如图,请分析加入CaO提高氢气产率的原因:

(2)将CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应: CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如图。
CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如图。
①曲线I、II对应的平衡常数大小关系为KⅠ
②一定温度下,在容积为1 L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1 mol CO2、3 mol H2 | 1molCO2、1molH2、1molCH3OH(g)、1 mol H2O(g) |
③一定温度下,此反应在恒压容器中进行,不能判断该反应达到化学平衡状态的依据是
a.容器中压强不变
b.H2的体积分数不变
c.c(H2)=3c(CH3OH)
d.容器中密度不变
e.2个C=O断裂的同时有3个H—H生成
(3)已知电离常数HCN:Ka=4.9×10-10,H2CO3:Ka1=4.3×10-7,Ka2=5.6×10-11,则向KCN溶液中通入少量CO2时的离子方程式为
(4)利用人工光合作用,借助太阳能使CO2和H2O转化为HCOOH,如图所示,在催化剂b表面发生的电极反应为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】能量转化是化学变化的重要特征,按要求回答下列问题:
(1)已知: 键的键能为
键的键能为 ,
, 键的键能为
键的键能为 ,
, 键的键能为
键的键能为 则反应
则反应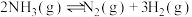 中,理论上消耗
中,理论上消耗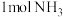
___________ (填“吸收”或“放出”)___________ kJ热量。
(2)把a、b、c、d四种金属片浸入稀硫酸中,用导线两两相连可以组成各种原电池。若a、b相连,a为正极:c、d相连,c为负极:a﹑c相连,c上有气泡逸出:b、d相连,b质量减小,则四种金属的活动性由强到弱顺序为:___________ 。
(3)中国科学院长春应用化学研究所曾在甲烷( )燃料电池技术方面获得重大突破。甲烷燃料电池工作的原理如图所示,甲烷燃料电池采用铂作电板催化剂,电池中的质子交换膜只允许质子(
)燃料电池技术方面获得重大突破。甲烷燃料电池工作的原理如图所示,甲烷燃料电池采用铂作电板催化剂,电池中的质子交换膜只允许质子( )和水分子通过。其工作原理的示意图如下,请回答下列问题:
)和水分子通过。其工作原理的示意图如下,请回答下列问题:
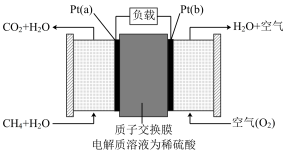
① 的电子式为
的电子式为___________ ,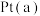 电极反应式为
电极反应式为___________
②电解质溶液中的 向
向___________ (填“a”或“b”)极移动,电子流出的电极是___________ (填“a”或“b”)极。
③该电池工作时消耗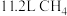 (标准状况下),假设电池的能量转化率为80%,则电路中通过
(标准状况下),假设电池的能量转化率为80%,则电路中通过___________ mol电子。
(1)已知:
 键的键能为
键的键能为 ,
, 键的键能为
键的键能为 ,
, 键的键能为
键的键能为 则反应
则反应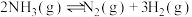 中,理论上消耗
中,理论上消耗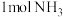
(2)把a、b、c、d四种金属片浸入稀硫酸中,用导线两两相连可以组成各种原电池。若a、b相连,a为正极:c、d相连,c为负极:a﹑c相连,c上有气泡逸出:b、d相连,b质量减小,则四种金属的活动性由强到弱顺序为:
(3)中国科学院长春应用化学研究所曾在甲烷(
 )燃料电池技术方面获得重大突破。甲烷燃料电池工作的原理如图所示,甲烷燃料电池采用铂作电板催化剂,电池中的质子交换膜只允许质子(
)燃料电池技术方面获得重大突破。甲烷燃料电池工作的原理如图所示,甲烷燃料电池采用铂作电板催化剂,电池中的质子交换膜只允许质子( )和水分子通过。其工作原理的示意图如下,请回答下列问题:
)和水分子通过。其工作原理的示意图如下,请回答下列问题:
①
 的电子式为
的电子式为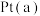 电极反应式为
电极反应式为②电解质溶液中的
 向
向③该电池工作时消耗
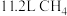 (标准状况下),假设电池的能量转化率为80%,则电路中通过
(标准状况下),假设电池的能量转化率为80%,则电路中通过
您最近一年使用:0次
【推荐1】中科院大连化物所的科学家在乙酰酮修饰锰氧化物L酸催化胺选择氧化方面的研究取得新进展。回答下列问题:
(1)Mn元素的价层电子排布式为_______ ;Mn元素的一种配合物K3[Mn(CN)6]具有反磁性,配体CN-的电子式为_______ 。
(2)乙腈(CH3CN)分子中碳原子的杂化类型有_______ ,该分子中σ键和π键的个数比为_______ 。
(3)苯胺(C6H5NH2)的晶体类型是_______ ,苯胺与甲苯的相对分子质量相近,但苯胺的熔、沸点分别高于甲苯的熔、沸点,原因是_______ 。
(4)锰的某种氧化物的晶胞结构如图所示:

该锰元素的氧化物化学式为_______ ,晶体的密度为_______  (用含a、b和NA的代数式表示,NA为阿伏加德罗常数的值)。
(用含a、b和NA的代数式表示,NA为阿伏加德罗常数的值)。
(1)Mn元素的价层电子排布式为
(2)乙腈(CH3CN)分子中碳原子的杂化类型有
(3)苯胺(C6H5NH2)的晶体类型是
(4)锰的某种氧化物的晶胞结构如图所示:

该锰元素的氧化物化学式为
 (用含a、b和NA的代数式表示,NA为阿伏加德罗常数的值)。
(用含a、b和NA的代数式表示,NA为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】2024年2月24日,中国载人月球探测任务新飞行器命名为“梦舟”,月面着陆器命名为“揽月”,登陆月球成为中国人探索太空的下一个目标。月壤中存在天然的铜、锌、铁等矿物颗粒,回答下列问题:
(1)基态 原子的价层电子排布式为
原子的价层电子排布式为___________ 。
(2)配合物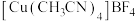 中,
中,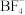 的空间构型是
的空间构型是___________ 。
(3) 与
与 形成的某种晶体的晶胞如下图所示,该晶胞中
形成的某种晶体的晶胞如下图所示,该晶胞中 微粒的配位数为
微粒的配位数为___________ ,该化合物的化学式为___________ 。
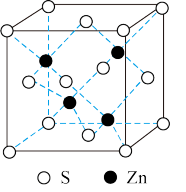
写出该化合物与稀硫酸反应的离子方程式___________ 。
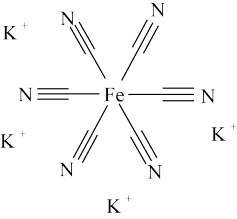
(4)亚铁氰化钾别名黄血盐,化学式: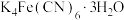 ,加入食盐中可防止食盐板结。其中
,加入食盐中可防止食盐板结。其中 三种元素的电负性由小到大顺序为
三种元素的电负性由小到大顺序为___________ ,其不含结晶水的盐结构如下图所示,其中 原子的杂化轨道类型为
原子的杂化轨道类型为___________ 杂化。
(1)基态
 原子的价层电子排布式为
原子的价层电子排布式为(2)配合物
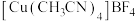 中,
中,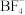 的空间构型是
的空间构型是(3)
 与
与 形成的某种晶体的晶胞如下图所示,该晶胞中
形成的某种晶体的晶胞如下图所示,该晶胞中 微粒的配位数为
微粒的配位数为
写出该化合物与稀硫酸反应的离子方程式
(4)亚铁氰化钾别名黄血盐,化学式:
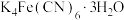 ,加入食盐中可防止食盐板结。其中
,加入食盐中可防止食盐板结。其中 三种元素的电负性由小到大顺序为
三种元素的电负性由小到大顺序为 原子的杂化轨道类型为
原子的杂化轨道类型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】 和
和 都是常见的氧化剂。
都是常见的氧化剂。
(1) 的基态原子的核外电子排布式为
的基态原子的核外电子排布式为_______ , 的基态原子核外电子有
的基态原子核外电子有_______ 种运动状态。
(2) 是石油化工中重要的催化剂之一,可催化异丙苯裂化生成苯和丙烯。
是石油化工中重要的催化剂之一,可催化异丙苯裂化生成苯和丙烯。 丙烯分子中含有
丙烯分子中含有 键与
键与 键数目之比为
键数目之比为_______ ,丙烯分子中碳原子的杂化轨道类型为_______ 。
(3)H、O、 三种元素的电负性按由大到小的顺序为
三种元素的电负性按由大到小的顺序为_______ (用元素符号表示)。
(4) 是一种弱酸,其结构式为
是一种弱酸,其结构式为_______ 。
(5) 的氧化物有多种,其中五氧化铬,常温下为蓝色结晶,化学式为
的氧化物有多种,其中五氧化铬,常温下为蓝色结晶,化学式为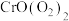 ,也可写成
,也可写成 ,则其中过氧键的数目为
,则其中过氧键的数目为_______ 。
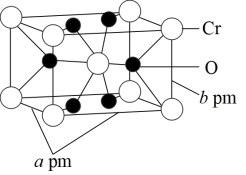
(6) 的某种氧化物晶体的晶胞结构如图所示,其化学式为
的某种氧化物晶体的晶胞结构如图所示,其化学式为_______ .设阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为_______  。
。
 和
和 都是常见的氧化剂。
都是常见的氧化剂。(1)
 的基态原子的核外电子排布式为
的基态原子的核外电子排布式为 的基态原子核外电子有
的基态原子核外电子有(2)
 是石油化工中重要的催化剂之一,可催化异丙苯裂化生成苯和丙烯。
是石油化工中重要的催化剂之一,可催化异丙苯裂化生成苯和丙烯。 丙烯分子中含有
丙烯分子中含有 键与
键与 键数目之比为
键数目之比为(3)H、O、
 三种元素的电负性按由大到小的顺序为
三种元素的电负性按由大到小的顺序为(4)
 是一种弱酸,其结构式为
是一种弱酸,其结构式为(5)
 的氧化物有多种,其中五氧化铬,常温下为蓝色结晶,化学式为
的氧化物有多种,其中五氧化铬,常温下为蓝色结晶,化学式为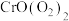 ,也可写成
,也可写成 ,则其中过氧键的数目为
,则其中过氧键的数目为(6)
 的某种氧化物晶体的晶胞结构如图所示,其化学式为
的某种氧化物晶体的晶胞结构如图所示,其化学式为 ,则该晶体的密度为
,则该晶体的密度为 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】硫代硫酸钠晶体(Na2S2O3·5H2O,M=248g∙mol−1)是重要的化工原料,易溶于水,不溶于乙醇,具有较强的还原性和配位能力,在中性或碱性环境中稳定。某兴趣小组用如图装置制备 。
。

I.制备Na2S2O3∙5H2O
合成反应: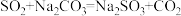 、
、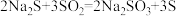 、
、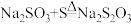
实验步骤:装置A制备的 通入装置C中的混合溶液,加热、搅拌,至溶液pH约为8时,停止通入
通入装置C中的混合溶液,加热、搅拌,至溶液pH约为8时,停止通入 气体,得产品混合溶液。产品混合溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到
气体,得产品混合溶液。产品混合溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到 产品。
产品。
(1)装置B中长颈漏斗的作用是__ ,另外可以通过装置B观察SO2的生成速率,其中的液体可以选择_ 。
a.浓H2SO4 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaCl溶液
(2)仪器C的名称是___ ,该实验一般控制在碱性环境下进行,否则产品发黄,用离子方程式表示其原因:__ 。
(3)下列说法正确的是____ 。
A.快速蒸发溶液中水分,可得较大晶体颗粒
B.蒸发浓缩至溶液表面出现晶膜时,停止加热
C.冷却结晶后的固液混合物中加入乙醇可提高产率
D.可选用冷的Na2CO3溶液作洗涤剂
II.测定产品纯度
利用K2Cr2O7标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
(4)称取1.5000g某硫代硫酸钠晶体样品溶于水配成100.00mL溶液,取0.00900mol∙L−1的K2Cr2O7标准溶液25.00mL,硫酸酸化后加入过量KI,发生反应: +6I-+14H+=3I2+2Cr3++7H2O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2
+6I-+14H+=3I2+2Cr3++7H2O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2 =
= +2I-。加入淀粉溶液作为指示剂,继续滴定至终点。平行滴定3次,样品溶液的平均用量为24.80mL,则样品纯度为
+2I-。加入淀粉溶液作为指示剂,继续滴定至终点。平行滴定3次,样品溶液的平均用量为24.80mL,则样品纯度为________ %(保留1位小数)。
III. Na2S2O3的应用
(5)Na2S2O3溶液常用作定影剂,溶去胶片上未感光的AgBr,该反应的离子方程式_______ 。
 。
。
I.制备Na2S2O3∙5H2O
合成反应:
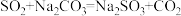 、
、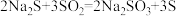 、
、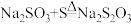
实验步骤:装置A制备的
 通入装置C中的混合溶液,加热、搅拌,至溶液pH约为8时,停止通入
通入装置C中的混合溶液,加热、搅拌,至溶液pH约为8时,停止通入 气体,得产品混合溶液。产品混合溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到
气体,得产品混合溶液。产品混合溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到 产品。
产品。(1)装置B中长颈漏斗的作用是
a.浓H2SO4 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaCl溶液
(2)仪器C的名称是
(3)下列说法正确的是
A.快速蒸发溶液中水分,可得较大晶体颗粒
B.蒸发浓缩至溶液表面出现晶膜时,停止加热
C.冷却结晶后的固液混合物中加入乙醇可提高产率
D.可选用冷的Na2CO3溶液作洗涤剂
II.测定产品纯度
利用K2Cr2O7标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
(4)称取1.5000g某硫代硫酸钠晶体样品溶于水配成100.00mL溶液,取0.00900mol∙L−1的K2Cr2O7标准溶液25.00mL,硫酸酸化后加入过量KI,发生反应:
 +6I-+14H+=3I2+2Cr3++7H2O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2
+6I-+14H+=3I2+2Cr3++7H2O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2 =
= +2I-。加入淀粉溶液作为指示剂,继续滴定至终点。平行滴定3次,样品溶液的平均用量为24.80mL,则样品纯度为
+2I-。加入淀粉溶液作为指示剂,继续滴定至终点。平行滴定3次,样品溶液的平均用量为24.80mL,则样品纯度为III. Na2S2O3的应用
(5)Na2S2O3溶液常用作定影剂,溶去胶片上未感光的AgBr,该反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】实验室以废铜为原料制取碱式碳酸铜【Cu2(OH)2CO3】的过程如下:
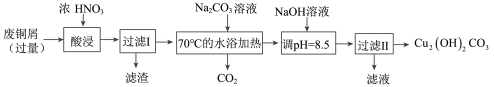
完成下列填空:
(1)酸浸中产生的气体是_________ (填化学式)。
(2)检验过滤Ⅱ的沉淀是否洗净的方法是________ 。
(3)从实验流程中可看出影响产品生成的因素有多种,请写出其中两个:___________ , 并任选其中一个因素,说明其原因___________ 。
(4)CuSO4溶液和纯碱溶液混合同样也可以制得Cu2(OH)2CO3,写出该反应的化学方程式:______ 。
(5)产品中Cu含量的测定步骤是:称取mg样品,用适量稀硫酸完全溶解,加水稀释,调节溶液为中性或弱酸性,再加入过量的KI-淀粉溶液后,用c mol/L的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液v mL。实验中反应的离子方程式为2Cu2++4I-→2CuI(白色)↓+I2;I2+2S2O32-→2I-+S4O62-。
(i)样品溶于稀硫酸后,需加水稀释,控制溶液为中性或弱酸性,其原因是________ 。
(ii)产品中Cu的含量为__________________ (用含m、c、v的代数式表示)。

完成下列填空:
(1)酸浸中产生的气体是
(2)检验过滤Ⅱ的沉淀是否洗净的方法是
(3)从实验流程中可看出影响产品生成的因素有多种,请写出其中两个:
(4)CuSO4溶液和纯碱溶液混合同样也可以制得Cu2(OH)2CO3,写出该反应的化学方程式:
(5)产品中Cu含量的测定步骤是:称取mg样品,用适量稀硫酸完全溶解,加水稀释,调节溶液为中性或弱酸性,再加入过量的KI-淀粉溶液后,用c mol/L的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液v mL。实验中反应的离子方程式为2Cu2++4I-→2CuI(白色)↓+I2;I2+2S2O32-→2I-+S4O62-。
(i)样品溶于稀硫酸后,需加水稀释,控制溶液为中性或弱酸性,其原因是
(ii)产品中Cu的含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。某兴趣小组 用高钛渣(主要成分为TiO2,含少量Fe2O3和二氧化硅) 为原料制备纳米TiO2,流程如下:

已知:①TiCl4沸点136.4℃,极易水解: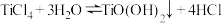
②
③TiO2化学性质稳定,是偏酸性的两性氧化物,不溶于水、有机物,也不溶于稀酸、稀碱等。
请回答:
(1)步骤Ⅰ,小火加热的目的是______ 。
(2)下列说法正确的是______ 。
A.步骤Ⅱ,发生的主要反应为
B.步骤Ⅲ,可以用油浴加热的方法精馏获得TiCl4
C.步骤Ⅳ,为加快反应速率,最好用浓NaOH溶液代替氨水
D.步骤Ⅳ,为提高产率,反应后的容器在后续操作中需要洗涤并转移利用
(3)步骤Ⅳ,调pH的目的是______ ;为制得纳米TiO2,后续操作步骤Ⅴ是______ 。
(4)为了测定TiO2产品的纯度,可采用氧化还原滴定法。
①一定条件下,将TiO2溶解并还原为Ti3+,再用硫酸酸化的KMnO4标准溶液滴定Ti3+至全部生成Ti4+。从下列选项中选出合理的操作并排序:______ →______ →取酸式滴定管检漏、水洗并用KMnO4标准溶液润洗→______ →______ →______ →重复滴定,记录数据,并处理。
a.向滴定管中注入KMnO4标准溶液
b.量取25.00 mL待测溶液于锥形瓶
c.往锥形瓶中滴入几滴甲基橙溶液
d.滴定至不再有气泡产生,记录读数V2
e.滴定至溶液呈微红色,30 s内不褪色,记录读数V2
f.称取m g TiO2,溶解后配成100 mL待测溶液
g.排气泡后调节液面,记录数据V1
②酸化 溶液的酸还可选择下列
溶液的酸还可选择下列______ ;
A.HCl B.CH3COOH C.H2C2O4
如果选择上述其它酸,测定结果将______ (填“偏高”、“偏低”或“无影响”)。

已知:①TiCl4沸点136.4℃,极易水解:
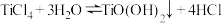
②

③TiO2化学性质稳定,是偏酸性的两性氧化物,不溶于水、有机物,也不溶于稀酸、稀碱等。
请回答:
(1)步骤Ⅰ,小火加热的目的是
(2)下列说法正确的是
A.步骤Ⅱ,发生的主要反应为

B.步骤Ⅲ,可以用油浴加热的方法精馏获得TiCl4
C.步骤Ⅳ,为加快反应速率,最好用浓NaOH溶液代替氨水
D.步骤Ⅳ,为提高产率,反应后的容器在后续操作中需要洗涤并转移利用
(3)步骤Ⅳ,调pH的目的是
(4)为了测定TiO2产品的纯度,可采用氧化还原滴定法。
①一定条件下,将TiO2溶解并还原为Ti3+,再用硫酸酸化的KMnO4标准溶液滴定Ti3+至全部生成Ti4+。从下列选项中选出合理的操作并排序:
a.向滴定管中注入KMnO4标准溶液
b.量取25.00 mL待测溶液于锥形瓶
c.往锥形瓶中滴入几滴甲基橙溶液
d.滴定至不再有气泡产生,记录读数V2
e.滴定至溶液呈微红色,30 s内不褪色,记录读数V2
f.称取m g TiO2,溶解后配成100 mL待测溶液
g.排气泡后调节液面,记录数据V1
②酸化
 溶液的酸还可选择下列
溶液的酸还可选择下列A.HCl B.CH3COOH C.H2C2O4
如果选择上述其它酸,测定结果将
您最近一年使用:0次



