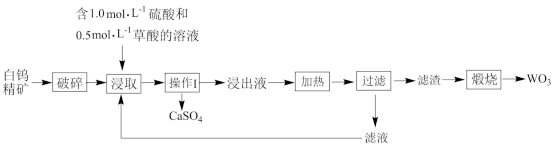
三氧化钨(WO3)常川于制备特种介金、防火材料和防腐涂层。现利用白钨精矿(含80% CaWO4及少量比Fe、Zn 和Mg等的氧化物)生产WO3。设计了如图工艺流程:
已知:①浸出液中钨(W)以[WO3C2O4.H2O]2-形式存在。
②钨酸(H2WO4)难溶于水。
③Ksp(CaSO4)=4.9×10-5; Ksp(CaC2O4)=2.3×10-9;Ka1(H2C2O4)=5.6×10-2、 Ka2(H2C2O4)=1.6×10-4。
回答下列问题:
(1)“破碎”的目的是_______ ;“破碎”后的白钨精矿粒径约为50μm,往其中加入浸取液后形成的分散系属于_______
(2)操作1的名称为_______ 。
(3)浸出液中含量最大的阳离子是_______ ;[WO3C2O4.H2O]2-中W元素的化合价为_______
(4)“加热”时发生反应的离子方程式为_______ ;煅烧”时发生反应的化学方程式为_______ 。
(5)本工艺中能循环使用的物质是_______
(6)通过计算说明“浸取”过程形成CaSO4而不能形成CaC2O4,的原因:_______

已知:①浸出液中钨(W)以[WO3C2O4.H2O]2-形式存在。
②钨酸(H2WO4)难溶于水。
③Ksp(CaSO4)=4.9×10-5; Ksp(CaC2O4)=2.3×10-9;Ka1(H2C2O4)=5.6×10-2、 Ka2(H2C2O4)=1.6×10-4。
回答下列问题:
(1)“破碎”的目的是
(2)操作1的名称为
(3)浸出液中含量最大的阳离子是
(4)“加热”时发生反应的离子方程式为
(5)本工艺中能循环使用的物质是
(6)通过计算说明“浸取”过程形成CaSO4而不能形成CaC2O4,的原因:
2021·广东·一模 查看更多[3]
(已下线)二轮拔高卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)(已下线)押山东卷第16题 化工流程综合题-备战2021年高考化学临考题号押题(山东卷)广东省2021届普通高中学业水平选择考模拟测试(一)化学试题
更新时间:2021-04-05 17:23:10
|
相似题推荐
【推荐1】硫酸锌是制造锌钡白和锌盐的主要原料,也可用作木材的防腐剂等。用氧化锌烟尘(主要成分为ZnO,还含有少量PbO、CuO、Fe2O3、FeO等)生产ZnSO4∙7H2O的流程如下:

有关金属离子[c(Mn+)=0.1 mol/L]形成氢氧化物沉淀的pH范围如下:
(1)“酸浸”时用的稀酸是_______ 。
(2)“氧化”时的离子方程式为_______ ,加入ZnO除杂时溶液的pH控制范围是_______ ~5.0。
(3)滤渣3含有锌和_______ (写化学式);由滤液得到ZnSO4∙7H2O的操作是_______ 、洗涤、干燥。
(4)取14.35 g ZnSO4∙7H2O (287 g/mol)加热至不同温度,剩余固体的质量如下表:
则680℃时剩余固体的化学式为_______(填字母,括号内为摩尔质量)。

有关金属离子[c(Mn+)=0.1 mol/L]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cu2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 4.7 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 6.7 |
(2)“氧化”时的离子方程式为
(3)滤渣3含有锌和
(4)取14.35 g ZnSO4∙7H2O (287 g/mol)加热至不同温度,剩余固体的质量如下表:
| 温度/℃ | 100 | 250 | 680 | 930 |
| 质量/g | 8.95 | 8.05 | 6.72 | 4.05 |
A.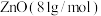 | B.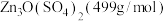 |
C.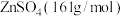 | D.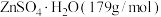 |
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】以菱镁矿(主要成分为MgCO3,含少量SiO2、Fe2O3和A12O3)为原料制备高纯镁砂的工艺流程如下:
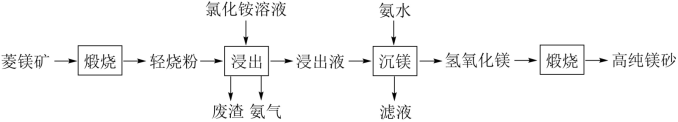
(注:轻烧粉为多种氧化物的混合物)
(1)废渣中除含Fe(OH)3、Al(OH)3外,还有_______ 。
(2)“浸出”时生成Mg2+的离子方程式为_______ 。
(3)已知常温时Ksp[Mg(OH)2]=1.0×10-11,“沉镁”时为了使Mg2+完全沉淀(浓度小于1.0×10-5mol/L),溶液的pH应不低于_______ 。
(4)氢氧化镁煅烧前要洗涤干净,证明其是否洗涤干净的操作为_______ 。
(5)上述流程中可循环使用的物质有_______ (填化学式)。
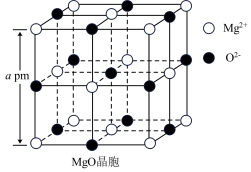
(6)氧化镁形成的一种立方晶胞如图所示。已知晶胞参数为apm,该晶胞中Mg2+的配位数为_______ ,晶体的密度为_______ g/cm3(NA为阿伏加德罗常数的值,用含a和NA的代数式表示)。

(注:轻烧粉为多种氧化物的混合物)
(1)废渣中除含Fe(OH)3、Al(OH)3外,还有
(2)“浸出”时生成Mg2+的离子方程式为
(3)已知常温时Ksp[Mg(OH)2]=1.0×10-11,“沉镁”时为了使Mg2+完全沉淀(浓度小于1.0×10-5mol/L),溶液的pH应不低于
(4)氢氧化镁煅烧前要洗涤干净,证明其是否洗涤干净的操作为
(5)上述流程中可循环使用的物质有
(6)氧化镁形成的一种立方晶胞如图所示。已知晶胞参数为apm,该晶胞中Mg2+的配位数为

您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】锰酸锂离子蓄电池是第二代锂离子动力电池。一种以软锰矿浆(主要成分为 ,含少量
,含少量 、FeO、
、FeO、 、
、 等杂质)为原料制备锰酸锂的流程如图所示。
等杂质)为原料制备锰酸锂的流程如图所示。
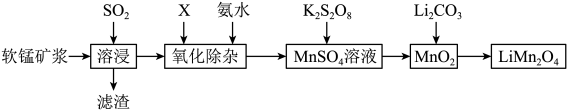
(1) 的最外层电子排布式为
的最外层电子排布式为___________
(2)溶浸过程中为提高 吸收率可采取的措施有
吸收率可采取的措施有___________ (填序号)。
a.粉碎矿石
b.不断搅拌,使 和软锰矿浆充分接触
和软锰矿浆充分接触
c.减小通入 的流速
的流速
d.升高温度
(3)已知:室温下,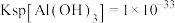 ,
,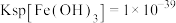 ,pH=7.1时
,pH=7.1时 开始沉淀。氧化除杂时(室温)除去
开始沉淀。氧化除杂时(室温)除去 溶液中的
溶液中的 、
、 (使其浓度小于
(使其浓度小于 ),需调节溶液pH范围为
),需调节溶液pH范围为___________ 。
(4) (结构为
(结构为 )在流程中的作用是
)在流程中的作用是___________ ,它与 溶液常温下混合一周,可以慢慢得到球形二氧化锰(
溶液常温下混合一周,可以慢慢得到球形二氧化锰( )。试写出该反应的离子方程式
)。试写出该反应的离子方程式___________ 。
(5)将 和
和 按4∶1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品
按4∶1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品 并生两种气体。则该反应的化学方程式为
并生两种气体。则该反应的化学方程式为___________ 。
(6)锰酸锂可充电电池的总反应为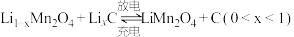
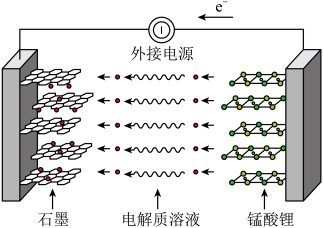
①充电时石墨电极是___________ (填“嵌锂”或“脱嵌”)过程。
②放电时,电池的正极反应式为___________ 。
 ,含少量
,含少量 、FeO、
、FeO、 、
、 等杂质)为原料制备锰酸锂的流程如图所示。
等杂质)为原料制备锰酸锂的流程如图所示。
(1)
 的最外层电子排布式为
的最外层电子排布式为(2)溶浸过程中为提高
 吸收率可采取的措施有
吸收率可采取的措施有a.粉碎矿石
b.不断搅拌,使
 和软锰矿浆充分接触
和软锰矿浆充分接触c.减小通入
 的流速
的流速d.升高温度
(3)已知:室温下,
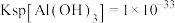 ,
,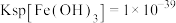 ,pH=7.1时
,pH=7.1时 开始沉淀。氧化除杂时(室温)除去
开始沉淀。氧化除杂时(室温)除去 溶液中的
溶液中的 、
、 (使其浓度小于
(使其浓度小于 ),需调节溶液pH范围为
),需调节溶液pH范围为(4)
 (结构为
(结构为 )在流程中的作用是
)在流程中的作用是 溶液常温下混合一周,可以慢慢得到球形二氧化锰(
溶液常温下混合一周,可以慢慢得到球形二氧化锰( )。试写出该反应的离子方程式
)。试写出该反应的离子方程式(5)将
 和
和 按4∶1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品
按4∶1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品 并生两种气体。则该反应的化学方程式为
并生两种气体。则该反应的化学方程式为(6)锰酸锂可充电电池的总反应为
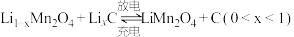

①充电时石墨电极是
②放电时,电池的正极反应式为
您最近半年使用:0次
【推荐1】连二亚硫酸钠(Na2S2O4)俗称保险粉,有极强的还原性。受热、遇水都会发生分解反应放出大量的热,甚至引起燃烧。不溶于乙醇,可溶于氢氧化钠水溶液并稳定存在。
(1)保险粉应如何保存?_______________________________________ 。
(2)锌粉法是制备Na2S2O4的一种常见方法,其原理如图所示:
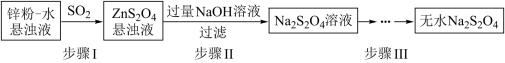
①步骤I中SO2表现了____________ (填“氧化性”、“还原性”或“酸性”);若用Na2SO3固体和某酸反应制备SO2气体,你认为下列最适宜选用的酸是____________
A.浓盐酸 B.质量分数为70%的H2SO4
C.稀硝酸 D.质量分数为10%的稀硫酸
②常温下,若ZnS2O4悬浊液中c(Zn2+)=0.1mol·L-1,则应加氢氧化钠溶液调至pH≥_________ ,才能使Zn(OH)2沉淀完全(已知离子浓度≤1.0×10-5mol·L-1,即沉淀完全;Ksp[Zn(OH)2]=1.0×10-17)
③步骤Ⅲ过程较为复杂,其中涉及过滤,洗涤,干燥等过程,请写出洗涤过程:_______________ .
(3)甲酸钠法是制备Na2S2O4的一种新方法,其原理为将甲酸钠(HCOONa)、碳酸钠溶于乙醇中,再通入足量的SO2气体,析出Na2S2O4固体。完成反应的化学方程式:_________________
____HCOONa+____SO2+___Na2CO3=____Na2S2O4↓+___H2O+______
(4)保险粉在空气中容易吸收氧气而发生氧化。其方程式为:
①2Na2S2O4+O2+H2O=4NaHSO3或 ②2Na2S2O4+O2+H2O=4NaHSO3+NaHSO4
请设计实验证明氧化时发生的是②的反应。____________________________ .
(1)保险粉应如何保存?
(2)锌粉法是制备Na2S2O4的一种常见方法,其原理如图所示:

①步骤I中SO2表现了
A.浓盐酸 B.质量分数为70%的H2SO4
C.稀硝酸 D.质量分数为10%的稀硫酸
②常温下,若ZnS2O4悬浊液中c(Zn2+)=0.1mol·L-1,则应加氢氧化钠溶液调至pH≥
③步骤Ⅲ过程较为复杂,其中涉及过滤,洗涤,干燥等过程,请写出洗涤过程:
(3)甲酸钠法是制备Na2S2O4的一种新方法,其原理为将甲酸钠(HCOONa)、碳酸钠溶于乙醇中,再通入足量的SO2气体,析出Na2S2O4固体。完成反应的化学方程式:
____HCOONa+____SO2+___Na2CO3=____Na2S2O4↓+___H2O+______
(4)保险粉在空气中容易吸收氧气而发生氧化。其方程式为:
①2Na2S2O4+O2+H2O=4NaHSO3或 ②2Na2S2O4+O2+H2O=4NaHSO3+NaHSO4
请设计实验证明氧化时发生的是②的反应。
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制得Cl2,进而制备少量KClO3和NaClO。
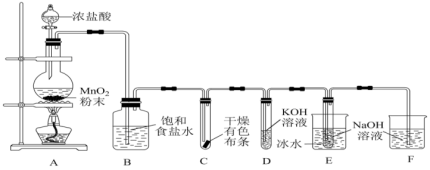
已知: Cl2与KOH溶液在70~80 ℃时反应生成KClO3,而在温度较低时会反应生成KClO。回答下列问题:
(1)装置A中盛放浓盐酸的仪器名称是___________ 。
(2)A中制备Cl2的化学方程式为___________ , 该反应中盐酸表现的性质有哪些:___________ 。
(3)B中饱和食盐水的作用是___________ 。C中的实验现象是 ___________ 。
(4)D需要进行加热,采用适宜的加热方式是___________ 。
(5)E中反应的离子方程式为___________ 。
(6)F的作用是___________ 。

已知: Cl2与KOH溶液在70~80 ℃时反应生成KClO3,而在温度较低时会反应生成KClO。回答下列问题:
(1)装置A中盛放浓盐酸的仪器名称是
(2)A中制备Cl2的化学方程式为
(3)B中饱和食盐水的作用是
(4)D需要进行加热,采用适宜的加热方式是
(5)E中反应的离子方程式为
(6)F的作用是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】2019年诺贝尔化学奖颁给了为锂电池发展作出突出贡献的三位科学家。某废旧锂电池正极主要由 、铝箔、炭黑等组成,
、铝箔、炭黑等组成, 、
、 、P具有极高的回收价值,具体流程如图1所示:
、P具有极高的回收价值,具体流程如图1所示:

(1)过程i生成 溶液的离子方程式是
溶液的离子方程式是___________ ,该反应的氧化剂为___________ 。
(2)过程ii中 /
/ 的作用是
的作用是___________ 。
(3)浸出液X的主要成分为 、
、 、
、 等。过程iii控制碳酸钠溶液浓度20%、温度85℃、反应时间3h条件下探究
等。过程iii控制碳酸钠溶液浓度20%、温度85℃、反应时间3h条件下探究 对磷酸铁沉淀的影响,如图所示。
对磷酸铁沉淀的影响,如图所示。

①综合考虑铁和磷沉淀率,最佳 为
为___________ 。
②结合平衡移动原理,解释过程iii中 增大,铁和磷沉淀率增大的原因
增大,铁和磷沉淀率增大的原因___________ 。
③当 后,随
后,随 增加,磷沉淀率出现了减小的趋势,解释其原因
增加,磷沉淀率出现了减小的趋势,解释其原因___________ 。
(4) 可以通过
可以通过 、
、 与
与 以物质的量之比为
以物质的量之比为 的关系发生共沉淀反应制取,共沉淀反应的化学方程式为
的关系发生共沉淀反应制取,共沉淀反应的化学方程式为___________ 。
 、铝箔、炭黑等组成,
、铝箔、炭黑等组成, 、
、 、P具有极高的回收价值,具体流程如图1所示:
、P具有极高的回收价值,具体流程如图1所示:
(1)过程i生成
 溶液的离子方程式是
溶液的离子方程式是(2)过程ii中
 /
/ 的作用是
的作用是(3)浸出液X的主要成分为
 、
、 、
、 等。过程iii控制碳酸钠溶液浓度20%、温度85℃、反应时间3h条件下探究
等。过程iii控制碳酸钠溶液浓度20%、温度85℃、反应时间3h条件下探究 对磷酸铁沉淀的影响,如图所示。
对磷酸铁沉淀的影响,如图所示。
①综合考虑铁和磷沉淀率,最佳
 为
为②结合平衡移动原理,解释过程iii中
 增大,铁和磷沉淀率增大的原因
增大,铁和磷沉淀率增大的原因③当
 后,随
后,随 增加,磷沉淀率出现了减小的趋势,解释其原因
增加,磷沉淀率出现了减小的趋势,解释其原因(4)
 可以通过
可以通过 、
、 与
与 以物质的量之比为
以物质的量之比为 的关系发生共沉淀反应制取,共沉淀反应的化学方程式为
的关系发生共沉淀反应制取,共沉淀反应的化学方程式为
您最近半年使用:0次



