 是一种常见的氧化剂,工业上利用软锰矿
是一种常见的氧化剂,工业上利用软锰矿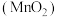 制备高锰酸钾的流程如下,在实验室中模拟该流程制备
制备高锰酸钾的流程如下,在实验室中模拟该流程制备 ,并对产物纯度进行测定。
,并对产物纯度进行测定。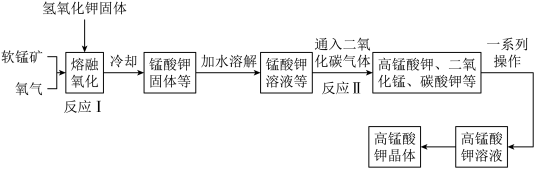
回答下列问题:
(1)反应Ⅰ需要的温度约为400℃,应选择的加热仪器为
A酒精灯 B.电磁炉 C.电吹风
(2)加水溶解步骤必须要用到的玻璃仪器有_______。
| A.烧杯 | B.玻璃棒 | C.量筒 | D.酒精灯 |
 、
、 溶液中的
溶液中的 ,应进行操作
,应进行操作(4)由
 溶液获的
溶液获的 晶体的一系列操作为:蒸发浓缩至饱和、
晶体的一系列操作为:蒸发浓缩至饱和、(5)研究表明,反应Ⅰ分两步进行:
第一步反应生成
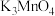 ,反应方程式为
,反应方程式为第二步反应方程式为
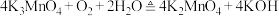
(6)写出反应Ⅱ的离子方程式
(7)所得产品中只含有杂质
 ,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
更新时间:2022-10-23 09:31:00
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】食品添加剂的常见类别有:着色剂、增味剂、膨松剂、凝固剂、防腐剂、营养强化剂等。
(1)碘酸钾为___________ (填食品添加剂的类别)。
(2)从海带中提取碘的主要实验过程如下图所示:

①干海带的“灼烧”需在___________ (填仪器名称)中进行。
②操作1为___________ (填操作名称)。
③在“氧化”步骤中,最符合绿色化学思想的氧化剂是下列物质中的___________ (填选项字母),酸性条件下该反应的离子方程式为___________ 。
A. 溶液 B.浓硝酸 C.
溶液 B.浓硝酸 C.
④检验操作2后水层中是否含有碘单质的方法为___________ 。
(3)在加热条件下,将 通入到
通入到 和
和 的混合溶液中制备
的混合溶液中制备 ,该反应的化学方程式为
,该反应的化学方程式为___________ ;若要制备500g的加碘食盐(碘含量为2.54%),至少需要
___________ g。
(1)碘酸钾为
(2)从海带中提取碘的主要实验过程如下图所示:

①干海带的“灼烧”需在
②操作1为
③在“氧化”步骤中,最符合绿色化学思想的氧化剂是下列物质中的
A.
 溶液 B.浓硝酸 C.
溶液 B.浓硝酸 C.
④检验操作2后水层中是否含有碘单质的方法为
(3)在加热条件下,将
 通入到
通入到 和
和 的混合溶液中制备
的混合溶液中制备 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氨氮废水中的氮多以 和NH3∙H2O形式存在。某工厂处理氨氮废水流程如下:
和NH3∙H2O形式存在。某工厂处理氨氮废水流程如下:
(1)过程I的目的是将 转化为NH3,其离子方程式为
转化为NH3,其离子方程式为___________ ,鼓入热空气能将氨吹出的原因是___________ 。
(2)过程II加入NaClO溶液可将废水中残留的NH3∙H2O转化为无污染气体,该反应的化学方程式为___________ 。
(3)含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到将余氯转化为无毒物质的目的___________ (填字母)。
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
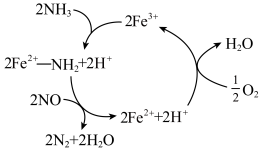
(4)有氧条件下,NH3催化还原NO是主要的烟气脱硝技术。在以Fe2O3为主的催化剂上可能发生的反应过程如图。写出总反应的化学方程式:___________ 。
 和NH3∙H2O形式存在。某工厂处理氨氮废水流程如下:
和NH3∙H2O形式存在。某工厂处理氨氮废水流程如下:
(1)过程I的目的是将
 转化为NH3,其离子方程式为
转化为NH3,其离子方程式为(2)过程II加入NaClO溶液可将废水中残留的NH3∙H2O转化为无污染气体,该反应的化学方程式为
(3)含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到将余氯转化为无毒物质的目的
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
(4)有氧条件下,NH3催化还原NO是主要的烟气脱硝技术。在以Fe2O3为主的催化剂上可能发生的反应过程如图。写出总反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】I.某探究小组在实验室中用铝土矿(主要成分为Al2O3,还含有Fe2O3、SiO2)提取氧化铝。回答下列问题:
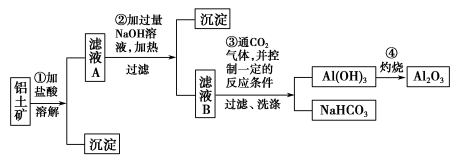
(1)在实验中需用1 mol·L-1的NaOH溶液480 mL,配制该溶液已有下列仪器:烧杯、托盘天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器是______________ 。
(2)写出步骤①中发生反应的离子方程式___________
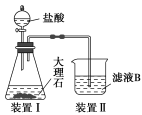
(3)甲同学在实验室中用如图装置制备CO2气体,并通入滤液B中制备Al(OH)3时,结果没有产生预期现象。
乙同学分析认为:甲同学通入CO2的量不足是导致实验失败的原因之一,你认为乙的分析是否合理?________ 。若合理,请用离子方程式解释其原因_________________________________ (若你认为不合理,该空不作答)。
II.某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:_____________________________
(2)实验②的化学反应中转移电子的物质的量是_______________________ 。
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是__________________________________________________________ 。

(1)在实验中需用1 mol·L-1的NaOH溶液480 mL,配制该溶液已有下列仪器:烧杯、托盘天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器是
(2)写出步骤①中发生反应的离子方程式
(3)甲同学在实验室中用如图装置制备CO2气体,并通入滤液B中制备Al(OH)3时,结果没有产生预期现象。
乙同学分析认为:甲同学通入CO2的量不足是导致实验失败的原因之一,你认为乙的分析是否合理?

II.某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:
(2)实验②的化学反应中转移电子的物质的量是
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】观察下列实验装置图,试回答下列问题:
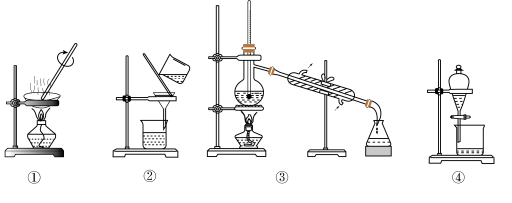
(1)图中③实验操作的名称是__________________ ;
(2)写出装置④中所用玻璃仪器的名称____________________ ;
(3)下列实验需要在哪套装置中进行(填序号):
a.从海水中提取蒸馏水:____________ 。
b.分离氯化钠和水:________________ 。
c.分离碳酸钙和水:________________ 。
d.分离植物油和水:________________ 。

(1)图中③实验操作的名称是
(2)写出装置④中所用玻璃仪器的名称
(3)下列实验需要在哪套装置中进行(填序号):
a.从海水中提取蒸馏水:
b.分离氯化钠和水:
c.分离碳酸钙和水:
d.分离植物油和水:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】含氯消毒剂可有效灭活新冠病毒,为新冠疫情防控做出了巨大贡献。二氧化氯(ClO2)就是其中一种高效消毒灭菌剂。二氧化氯(ClO2)是黄绿色易溶于水的气体,熔点-59°C,沸点11°C,但其浓度过高时易分解爆炸,故常采用H2O2和NaOH混合溶液将其吸收转化为NaClO2固体便于运输和贮存。现利用如下装置及试剂制备。
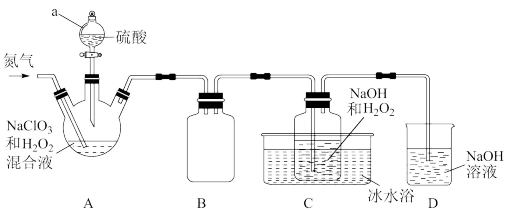
请回答下列问题:
(1)仪器a的名称为___________ ,装置A中反应的化学方程式为___________ 。
(2)通入氮气的主要作用___________ 、___________ 。
(3)装置B的作用是___________ 。装置D的作用是___________ 。
(4)一段时间后,C装置中有NaClO2晶体析出,则C装置中发生的离子反应方程式为___________ ,冰水浴冷却的目的是___________ 。
(5)测定NaClO2样品的纯度:取C中NaClO2晶体5.0g溶于水配成500mL溶液,取出10mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应(NaClO2被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.20mol·L-1Na2S2O3标准液滴定,达到滴定达终点时用去标准液20.00mL。(已知:I2+2 =
= +2I-)
+2I-)
①滴定终点的现象:___________ 。
②试计算NaClO2样品的纯度___________ 。

请回答下列问题:
(1)仪器a的名称为
(2)通入氮气的主要作用
(3)装置B的作用是
(4)一段时间后,C装置中有NaClO2晶体析出,则C装置中发生的离子反应方程式为
(5)测定NaClO2样品的纯度:取C中NaClO2晶体5.0g溶于水配成500mL溶液,取出10mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应(NaClO2被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.20mol·L-1Na2S2O3标准液滴定,达到滴定达终点时用去标准液20.00mL。(已知:I2+2
 =
= +2I-)
+2I-)①滴定终点的现象:
②试计算NaClO2样品的纯度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】传统的定量化学实验受到计量手段的制约而研究范围狭窄、精确度不高,DIS数字化信息系统(由传感器、数据采集器和计算机组成)因为可以准确测量溶液的pH等而在中和滴定的研究中应用越来越广泛深入。
(1)某学习小组利用 DIS 系统探究强碱和不同酸的中和反应,实验过程如下:
①分别配制0.1000 mol/L的NaOH、HCl、CH3COOH溶液备用。
②用0.1000 mol/L的NaOH溶液分别滴定10.00 mL 0.1000 mol/L的HCl和CH3COOH溶液,连接数据采集器和pH传感器。
③由计算机绘制的滴定曲线如图:
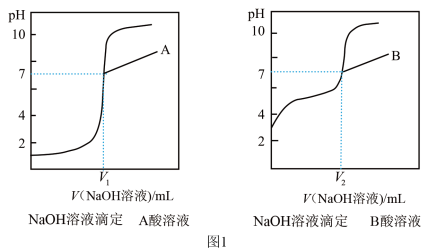
(2)①A是_____ 酸(填“醋酸”或“盐酸”)
②两曲线图中 V1________ V2(填“>”“=”或“<”),A点和B点,水的电离程度_____ (填“A 点大”、“B 点大”、“A 和 B 点相同”或“无法判断”)
(3)另一个学习小组利用DIS系统测定某醋酸溶液的物质的量浓度,以测量溶液导电能力来判断滴定终点,实验步骤如下:
①用________ (填仪器名称)量取 20.00 mL 醋酸溶液样品,倒入洁净干燥锥形瓶中,连接好 DIS系统,如果锥形瓶中含有少量蒸馏水,是否会影响测量结果?______ (填“是”“否”或“不能确定”)。向锥形瓶中滴加 0.1000 mol/L的NaOH溶液,计算机屏幕上显示溶液导电能力与加入NaOH溶液体积关系的曲线图(见如图)。
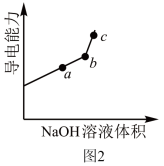
②醋酸与NaOH溶液反应的离子方程式为______ 。
③图中b点时,溶液中各离子浓度大小的关系是_________ ,c(CH3COOH)+c(CH3COO-)=_________ mol/L。
④若图中某一点 pH 等于8,则 c(Na+)-c(CH3COO-)的精确值为________ mol/L。
(1)某学习小组利用 DIS 系统探究强碱和不同酸的中和反应,实验过程如下:
①分别配制0.1000 mol/L的NaOH、HCl、CH3COOH溶液备用。
②用0.1000 mol/L的NaOH溶液分别滴定10.00 mL 0.1000 mol/L的HCl和CH3COOH溶液,连接数据采集器和pH传感器。
③由计算机绘制的滴定曲线如图:

(2)①A是
②两曲线图中 V1
(3)另一个学习小组利用DIS系统测定某醋酸溶液的物质的量浓度,以测量溶液导电能力来判断滴定终点,实验步骤如下:
①用

②醋酸与NaOH溶液反应的离子方程式为
③图中b点时,溶液中各离子浓度大小的关系是
④若图中某一点 pH 等于8,则 c(Na+)-c(CH3COO-)的精确值为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】盐湖卤水(主要含Na+、Mg2+、Li+、Cl-、 和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备
和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备 的工艺流程如图:
的工艺流程如图:
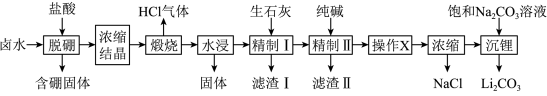
已知:常温下, 。相关化合物的溶解度与温度的关系如图所示。
。相关化合物的溶解度与温度的关系如图所示。

回答下列问题:
(1)含硼固体中的B(OH)3在水中存在平衡: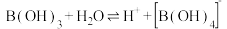 (常温下,
(常温下, );B(OH)3与
);B(OH)3与 溶液反应可制备硼砂
溶液反应可制备硼砂 。常温下,在
。常温下,在 硼砂溶液中,
硼砂溶液中,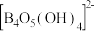 水解生成等物质的量浓度的B(OH)3和
水解生成等物质的量浓度的B(OH)3和 ,该水解反应的离子方程式为
,该水解反应的离子方程式为___________ ,该溶液pH=___________ 。
(2)滤渣Ⅰ的主要成分是___________ (填化学式);精制Ⅰ后溶液中Li+浓度为 ,则常温下精制Ⅱ过程中
,则常温下精制Ⅱ过程中 浓度应控制在
浓度应控制在___________  以下。若脱硼后直接进行精制Ⅰ,除无法回收HCl外,还将增加
以下。若脱硼后直接进行精制Ⅰ,除无法回收HCl外,还将增加___________ 的用量(填化学式)。
(3)精制Ⅱ的目的是___________ ;进行操作X时应选择的试剂是___________ 。
 和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备
和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备 的工艺流程如图:
的工艺流程如图:
已知:常温下,
 。相关化合物的溶解度与温度的关系如图所示。
。相关化合物的溶解度与温度的关系如图所示。 
回答下列问题:
(1)含硼固体中的B(OH)3在水中存在平衡:
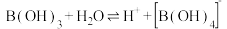 (常温下,
(常温下, );B(OH)3与
);B(OH)3与 溶液反应可制备硼砂
溶液反应可制备硼砂 。常温下,在
。常温下,在 硼砂溶液中,
硼砂溶液中,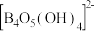 水解生成等物质的量浓度的B(OH)3和
水解生成等物质的量浓度的B(OH)3和 ,该水解反应的离子方程式为
,该水解反应的离子方程式为(2)滤渣Ⅰ的主要成分是
 ,则常温下精制Ⅱ过程中
,则常温下精制Ⅱ过程中 浓度应控制在
浓度应控制在 以下。若脱硼后直接进行精制Ⅰ,除无法回收HCl外,还将增加
以下。若脱硼后直接进行精制Ⅰ,除无法回收HCl外,还将增加(3)精制Ⅱ的目的是
您最近一年使用:0次
【推荐2】实验室以K2MnO4为原料,用两种方法制备高锰酸钾。已知:K2MnO4在浓强碱溶液中可稳定存在,溶液呈墨绿色,当溶液碱性减弱时易发生反应 。
。
(1) CO2法:实验装置如图。

①反应一段时间后,用玻璃棒蘸取溶液点在滤纸上,仅有紫红色而没有绿色痕迹,由此可知___________ 。
②停止通入CO2,过滤除去___________ (填化学式,下同),将滤液蒸发浓缩、冷却结晶,抽滤得到KMnO4粗品。若通入过多CO2,产品中可能混有的杂质是___________ 。
(2)电解法:实验装置如图。
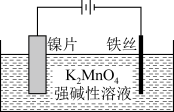
阳极的电极反应式为___________ ,阴极产生的气体为___________ (填化学式)。
(3)如用氨燃料电池电解溶液,已知氨燃料电池使用的电解质溶液是KOH溶液,电池总反应为 。则其负极反应式为
。则其负极反应式为___________ 。
(4)若用钢铁(含Fe、C)制品盛装NaClO溶液会发生电化学腐蚀,钢铁制品表面生成红褐色沉淀,溶液会失去漂白、杀菌消毒功效。该电化学腐蚀过程中的正极反应式为___________ 。
 。
。(1) CO2法:实验装置如图。

①反应一段时间后,用玻璃棒蘸取溶液点在滤纸上,仅有紫红色而没有绿色痕迹,由此可知
②停止通入CO2,过滤除去
(2)电解法:实验装置如图。

阳极的电极反应式为
(3)如用氨燃料电池电解溶液,已知氨燃料电池使用的电解质溶液是KOH溶液,电池总反应为
 。则其负极反应式为
。则其负极反应式为(4)若用钢铁(含Fe、C)制品盛装NaClO溶液会发生电化学腐蚀,钢铁制品表面生成红褐色沉淀,溶液会失去漂白、杀菌消毒功效。该电化学腐蚀过程中的正极反应式为
您最近一年使用:0次
【推荐3】回答下列问题:
(1)节能减排是当今社会的热门话题,研发混合动力汽车对于中国汽车业的未来具有重要的战略意义,镍氢电池的使用可以减少对环境的污染,它采用储氢金属为负极,碱液NaOH为电解液,镍氢电池充放电时发生反应NiO(OH)+ H2
H2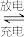 Ni(OH)2。其放电时的正极的电极反应方程式为
Ni(OH)2。其放电时的正极的电极反应方程式为_______ 。
(2)二氧化锰、锌是制备干电池的重要原料,工业上用软锰矿(含MnO2)和闪锌矿(含ZnS)联合生产二氧化锰、锌的工艺如下:
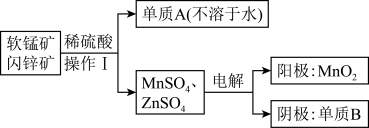
①操作I需要的玻璃仪器是_______ 。
②软锰矿(含MnO2)和闪锌矿与稀硫酸恰好完全反应,化学方程式为_______ ,上述电解过程中,当阴极生成6.5gB时,阳极生成的MnO2的质量为_______ ,此阳极的电极反应是_______ ,阴极的电极反应_______ 。
(1)节能减排是当今社会的热门话题,研发混合动力汽车对于中国汽车业的未来具有重要的战略意义,镍氢电池的使用可以减少对环境的污染,它采用储氢金属为负极,碱液NaOH为电解液,镍氢电池充放电时发生反应NiO(OH)+
 H2
H2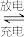 Ni(OH)2。其放电时的正极的电极反应方程式为
Ni(OH)2。其放电时的正极的电极反应方程式为(2)二氧化锰、锌是制备干电池的重要原料,工业上用软锰矿(含MnO2)和闪锌矿(含ZnS)联合生产二氧化锰、锌的工艺如下:

①操作I需要的玻璃仪器是
②软锰矿(含MnO2)和闪锌矿与稀硫酸恰好完全反应,化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】直接氧化法制备混凝剂聚合硫酸铁[Fe2(OH)n(SO4)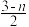 ]m(n>2,m≤10)的实验流程如下:
]m(n>2,m≤10)的实验流程如下:

已知:盐基度= ×100%.式中n(OH-)、n(Fe)分别表示PFS中OH-和Fe3+的物质的量.所得产品若要用于饮用水处理,需达到盐基度指标为 8.0%~16.0%.
×100%.式中n(OH-)、n(Fe)分别表示PFS中OH-和Fe3+的物质的量.所得产品若要用于饮用水处理,需达到盐基度指标为 8.0%~16.0%.
(1)实验加入硫酸的作用是____________,取样分析Fe2+浓度,其目的是____________。
(2)用pH试纸测定溶液pH的操作方法为____________,若溶液的pH偏小,将导致聚合硫酸铁中铁的质量分数____________(填“偏高”、“偏低”、“无影响”)
(3)聚合反应的原理为m[Fe2(OH)n(SO4) 3-n/2]⇌[Fe2(OH)n(SO4)3-n/2]m,则水解反应的化学方程式为____________.
(4)产品盐基度的测定方法:
Ⅰ称取m g固体试样,置于400mL聚乙烯烧杯中,加入25mL盐酸标准溶液,再加20mL煮沸后冷却的蒸馏水,摇匀,盖上表面皿.
Ⅱ室温下放置10min,再加入10mL氟化钾溶液,摇匀,掩蔽Fe3+,形成白色沉淀.
Ⅲ加入5滴酚酞指示剂,立即用物质的量浓度为c mol•L-1的氢氧化钠标准液滴定至终点,消耗体积为VmL.
Ⅳ向聚乙烯烧杯中,加入25mL盐酸标准溶液,再加20mL煮沸后冷却的蒸馏水,摇匀,盖上表面皿.然后重复Ⅱ、Ⅲ做空白试验,消耗氢氧化钠标准液的体积为V0mL.
①达到滴定终点的现象为____________。
②已知试样中Fe3+的质量分数为w1,则该试样的盐基度(w)的计算表达式为____________。
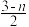 ]m(n>2,m≤10)的实验流程如下:
]m(n>2,m≤10)的实验流程如下:
已知:盐基度=
 ×100%.式中n(OH-)、n(Fe)分别表示PFS中OH-和Fe3+的物质的量.所得产品若要用于饮用水处理,需达到盐基度指标为 8.0%~16.0%.
×100%.式中n(OH-)、n(Fe)分别表示PFS中OH-和Fe3+的物质的量.所得产品若要用于饮用水处理,需达到盐基度指标为 8.0%~16.0%.(1)实验加入硫酸的作用是____________,取样分析Fe2+浓度,其目的是____________。
(2)用pH试纸测定溶液pH的操作方法为____________,若溶液的pH偏小,将导致聚合硫酸铁中铁的质量分数____________(填“偏高”、“偏低”、“无影响”)
(3)聚合反应的原理为m[Fe2(OH)n(SO4) 3-n/2]⇌[Fe2(OH)n(SO4)3-n/2]m,则水解反应的化学方程式为____________.
(4)产品盐基度的测定方法:
Ⅰ称取m g固体试样,置于400mL聚乙烯烧杯中,加入25mL盐酸标准溶液,再加20mL煮沸后冷却的蒸馏水,摇匀,盖上表面皿.
Ⅱ室温下放置10min,再加入10mL氟化钾溶液,摇匀,掩蔽Fe3+,形成白色沉淀.
Ⅲ加入5滴酚酞指示剂,立即用物质的量浓度为c mol•L-1的氢氧化钠标准液滴定至终点,消耗体积为VmL.
Ⅳ向聚乙烯烧杯中,加入25mL盐酸标准溶液,再加20mL煮沸后冷却的蒸馏水,摇匀,盖上表面皿.然后重复Ⅱ、Ⅲ做空白试验,消耗氢氧化钠标准液的体积为V0mL.
①达到滴定终点的现象为____________。
②已知试样中Fe3+的质量分数为w1,则该试样的盐基度(w)的计算表达式为____________。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
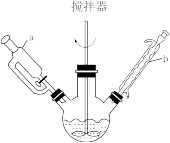
【推荐2】山梨酸乙酯对细菌、霉菌等有很好的灭活作用,广泛地用作各类食品的保鲜剂以及家畜、家禽的消毒剂。直接酯化法合成山梨酸乙酯的装置(夹持装置省略)如图所示,该方法简单,原料易得,产物纯度高,反应方程式如下:

可能用到的有关数据如下表:
实验步骤:
在三口烧瓶中加入5. 6 g山梨酸、足量乙醇、环己烷、少量催化剂和几粒沸石,油浴加热三口烧瓶,反应温度为110°C,回流4小时后停止加热和搅拌反应液冷却至室温,滤去催化剂和沸石,将滤液倒入分液漏斗中,先用5% NaHCO3溶液洗涤至中性,再用水洗涤,分液,在有机层中加入少量无水MgSO4,静置片刻,过滤,将滤液进行蒸馏,收集195 °C的馏分得到纯净的山梨酸乙酯5.0g。
回答下列问题:
(1)仪器a的名称是___________ ,仪器b的作用是___________ 。
(2)洗涤、分液过程中,加入5% NaHCO3溶液的目的是___________ 。有机层从分液漏斗的___________ (填“ 上口倒出”或“下口放出”)。
(3)在有机层中加入少量无水MgSO4的目的是___________ 。
(4)在本实验中,山梨酸乙酯的产率是___________ (精确至0. 1%)。
(5)为提高反应正向进行的程度,可以将反应中生成的水及时移出反应体系,常加入带水剂。可作带水剂的物质必须满足以下条件:
①能够与水形成共沸物(沸点相差30 ° C以上的两个组分难以形成共沸物);
②在水中的溶解度很小。
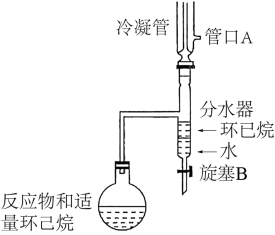
本实验室常使用如图所示装置(夹持、加热装置已略去)提高产物的产率。下列说法正确的是___________(填标号)。


可能用到的有关数据如下表:
| 物质 | 相对分子质量 | 密度/(g·cm-3) | 沸点/°C | 水溶性 |
| 山梨酸 | 112 | 1.204 | 228 | 易溶 |
| 乙醇 | 46 | 0.789 | 78 | 易溶 |
| 山梨酸乙酯 | 140 | 0. 926 | 195 | 难溶 |
| 环己烷 | 84 | 0.780 | 80.7 | 难溶 |
在三口烧瓶中加入5. 6 g山梨酸、足量乙醇、环己烷、少量催化剂和几粒沸石,油浴加热三口烧瓶,反应温度为110°C,回流4小时后停止加热和搅拌反应液冷却至室温,滤去催化剂和沸石,将滤液倒入分液漏斗中,先用5% NaHCO3溶液洗涤至中性,再用水洗涤,分液,在有机层中加入少量无水MgSO4,静置片刻,过滤,将滤液进行蒸馏,收集195 °C的馏分得到纯净的山梨酸乙酯5.0g。
回答下列问题:
(1)仪器a的名称是
(2)洗涤、分液过程中,加入5% NaHCO3溶液的目的是
(3)在有机层中加入少量无水MgSO4的目的是
(4)在本实验中,山梨酸乙酯的产率是
(5)为提高反应正向进行的程度,可以将反应中生成的水及时移出反应体系,常加入带水剂。可作带水剂的物质必须满足以下条件:
①能够与水形成共沸物(沸点相差30 ° C以上的两个组分难以形成共沸物);
②在水中的溶解度很小。
本实验室常使用如图所示装置(夹持、加热装置已略去)提高产物的产率。下列说法正确的是___________(填标号)。

| A.管口A是冷凝水的出水口 |
| B.环己烷可将反应产生的水及时带出 |
| C.工作一段时间后,当环己烷即将流回烧瓶中时,必须将分水器中的水和环己烷放出 |
| D.工作段时间后,环己烷可在烧瓶与分水器中循环流动 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硫代硫酸钠(Na2S2O3)俗称保险粉,可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等。实验室可通过Na2S、Na2CO3和SO2共同反应来制取Na2S2O3。
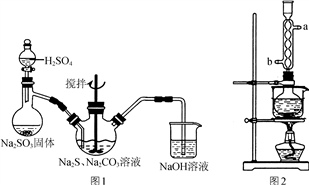
(1)写出图1所示装置中三颈瓶中由反应制取Na2S2O3的化学方程式:_______________ 。
(2)为测定所得保险粉样品中Na2S2O3·5H2O的质量分数,可用标准碘溶液进行滴定,反应方程式为2Na2S2O3+I2===2NaI+Na2S4O6。
① 利用KIO3、KI和HCl可配制标准碘溶液。写出配制时所发生反应的离子方程式:__________________________________ 。
② 准确称取一定质量的Na2S2O3·5H2O样品于锥形瓶中,加水溶解,并滴加________ 作指示剂,用所配制的标准碘溶液滴定。滴定时所用的玻璃仪器除锥形瓶外,还有________ 。
③ 若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3·5H2O的质量分数的测量结果________ (填“偏高”“偏低”或“不变”)。
(3)本实验对Na2S的纯度要求较高,利用图2所示的装置可将工业级的Na2S提纯。已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯步骤依次为:
① 将已称量好的工业Na2S放入圆底烧瓶中,并加入一定质量的酒精和少量水;
② 按图2所示装配所需仪器,向冷凝管中通入冷却水,水浴加热;
③ 待________ 时,停止加热,将烧瓶取下;
④______________________________ ;
⑤______________________________ ;
⑥ 将所得固体洗涤、干燥,得到Na2S·9H2O晶体。

(1)写出图1所示装置中三颈瓶中由反应制取Na2S2O3的化学方程式:
(2)为测定所得保险粉样品中Na2S2O3·5H2O的质量分数,可用标准碘溶液进行滴定,反应方程式为2Na2S2O3+I2===2NaI+Na2S4O6。
① 利用KIO3、KI和HCl可配制标准碘溶液。写出配制时所发生反应的离子方程式:
② 准确称取一定质量的Na2S2O3·5H2O样品于锥形瓶中,加水溶解,并滴加
③ 若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3·5H2O的质量分数的测量结果
(3)本实验对Na2S的纯度要求较高,利用图2所示的装置可将工业级的Na2S提纯。已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯步骤依次为:
① 将已称量好的工业Na2S放入圆底烧瓶中,并加入一定质量的酒精和少量水;
② 按图2所示装配所需仪器,向冷凝管中通入冷却水,水浴加热;
③ 待
④
⑤
⑥ 将所得固体洗涤、干燥,得到Na2S·9H2O晶体。
您最近一年使用:0次



