食品添加剂的常见类别有:着色剂、增味剂、膨松剂、凝固剂、防腐剂、营养强化剂等。
(1)碘酸钾为___________ (填食品添加剂的类别)。
(2)从海带中提取碘的主要实验过程如下图所示:

①干海带的“灼烧”需在___________ (填仪器名称)中进行。
②操作1为___________ (填操作名称)。
③在“氧化”步骤中,最符合绿色化学思想的氧化剂是下列物质中的___________ (填选项字母),酸性条件下该反应的离子方程式为___________ 。
A. 溶液 B.浓硝酸 C.
溶液 B.浓硝酸 C.
④检验操作2后水层中是否含有碘单质的方法为___________ 。
(3)在加热条件下,将 通入到
通入到 和
和 的混合溶液中制备
的混合溶液中制备 ,该反应的化学方程式为
,该反应的化学方程式为___________ ;若要制备500g的加碘食盐(碘含量为2.54%),至少需要
___________ g。
(1)碘酸钾为
(2)从海带中提取碘的主要实验过程如下图所示:

①干海带的“灼烧”需在
②操作1为
③在“氧化”步骤中,最符合绿色化学思想的氧化剂是下列物质中的
A.
 溶液 B.浓硝酸 C.
溶液 B.浓硝酸 C.
④检验操作2后水层中是否含有碘单质的方法为
(3)在加热条件下,将
 通入到
通入到 和
和 的混合溶液中制备
的混合溶液中制备 ,该反应的化学方程式为
,该反应的化学方程式为
更新时间:2023-06-30 18:19:42
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】在生活中亚硝酸钠 应用十分广泛,它是一种白色固体,外观与
应用十分广泛,它是一种白色固体,外观与 极其相似;少量可做食品的防腐剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知
极其相似;少量可做食品的防腐剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。 能被高锰酸钾氧化,但不能被浓硫酸氧化。
能被高锰酸钾氧化,但不能被浓硫酸氧化。
②酸性高锰酸钾溶液可将 氧化成
氧化成 。
。
回答下列问题:
(1)装置 中的装浓硝酸的仪器名称是
中的装浓硝酸的仪器名称是_____________________ ,仪器按气流方向连接顺序为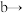
_____________________ 。
(2)①反应开始前打开止水夹 ,通入过量氮气的目的是
,通入过量氮气的目的是_________________________ 。
②反应结束后打开止水夹 ,再通入过量氮气的目的是
,再通入过量氮气的目的是_____________________ 。
(3)写出装置 中发生反应的离子方程式
中发生反应的离子方程式_________________________________________________________________ 。
(4)装置 能除去挥发的
能除去挥发的 蒸汽,另一作用是
蒸汽,另一作用是_________________________________________________ 。
(5)写出装置 中发生反应的离子方程式
中发生反应的离子方程式_________________________________________________________________ 。
 应用十分广泛,它是一种白色固体,外观与
应用十分广泛,它是一种白色固体,外观与 极其相似;少量可做食品的防腐剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知
极其相似;少量可做食品的防腐剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。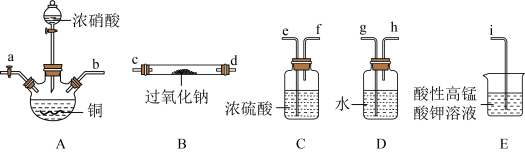
 能被高锰酸钾氧化,但不能被浓硫酸氧化。
能被高锰酸钾氧化,但不能被浓硫酸氧化。②酸性高锰酸钾溶液可将
 氧化成
氧化成 。
。回答下列问题:
(1)装置
 中的装浓硝酸的仪器名称是
中的装浓硝酸的仪器名称是
(2)①反应开始前打开止水夹
 ,通入过量氮气的目的是
,通入过量氮气的目的是②反应结束后打开止水夹
 ,再通入过量氮气的目的是
,再通入过量氮气的目的是(3)写出装置
 中发生反应的离子方程式
中发生反应的离子方程式(4)装置
 能除去挥发的
能除去挥发的 蒸汽,另一作用是
蒸汽,另一作用是(5)写出装置
 中发生反应的离子方程式
中发生反应的离子方程式
您最近一年使用:0次
【推荐2】亚氯酸钠( )是一种杀菌漂白剂,可用于棉纺漂白,食品消毒,水处理等,消毒时本身被还原成
)是一种杀菌漂白剂,可用于棉纺漂白,食品消毒,水处理等,消毒时本身被还原成 。亚氯酸钠晶体的一种生产工艺如下:
。亚氯酸钠晶体的一种生产工艺如下:
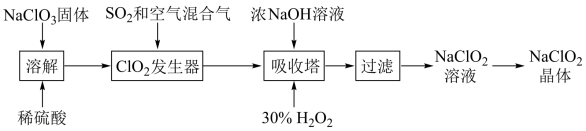
已知:① 浓度过高时易发生分解爆炸,一般用稀有气体或空气稀释至含量10%以下。
浓度过高时易发生分解爆炸,一般用稀有气体或空气稀释至含量10%以下。
② 在温度高于60℃时易分解生成
在温度高于60℃时易分解生成 和NaCl。
和NaCl。
(1)在“ 发生器”中,
发生器”中, 与
与 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为______ 。
(2)向“ 发生器”中鼓入空气的作用是
发生器”中鼓入空气的作用是______ (填字母)。
a.将 氧化成
氧化成 ,增强酸性
,增强酸性
b.将 氧化成
氧化成
c.稀释 ,以防分解爆炸
,以防分解爆炸
(3)“吸收塔”的作用是将产生的 反应转化为
反应转化为 ,在此过程中加入的
,在此过程中加入的 是作
是作______ (填“氧化剂”或“还原剂”)。“吸收塔”中需要控制温度不超过20℃,其原因是______ 。
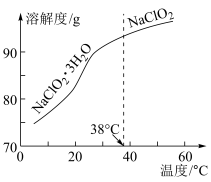
(4) 的溶解度曲线如下图所示。从
的溶解度曲线如下图所示。从 溶液中获得
溶液中获得 晶体的操作是:将
晶体的操作是:将 溶液
溶液______ 、______ ,过滤,洗涤,干燥。
(5)为测定所得 产品的纯度,进行如下实验:
产品的纯度,进行如下实验:
步骤①:取1.000 g样品于烧杯中,用适量蒸馏水溶解后,加入略过量的KI晶体,再滴加适量的稀硫酸,充分反应;(反应方程式为: )
)
步骤②:将所得溶液转移至250 mL容量瓶中,稀释定容得溶液A;
步骤③:准确移取25.00 mL溶液A于锥形瓶中,向锥形瓶中滴加两滴淀粉溶液作指示剂,用0.2000 的
的 标准溶液与之反应,至恰好完全反应时消耗
标准溶液与之反应,至恰好完全反应时消耗 溶液22.00 mL。(反应方程式为:
溶液22.00 mL。(反应方程式为: ),计算该
),计算该 产品的纯度(写出计算过程)。
产品的纯度(写出计算过程)。____________________
 )是一种杀菌漂白剂,可用于棉纺漂白,食品消毒,水处理等,消毒时本身被还原成
)是一种杀菌漂白剂,可用于棉纺漂白,食品消毒,水处理等,消毒时本身被还原成 。亚氯酸钠晶体的一种生产工艺如下:
。亚氯酸钠晶体的一种生产工艺如下:
已知:①
 浓度过高时易发生分解爆炸,一般用稀有气体或空气稀释至含量10%以下。
浓度过高时易发生分解爆炸,一般用稀有气体或空气稀释至含量10%以下。②
 在温度高于60℃时易分解生成
在温度高于60℃时易分解生成 和NaCl。
和NaCl。(1)在“
 发生器”中,
发生器”中, 与
与 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(2)向“
 发生器”中鼓入空气的作用是
发生器”中鼓入空气的作用是a.将
 氧化成
氧化成 ,增强酸性
,增强酸性b.将
 氧化成
氧化成
c.稀释
 ,以防分解爆炸
,以防分解爆炸(3)“吸收塔”的作用是将产生的
 反应转化为
反应转化为 ,在此过程中加入的
,在此过程中加入的 是作
是作(4)
 的溶解度曲线如下图所示。从
的溶解度曲线如下图所示。从 溶液中获得
溶液中获得 晶体的操作是:将
晶体的操作是:将 溶液
溶液
(5)为测定所得
 产品的纯度,进行如下实验:
产品的纯度,进行如下实验:步骤①:取1.000 g样品于烧杯中,用适量蒸馏水溶解后,加入略过量的KI晶体,再滴加适量的稀硫酸,充分反应;(反应方程式为:
 )
)步骤②:将所得溶液转移至250 mL容量瓶中,稀释定容得溶液A;
步骤③:准确移取25.00 mL溶液A于锥形瓶中,向锥形瓶中滴加两滴淀粉溶液作指示剂,用0.2000
 的
的 标准溶液与之反应,至恰好完全反应时消耗
标准溶液与之反应,至恰好完全反应时消耗 溶液22.00 mL。(反应方程式为:
溶液22.00 mL。(反应方程式为: ),计算该
),计算该 产品的纯度(写出计算过程)。
产品的纯度(写出计算过程)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】海洋资源的综合利用是21世纪海祥开发利用的重点发展领域之一、从海水中可以制取氯、溴、镁等多种化工产品。在元素周期表中,溴(Br)位于第四周期,与Cl同主族。氯气可用于海水提溴,其工艺流程如下:
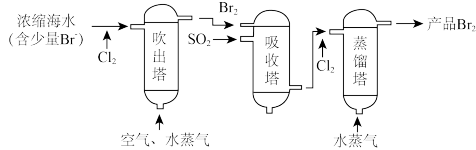
(1)进入吹出塔前海水中的 与
与 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(2)已知: 具有较强的氧化性,可氧化
具有较强的氧化性,可氧化 ,从吸收塔流出的溶液主要含
,从吸收塔流出的溶液主要含____ (写离子符号)。
(3)两次通入 的目的是富集浓缩溴,最终每获得
的目的是富集浓缩溴,最终每获得 ,理论上需消耗
,理论上需消耗_______ 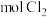 。
。
(4)某同学利用如图所示装置模拟吹出塔、吸收塔的实验,请回答下列问题:
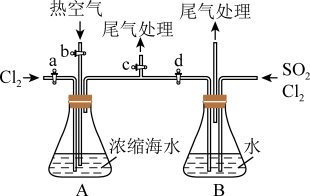
①进行吹出塔中实验时,应关闭活塞_______ ,打开活塞_______ 。
②可根据_______ (填现象),简单判断热空气的流速,通入热空气能吹出 的原因是
的原因是_______ 。
③装置B中要先通入 ,反应完全后再通入
,反应完全后再通入 ,简单判断通入的
,简单判断通入的 ,已反应完全的依据:
,已反应完全的依据:_______ 。

(1)进入吹出塔前海水中的
 与
与 发生反应的离子方程式为
发生反应的离子方程式为(2)已知:
 具有较强的氧化性,可氧化
具有较强的氧化性,可氧化 ,从吸收塔流出的溶液主要含
,从吸收塔流出的溶液主要含(3)两次通入
 的目的是富集浓缩溴,最终每获得
的目的是富集浓缩溴,最终每获得 ,理论上需消耗
,理论上需消耗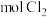 。
。(4)某同学利用如图所示装置模拟吹出塔、吸收塔的实验,请回答下列问题:

①进行吹出塔中实验时,应关闭活塞
②可根据
 的原因是
的原因是③装置B中要先通入
 ,反应完全后再通入
,反应完全后再通入 ,简单判断通入的
,简单判断通入的 ,已反应完全的依据:
,已反应完全的依据:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】江西稀土资源丰富。碳酸铈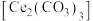 是一种稀土材料,工业上常以氟碳铈矿(主要成分为
是一种稀土材料,工业上常以氟碳铈矿(主要成分为 、
、 、
、 )为原料制备碳酸铈,其工艺流程如图所示
)为原料制备碳酸铈,其工艺流程如图所示 的
的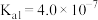 、
、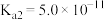 ,
, 的
的 。回答下列问题:
。回答下列问题:
(1)铈(Ce)原子序数为58,其在元素周期表中的位置______ 。
(2)“焙烧”中常采用高压空气、逆流操作(空气从焙烧炉下部通入,矿粉从中上部加入),这样操作的目的是______ 。
(3)滤渣A的主要成分为______ 、______ (写化学式)。
(4)硫脲结构为: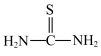 ,则硫脲中的键角:
,则硫脲中的键角: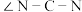
______  (填“大于”“小于”“等于”);硫脲与
(填“大于”“小于”“等于”);硫脲与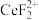 反应后生成物的结构为:
反应后生成物的结构为: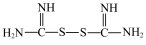 ,写出该反应的离子反应方程式
,写出该反应的离子反应方程式______ 。
(5)步骤④所发生的离子反应方程式______ ;常温下,若沉淀后溶液中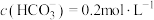 ,
,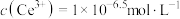 。此时溶液的
。此时溶液的
______ 。
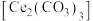 是一种稀土材料,工业上常以氟碳铈矿(主要成分为
是一种稀土材料,工业上常以氟碳铈矿(主要成分为 、
、 、
、 )为原料制备碳酸铈,其工艺流程如图所示
)为原料制备碳酸铈,其工艺流程如图所示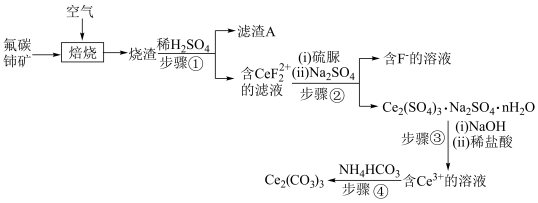
 的
的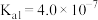 、
、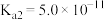 ,
, 的
的 。回答下列问题:
。回答下列问题:(1)铈(Ce)原子序数为58,其在元素周期表中的位置
(2)“焙烧”中常采用高压空气、逆流操作(空气从焙烧炉下部通入,矿粉从中上部加入),这样操作的目的是
(3)滤渣A的主要成分为
(4)硫脲结构为:
 ,则硫脲中的键角:
,则硫脲中的键角: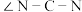
 (填“大于”“小于”“等于”);硫脲与
(填“大于”“小于”“等于”);硫脲与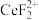 反应后生成物的结构为:
反应后生成物的结构为: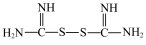 ,写出该反应的离子反应方程式
,写出该反应的离子反应方程式(5)步骤④所发生的离子反应方程式
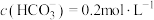 ,
,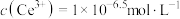 。此时溶液的
。此时溶液的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】为了将混有Na2SO4、NaHCO3的NaCl固体提纯,制得纯净的氯化钠溶液,某学习小组设计了如下图所示的实验方案:
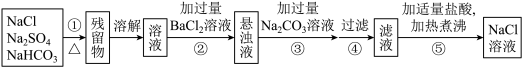
回答下列问题:
(1)操作①加热过程中,发生反应的化学方程式是_______ 。
(2)操作②不用Ba(NO3)2溶液的理由是:__________ 。
(3)进行操作②中,判断“BaCl2溶液是否过量”的方法是:_________ 。
(4)操作③“加入过量Na2CO3溶液”的目的是:________ 。
(5)操作⑤中“加适量盐酸”的主要目的是__________ 。

回答下列问题:
(1)操作①加热过程中,发生反应的化学方程式是
(2)操作②不用Ba(NO3)2溶液的理由是:
(3)进行操作②中,判断“BaCl2溶液是否过量”的方法是:
(4)操作③“加入过量Na2CO3溶液”的目的是:
(5)操作⑤中“加适量盐酸”的主要目的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有1L未知成分的混合溶液,其中除了含有0.2mol的Na+外,还可能含有下列离子中的一种或几种:
现进行如图实验操作(每次实验所加试剂均过量):
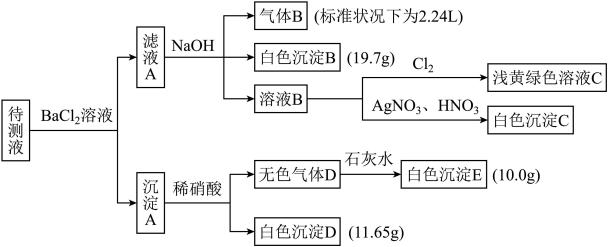
已知:①NH +OH-
+OH- NH3↑+H2O
NH3↑+H2O
②Cl2+2Br-=Br2+2Cl-
③Br2在常温下是深红棕色液体,微溶于水,其水溶液为黄色。
④标准状况下2.24L气体的物质的量为0.1mol。
(1)由气体B可确定待测液中含有的离子是_______ 。
(2)由沉淀D和沉淀E可以判断待测液中一定含有_______ 离子,据此可以排除的离子是_______ 。
(3)由白色沉淀B可确定待测液中含有的离子是_______ ,写出产生沉淀B的离子方程式_______ 。
(4)某同学读图后,认为待测液中一定不含Br-,他的判断依据是_______ 。
(5)综合分析,此1L待测液中K+的物质的量的取值范围为_______ 。
| 阳离子 | K+、NH 、Mg2+、Ba2+、Fe3+ 、Mg2+、Ba2+、Fe3+ |
| 阴离子 | Cl-、Br-、CO 、HCO 、HCO 、SO 、SO |

已知:①NH
 +OH-
+OH- NH3↑+H2O
NH3↑+H2O②Cl2+2Br-=Br2+2Cl-
③Br2在常温下是深红棕色液体,微溶于水,其水溶液为黄色。
④标准状况下2.24L气体的物质的量为0.1mol。
(1)由气体B可确定待测液中含有的离子是
(2)由沉淀D和沉淀E可以判断待测液中一定含有
(3)由白色沉淀B可确定待测液中含有的离子是
(4)某同学读图后,认为待测液中一定不含Br-,他的判断依据是
(5)综合分析,此1L待测液中K+的物质的量的取值范围为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】资源、能源、材料、环保、健康、安全等是当今社会重要的研究主题,化学与这些主题密切相关,在其研究与应用中发挥着重要作用。
Ⅰ.保证食品安全、保持营养均衡,是保障人体健康的基础。
(1)由于化学物质使用不当,给人印象不佳的化学名词越来越多:苏丹红、三聚氰胺……。下列做法不会危及人体健康的是_______(填字母)。
Ⅱ.20世纪90年代初,国际上提出了“预防污染”这一新概念。绿色化学是“预防污染”的根本手段,它的目标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各个环节中都实现净化和无污染。
(2)下列各项属于“绿色化学”要求的是_______ (填字母)。
A.处理污染物 B.治理污染点 C.杜绝污染源
Ⅲ.资源的利用有着重要的意义。我国具有广阔的海岸线,海洋中蕴含着丰富的资源。下面是海水综合利用联合工业体系的简图:
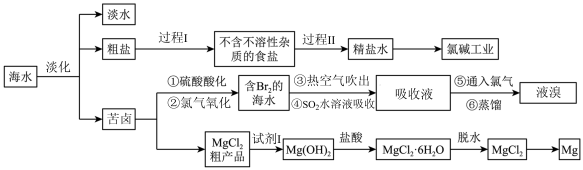
回答下列问题:
(3)过程I采用的操作是_______ 。
(4)工业上从海水中提取液溴的流程图中,步骤④除了用 吸收
吸收 外,理论上下列也能吸收
外,理论上下列也能吸收 的是_______(填字母)。
的是_______(填字母)。
(5)经过步骤①②已获得 ,不直接用含
,不直接用含 的海水进行蒸馏得到液溴,而要经过“热空气吹出、
的海水进行蒸馏得到液溴,而要经过“热空气吹出、 吸收、通入氯气”后再蒸馏,其目的是
吸收、通入氯气”后再蒸馏,其目的是_______ 。
(6)根据上述反应可判断 、
、 、
、 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是_______ 。
(7)为了使镁离子沉淀下来,并充分利用当地的贝壳(主要成分为碳酸钙)资源,加入的试剂I是_______ (填化学式)。
(8)步骤⑥的蒸馏过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:_______ 。
Ⅰ.保证食品安全、保持营养均衡,是保障人体健康的基础。
(1)由于化学物质使用不当,给人印象不佳的化学名词越来越多:苏丹红、三聚氰胺……。下列做法不会危及人体健康的是_______(填字母)。
| A.为改善食品品质而加入规定范围内的食品添加剂 |
| B.用霉变花生压榨食用油 |
| C.用小苏打做糕点的疏松剂 |
| D.用工业盐亚硝酸钠腌制鱼肉 |
Ⅱ.20世纪90年代初,国际上提出了“预防污染”这一新概念。绿色化学是“预防污染”的根本手段,它的目标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各个环节中都实现净化和无污染。
(2)下列各项属于“绿色化学”要求的是
A.处理污染物 B.治理污染点 C.杜绝污染源
Ⅲ.资源的利用有着重要的意义。我国具有广阔的海岸线,海洋中蕴含着丰富的资源。下面是海水综合利用联合工业体系的简图:

回答下列问题:
(3)过程I采用的操作是
(4)工业上从海水中提取液溴的流程图中,步骤④除了用
 吸收
吸收 外,理论上下列也能吸收
外,理论上下列也能吸收 的是_______(填字母)。
的是_______(填字母)。A. | B. | C. | D.NaCl |
 ,不直接用含
,不直接用含 的海水进行蒸馏得到液溴,而要经过“热空气吹出、
的海水进行蒸馏得到液溴,而要经过“热空气吹出、 吸收、通入氯气”后再蒸馏,其目的是
吸收、通入氯气”后再蒸馏,其目的是(6)根据上述反应可判断
 、
、 、
、 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是(7)为了使镁离子沉淀下来,并充分利用当地的贝壳(主要成分为碳酸钙)资源,加入的试剂I是
(8)步骤⑥的蒸馏过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】(1)油脂被摄入人体后,在酶的作用下水解为__________________ 和甘油(写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
(2)发育出现障碍,患营养缺乏症,这主要是由于摄取_________ (填“蛋白质”、“脂肪”或“糖类”)不足引起的。下列食物中富含该物质的是_________ (填字母)。
A.菠菜 B.花生油 C.瘦肉 D.西瓜
(3)某品牌抗酸药的成分主要有糖衣、碳酸钙、淀粉等。
①写出该抗酸药发挥功效时的离子方程式:______________________ 。
②淀粉在抗酸药中作填充剂、粘合剂,淀粉在人体内酶的催化作用下发生水解反应,写出其水解方程式:____________________________________ 。
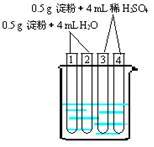
(4)上图所示4支试管同时水浴加热4min,为检验其中淀粉的水解程度,某同学的实验操作与现象记录如下:
①结合试管1、2中的现象,得出的结论是这两支试管中淀粉_____ 水解(填“没有”、“部分”或“全部”)。
②结合试管3、4中的现象,不能得出“这两支试管中淀粉没有水解”的结论,理由是____________ 。
(2)发育出现障碍,患营养缺乏症,这主要是由于摄取
A.菠菜 B.花生油 C.瘦肉 D.西瓜
(3)某品牌抗酸药的成分主要有糖衣、碳酸钙、淀粉等。
①写出该抗酸药发挥功效时的离子方程式:
②淀粉在抗酸药中作填充剂、粘合剂,淀粉在人体内酶的催化作用下发生水解反应,写出其水解方程式:

(4)上图所示4支试管同时水浴加热4min,为检验其中淀粉的水解程度,某同学的实验操作与现象记录如下:
| 编号 | 操作 | 现象 |
| 1 | 加入碘水 | 溶液变成蓝色 |
| 2 | 加入银氨溶液,水浴加热 | 未出现银镜 |
| 3 | 加入碘水 | 溶液变成蓝色 |
| 4 | 加入银氨溶液,水浴加热 | 未出现银镜 |
①结合试管1、2中的现象,得出的结论是这两支试管中淀粉
②结合试管3、4中的现象,不能得出“这两支试管中淀粉没有水解”的结论,理由是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】碘是人体必须的元素之一,海洋植物如海带、海藻中含有丰富的、以碘离子形式存在的碘元素。在实验室中,从海藻里提取碘的流程和实验装置如下:
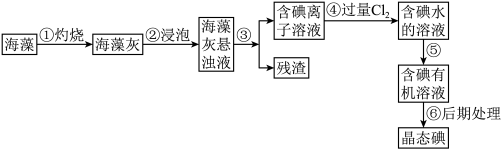
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是________ (填字母)。
A 烧杯 B 坩埚 C 表面皿 D 泥三角 E 酒精灯 F 干燥器
(2)步骤③的实验操作名称是____________ ,步骤⑤的操作名称是________ 。
(3)步骤④反应的离子方程式为_________________________________ 。
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:______________________ 。

请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
A 烧杯 B 坩埚 C 表面皿 D 泥三角 E 酒精灯 F 干燥器
(2)步骤③的实验操作名称是
(3)步骤④反应的离子方程式为
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】I.海洋植物如海带中含有丰富的碘元素,从海带中提取碘的实验需经过如下五个主要步骤:
①将海带灰转移到小烧杯中,向其中加入10 mL蒸馏水,搅拌、煮沸2—3 min;
②取3 g左右的干海带,剪碎后用酒精润湿,放入坩埚中,灼烧海带至完全变成灰烬,停止加热,冷却;
③向溶液中加入四氯化碳,振荡、静置、分液,得到含碘的有机溶液;
④向含碘离子的溶液中滴入几滴稀硫酸,再加入1 mL 3%H2O2溶液;
⑤过滤,得到含碘离子的溶液;
请回答下列问题:
(1)实验步骤的合理顺序是_______________ (填序号)
(2)步骤③中使用的主要仪器是____________
(3)步骤①中搅拌、煮沸2—3 min的目的是________________
(4)步骤④中反应的离子方程式是________________________________
Ⅱ.碲(Te,是第六主族元素)广泛用于彩色玻璃和陶瓷。工业上用精炼铜的阳极泥(主要含有TeO2、少量Ag、Au)为原料制备单质碲的一种工艺流程如下:
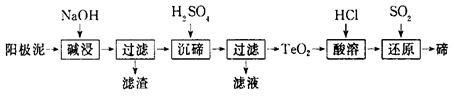
已知TeO2微溶于水,易溶于较浓的强酸和强碱。
(1)“碱浸”时发生反应的离子方程式为__________________
(2)碱浸后的“滤渣”可以部分溶于稀硝酸,发生反应的化学方程式是___________________________________
(3)“沉碲”时需控制溶液的pH值生成TeO2沉淀。酸性不能过强,其原因是__________________________________________
(4)“酸溶”后,将SO2通入TeCl4酸性溶液中进行“还原”得到碲,该反应的化学方程式是_________________________________________
①将海带灰转移到小烧杯中,向其中加入10 mL蒸馏水,搅拌、煮沸2—3 min;
②取3 g左右的干海带,剪碎后用酒精润湿,放入坩埚中,灼烧海带至完全变成灰烬,停止加热,冷却;
③向溶液中加入四氯化碳,振荡、静置、分液,得到含碘的有机溶液;
④向含碘离子的溶液中滴入几滴稀硫酸,再加入1 mL 3%H2O2溶液;
⑤过滤,得到含碘离子的溶液;
请回答下列问题:
(1)实验步骤的合理顺序是
(2)步骤③中使用的主要仪器是
(3)步骤①中搅拌、煮沸2—3 min的目的是
(4)步骤④中反应的离子方程式是
Ⅱ.碲(Te,是第六主族元素)广泛用于彩色玻璃和陶瓷。工业上用精炼铜的阳极泥(主要含有TeO2、少量Ag、Au)为原料制备单质碲的一种工艺流程如下:

已知TeO2微溶于水,易溶于较浓的强酸和强碱。
(1)“碱浸”时发生反应的离子方程式为
(2)碱浸后的“滤渣”可以部分溶于稀硝酸,发生反应的化学方程式是
(3)“沉碲”时需控制溶液的pH值生成TeO2沉淀。酸性不能过强,其原因是
(4)“酸溶”后,将SO2通入TeCl4酸性溶液中进行“还原”得到碲,该反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下图:
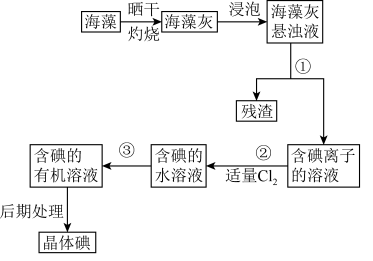
(1)实验室焙烧海带,需要下列仪器中的________ (填序号)。
a 试管 b 烧杯 c 坩埚 d 泥三角 e 铁三脚架 f 酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①__________ ,③________ 。
(3)提取碘的过程中,可选择的有机试剂是( )
A 甲苯、酒精 B 四氯化碳、苯
C 汽油、乙酸 D 汽油、甘油
(4)为使海藻灰中碘离子转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有__________ 、__________ 。
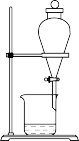
(5)小组用CCl4萃取碘水中的碘,在右图的分液漏斗中,下层液体呈__________ 色;
(6)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:
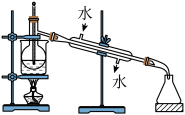
①____________________ ;
②_______________________________ ;
③____________________________ ;

(1)实验室焙烧海带,需要下列仪器中的
a 试管 b 烧杯 c 坩埚 d 泥三角 e 铁三脚架 f 酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①
(3)提取碘的过程中,可选择的有机试剂是
A 甲苯、酒精 B 四氯化碳、苯
C 汽油、乙酸 D 汽油、甘油
(4)为使海藻灰中碘离子转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有

(5)小组用CCl4萃取碘水中的碘,在右图的分液漏斗中,下层液体呈
(6)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:

①
②
③
您最近一年使用:0次



