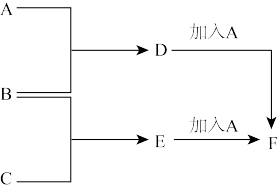
已知有以下物质的相互转化:

试回答:
(1)B的化学式为_____ ;D的化学式为_____ 。
(2)写出由E转变成F的化学方程式:______ 。
(3)常用____ (填试剂名称)检验G中的阳离子,其现象为______ 。
(4)向G溶液中加入A的有关反应的离子方程式为________ 。

试回答:
(1)B的化学式为
(2)写出由E转变成F的化学方程式:
(3)常用
(4)向G溶液中加入A的有关反应的离子方程式为
18-19高一下·云南文山·阶段练习 查看更多[6]
云南省广南二中2018-2019学年高一6月份考试化学试题甘肃省兰州市联片办学2019-2020学年高一上学期期末考试化学试题甘肃省天水市2019-2020学年高一上学期期末考试化学试题广西南宁市邕宁高中2020-2021学年高一上学期期末考试化学试题(已下线)易错专题23 Fe2+和Fe3+的检验与转化-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)新疆哈密市第十五中学2021-2022学年高一上学期期末考试化学试题
更新时间:2019-06-30 10:33:34
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下列图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物,B为淡黄色固体。
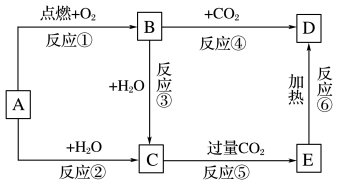
回答下列问题:
(1)写出化学式:A_____________ ,D_____________ 。
(2)写出基本反应类型:反应①_____________ ,反应②_____________ 。
(3)反应③的化学方程式为_______________________________________ 。
(4)向D溶液中通入 ,反应的化学方程式为
,反应的化学方程式为_______________________________________ 。

回答下列问题:
(1)写出化学式:A
(2)写出基本反应类型:反应①
(3)反应③的化学方程式为
(4)向D溶液中通入
 ,反应的化学方程式为
,反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A为常见的金属单质,根据如图所示的关系:
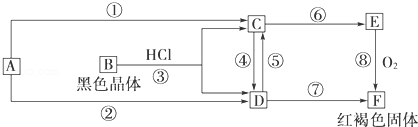
(1)确定A、B、C、D、E、F的化学式,A为_________ ,B为________ ,C为________ ,D为________ ,E为________ ,F为________ .
(2)写出③、④、⑤的离子方程式.
③_________________________ .
④_________________________ .
⑤_________________________ .

(1)确定A、B、C、D、E、F的化学式,A为
(2)写出③、④、⑤的离子方程式.
③
④
⑤
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E五种可溶性化合物,分别由阳离子Fe3+、 Ba2+、Al3+、Na+、Ag+和阴离子NO3-、OH-、SO42-、Cl-、CO32-中的各一种组成(离子不重复)。现做如下实验:
①A和E的溶液显碱性,0.1mol/L A溶液的pH小于13;
②在B的溶液中逐滴加入氨水有白色沉淀生成,继续加氨水至过量,沉淀消失;
③在C的溶液中加入铁粉,溶液的质量增加;
④在D的溶液中加入过量的Ba(OH)2溶液,没有沉淀。
(1)根据以上事实推断A-E的化学式:
A__________ 、B___________ 、C___________ 、E__________
(2)写出①A溶液呈碱性和③的离子方程式:
①_____________________________
③_____________________________
①A和E的溶液显碱性,0.1mol/L A溶液的pH小于13;
②在B的溶液中逐滴加入氨水有白色沉淀生成,继续加氨水至过量,沉淀消失;
③在C的溶液中加入铁粉,溶液的质量增加;
④在D的溶液中加入过量的Ba(OH)2溶液,没有沉淀。
(1)根据以上事实推断A-E的化学式:
A
(2)写出①A溶液呈碱性和③的离子方程式:
①
③
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】乳酸亚铁晶体[CH3CH(OH)COO]2Fe·2H2O是一种很好的食品铁强化剂,可由乳酸钙与FeCl2反应制得,制备流程如图:
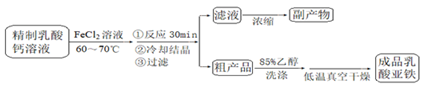
反应装置如图所示:
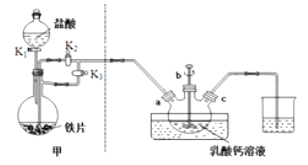
已知:1.潮湿的乳酸亚铁易被氧化。
2.物质的溶解性:乳酸钙:溶于冷水,易溶于热水;乳酸亚铁:溶于冷水和热水,难溶于乙醇。
请回答:
(1)盛放乳酸钙溶液的装置的名称为___ 。
(2)部分实验操作过程如下,请按正确操作顺序填入字母,其正确的操作顺序是:___ 。
检查气密性→按图示要求加入试剂→将三颈烧瓶置于水浴中→( )→( )一(f)→( )→( )→( )→开动搅拌器→……
a.关闭K1;
b.盖上分液漏斗上口玻璃塞;
c.关闭K3,打开K2;
d.关闭K2,打开K3;
e.打开分液漏斗上口玻璃塞;
f.打开K1
(3)该装置制备乳酸亚铁的优点是___ ,副产物为___ 。
(4)下列说法正确的是___ 。
A.装置甲中的主要仪器是球形分液漏斗和蒸馏烧瓶
B.本实验采用较大铁片而不是铁粉的主要原因是控制反应速率,防止进入三颈烧瓶的氯化亚铁过多,反应过于剧烈
C.乳酸亚铁悬浊液应从b口倒出进行抽滤,并用滤液洗涤三颈烧瓶,将洗涤液倒入布氏漏斗再次抽滤
D.粗产品的洗涤液,经蒸馏后所得的残留液,与滤液混合可提高副产物的产量
(5)有同学提出可直接用KMnO4滴定法测定样品中的Fe2+量进而计算纯度,但实验后发现结果总是大于100%,其主要原因可能是___ 。

反应装置如图所示:

已知:1.潮湿的乳酸亚铁易被氧化。
2.物质的溶解性:乳酸钙:溶于冷水,易溶于热水;乳酸亚铁:溶于冷水和热水,难溶于乙醇。
请回答:
(1)盛放乳酸钙溶液的装置的名称为
(2)部分实验操作过程如下,请按正确操作顺序填入字母,其正确的操作顺序是:
检查气密性→按图示要求加入试剂→将三颈烧瓶置于水浴中→( )→( )一(f)→( )→( )→( )→开动搅拌器→……
a.关闭K1;
b.盖上分液漏斗上口玻璃塞;
c.关闭K3,打开K2;
d.关闭K2,打开K3;
e.打开分液漏斗上口玻璃塞;
f.打开K1
(3)该装置制备乳酸亚铁的优点是
(4)下列说法正确的是
A.装置甲中的主要仪器是球形分液漏斗和蒸馏烧瓶
B.本实验采用较大铁片而不是铁粉的主要原因是控制反应速率,防止进入三颈烧瓶的氯化亚铁过多,反应过于剧烈
C.乳酸亚铁悬浊液应从b口倒出进行抽滤,并用滤液洗涤三颈烧瓶,将洗涤液倒入布氏漏斗再次抽滤
D.粗产品的洗涤液,经蒸馏后所得的残留液,与滤液混合可提高副产物的产量
(5)有同学提出可直接用KMnO4滴定法测定样品中的Fe2+量进而计算纯度,但实验后发现结果总是大于100%,其主要原因可能是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
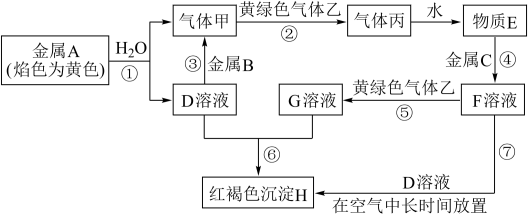
请根据以上信息完成下列各题:
(1)写出下列物质的化学式:C___ ,丙___ 。
(2)写出实验室制备黄绿色气体乙的化学方程式:___ ,过程⑦可能观察到的实验现象是:__ 。
(3)写出过程⑦涉及的化学方程式___ ,___ 。
(4)反应③中的离子方程式是___ 。

请根据以上信息完成下列各题:
(1)写出下列物质的化学式:C
(2)写出实验室制备黄绿色气体乙的化学方程式:
(3)写出过程⑦涉及的化学方程式
(4)反应③中的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请回答下列问题:
(1)FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)_______ 。
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。完成NaClO3氧化FeCl2的离子方程式:_______
某化学研究性学习小组探究Fe3+和 之间发生的反应
之间发生的反应
(3)取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。无气泡产生,无沉淀生成。除了观察到以上的现象外,有成员提出了另一种可能:发生氧化还原反应。反应的离子方程式为_______ 。
(4)研究性学习小组设计了两种实验方案证明发生了氧化还原反应。请把实验方案补充完整:
(方案一)检验溶液中含有Fe2+证明发生了氧化还原反应
(方案二)检验溶液中含有_______ 证明发生了氧化还原反应
Ⅰ.预处理:将(方案一)中获得的混合物放在如图装置中处理足够时间。

Ⅱ.检验过程
①简述证明溶液中含有Fe2+的操作方法及现象:_______ ;
②检验溶液中含有另一种离子可选用的试剂是:_______ 。
(1)FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。完成NaClO3氧化FeCl2的离子方程式:
某化学研究性学习小组探究Fe3+和
 之间发生的反应
之间发生的反应(3)取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。无气泡产生,无沉淀生成。除了观察到以上的现象外,有成员提出了另一种可能:发生氧化还原反应。反应的离子方程式为
(4)研究性学习小组设计了两种实验方案证明发生了氧化还原反应。请把实验方案补充完整:
(方案一)检验溶液中含有Fe2+证明发生了氧化还原反应
(方案二)检验溶液中含有
Ⅰ.预处理:将(方案一)中获得的混合物放在如图装置中处理足够时间。

Ⅱ.检验过程
①简述证明溶液中含有Fe2+的操作方法及现象:
②检验溶液中含有另一种离子可选用的试剂是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】Ⅰ.某工厂的酸性废水中主要含有 、
、 等离子,为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾 (
等离子,为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾 ( )。
)。
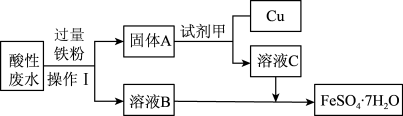
(1)操作Ⅰ是_______ ;试剂甲是_______ (填化学式)。
(2)获得的 需密闭保存,原因是
需密闭保存,原因是_______ 。
(3)绿矾可消除某种酸性工业废水中+6价铬( )的污染,使之转化为毒性较小的
)的污染,使之转化为毒性较小的 ,该反应的离子方程式是
,该反应的离子方程式是_______ 。
(4)黄铜是铜锌合金,是用来制造铜钱的原料,能鉴别黄铜中有金属锌的试剂是_______ 。
Ⅱ.某小组为探究 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:
【查阅资料】稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。氧化性强弱探究:
【分析与解释】
(5)实验Ⅰ中a试管中反应的离子方程式是_______ 。
(6)①甲同学认为:实验Ⅱ观察到_______ 现象,得出氧化性 。
。
②乙同学对上述实验进行反思,认为实验Ⅱ不能充分证明氧化性 ;他补做了实验Ⅲ。补做实验Ⅲ的目的是
;他补做了实验Ⅲ。补做实验Ⅲ的目的是_______ 。
 、
、 等离子,为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾 (
等离子,为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾 ( )。
)。
(1)操作Ⅰ是
(2)获得的
 需密闭保存,原因是
需密闭保存,原因是(3)绿矾可消除某种酸性工业废水中+6价铬(
 )的污染,使之转化为毒性较小的
)的污染,使之转化为毒性较小的 ,该反应的离子方程式是
,该反应的离子方程式是(4)黄铜是铜锌合金,是用来制造铜钱的原料,能鉴别黄铜中有金属锌的试剂是
Ⅱ.某小组为探究
 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:【查阅资料】稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。氧化性强弱探究:
| 实验Ⅰ | 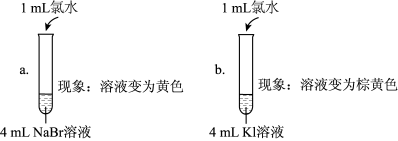 |
| 实验Ⅱ | 取a中的黄色溶液少许,加入KI溶液,再加入淀粉溶液 |
| 实验Ⅲ | 另取a中的黄色溶液少许,先加入足量的NaBr固体,充分振荡,然后加入KI溶液和淀粉溶液 |
(5)实验Ⅰ中a试管中反应的离子方程式是
(6)①甲同学认为:实验Ⅱ观察到
 。
。②乙同学对上述实验进行反思,认为实验Ⅱ不能充分证明氧化性
 ;他补做了实验Ⅲ。补做实验Ⅲ的目的是
;他补做了实验Ⅲ。补做实验Ⅲ的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
【推荐3】聚合硫酸铁又称聚铁,化学式[Fe2(OH)n(SO4)3-0.5n]n,广泛用于污水处理,实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、 SiO2等)制备聚铁和绿矾(FeSO4·7H2O),过程如下:
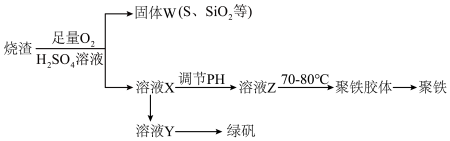
(1)验证固体W焙烧后产生的气体含有SO2的方法是_____________ 。
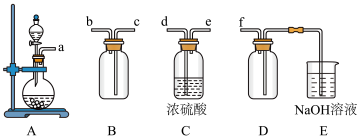
(2)实验室制备,收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器口,顺序为a→_____ →_____ →_____ →_____ →f。装置D的作用是_________ ,装置E中NaOH溶液的作用是________________ 。
(3)制备绿矾时,向溶液X中加入过量_________ ,充分反应后,经_________ 操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾。
(4)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH的操作方法为________ 。
若溶液Z的pH偏小,将导致聚铁中铁的质量分数偏_____________________ 。

(1)验证固体W焙烧后产生的气体含有SO2的方法是
(2)实验室制备,收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器口,顺序为a→

(3)制备绿矾时,向溶液X中加入过量
(4)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH的操作方法为
若溶液Z的pH偏小,将导致聚铁中铁的质量分数偏
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A为金属单质,下列物质相互转化如图所示:
试回答:
(1)写出B的化学式____ ,D的化学式__________ 。
(2)写出由E转变成F的化学方程式____ 。
(3)向G溶液加入A的有关离子反应方程式______________________ 。
(4)某同学取B的溶液酸化后加入碘化钾淀粉溶液,在空气中放置一会儿变为蓝色,写出与上述变化过程相关的离子方程式____________ ,______________ 。

试回答:
(1)写出B的化学式
(2)写出由E转变成F的化学方程式
(3)向G溶液加入A的有关离子反应方程式
(4)某同学取B的溶液酸化后加入碘化钾淀粉溶液,在空气中放置一会儿变为蓝色,写出与上述变化过程相关的离子方程式
您最近一年使用:0次
【推荐2】食盐是日常生活的必需品,也是重要的化工原料。
I.海水中含有大量的NaCl,以及少量的 、
、 、
、 等离子。
等离子。
(1)①为得到纯净的饱和NaCl溶液,进行了如下操作,请补全操作步骤:
a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中加入过量氢氧化钡溶液,过滤;
c.向滤液中加入过量_______ 溶液,过滤;
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
②步骤b中反应的离子方程式是_______ 。
(2)加入足量的稀盐酸的目的是:_______ 。
II.某透明溶液中可能大量存在 、
、 、
、 、
、 、
、 中的几种离子。
中的几种离子。
(3)取少量原溶液,向其中加入过量NaOH溶液,有白色沉淀生成,迅速变为灰绿色,最后变成红褐色,说明原溶液中肯定存在的离子是_______ ,有关反应的离子方程式为_______ 、_______ 。
(4)检验原溶液中是否存在 的实验方法是
的实验方法是_______ 。
I.海水中含有大量的NaCl,以及少量的
 、
、 、
、 等离子。
等离子。(1)①为得到纯净的饱和NaCl溶液,进行了如下操作,请补全操作步骤:
a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中加入过量氢氧化钡溶液,过滤;
c.向滤液中加入过量
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
②步骤b中反应的离子方程式是
(2)加入足量的稀盐酸的目的是:
II.某透明溶液中可能大量存在
 、
、 、
、 、
、 、
、 中的几种离子。
中的几种离子。(3)取少量原溶液,向其中加入过量NaOH溶液,有白色沉淀生成,迅速变为灰绿色,最后变成红褐色,说明原溶液中肯定存在的离子是
(4)检验原溶液中是否存在
 的实验方法是
的实验方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】如图所示装置可用来制取Fe(OH)2和观察Fe(OH)2被氧化时的颜色变化,实验时必须使用铁屑、6mol/L硫酸,其他试剂任选。回答下列问题:
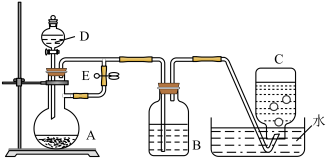
(1)仪器D的名称为________ ,该仪器中需要放入__________ ,装置B中盛有一定量的NaOH溶液,装置A中应预先加入的试剂是______ ,装置A中发生反应的离子方程式为___________ 。
(2)实验开始时应先将止水夹E______ (填“打开”或“关闭”),装置C中收集到的气体主要为______ ;待装置中空气排尽后,将止水夹E______ (填“打开”或“关闭”),此时装置B中可能发生的化学反应是:__________ (用离子方程式表示)。
(3)拔去装置B中的橡胶塞,使空气进入,此时B中发生反应的化学方程式为_________ 。

(1)仪器D的名称为
(2)实验开始时应先将止水夹E
(3)拔去装置B中的橡胶塞,使空气进入,此时B中发生反应的化学方程式为
您最近一年使用:0次