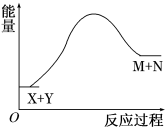
已知X+Y M+N反应中的能量变化过程如图,则下列有关说法正确的是
M+N反应中的能量变化过程如图,则下列有关说法正确的是
 M+N反应中的能量变化过程如图,则下列有关说法正确的是
M+N反应中的能量变化过程如图,则下列有关说法正确的是
| A.X的能量一定低于M的能量,Y的能量一定低于N的能量 |
| B.破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量 |
| C.因为该反应为吸热反应,故一定要加热反应才能进行 |
| D.加入催化剂,可减小M+N与X+Y间的能量差 |
更新时间:2019-06-28 09:36:37
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某反应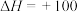 kJ/mol,下列有关该反应的叙述正确的是
kJ/mol,下列有关该反应的叙述正确的是
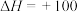 kJ/mol,下列有关该反应的叙述正确的是
kJ/mol,下列有关该反应的叙述正确的是| A.正反应活化能小于100 kJ/mol | B.逆反应活化能一定小于100 kJ/mol |
| C.正反应活化能不小于100 kJ/mol | D.正反应活化能比逆反应活化能大100 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是( )
| A.SO3溶于水放出大量的热,该反应为放热反应 |
| B.碳酸钙受热分解的反应中生成物总能量低于反应物总能量 |
| C.已知反应 C(石墨)→C(金刚石)的反应热ΔH>0,则金刚石比石墨稳定 |
| D.相同质量气态水比液态水熵值高,因此气态水更稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法
| A.ΔH < 0为放热反应 |
| B.化学键断裂与形成时的能量变化是化学变化中能量变化的主要原因 |
| C.在25℃和101 kPa时,相同浓度的盐酸、醋酸溶液分别与NaOH溶液发生中和反应生成1 mol H2O时,放出的热量相等 |
| D.已知甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g) + 2O2(g) =CO2(g) + 2H2O(l) ΔH = -890.3 kJ·mol-1 |
您最近一年使用:0次
【推荐2】下列图示与对应的叙述相符的是

| A.图甲代表浓H2SO4稀释过程中体系的能量变化 |
| B.图乙表示反应物断键吸收的能量小于生成物成键放出的能量 |
| C.图丙表示白磷比红磷稳定 |
| D.图丁表示CO与H2O的反应过程与能量变化的关系 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】反应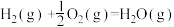 的能量变化如图所示。已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1molH-O键形成时放出热量463kJ。以下说法错误的是
的能量变化如图所示。已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1molH-O键形成时放出热量463kJ。以下说法错误的是

①c代表总反应放出的能量,为121kJ
②b代表新的化学键形成吸收的能量,为463kJ
③氢气中1molH-H键断裂时吸收热量为436kJ
④此反应为放热反应,所以无需加热就能进行
⑤NH4Cl晶体与Ba(OH)2·8H2O晶体混合搅拌与此反应的ΔH都<0
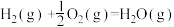 的能量变化如图所示。已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1molH-O键形成时放出热量463kJ。以下说法错误的是
的能量变化如图所示。已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1molH-O键形成时放出热量463kJ。以下说法错误的是
①c代表总反应放出的能量,为121kJ
②b代表新的化学键形成吸收的能量,为463kJ
③氢气中1molH-H键断裂时吸收热量为436kJ
④此反应为放热反应,所以无需加热就能进行
⑤NH4Cl晶体与Ba(OH)2·8H2O晶体混合搅拌与此反应的ΔH都<0
| A.①③④⑤ | B.②③④ | C.①②④⑤ | D.全部 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验是高中化学最重要的组成部分。下列有关实验的说法正确的是


| A.将实验(a)中的铝片更换为等质量的铝粉后,释放出的热量会增加 |
| B.实验(b)说明自发反应必须熵增 |
| C.实验(c)测定反应热时,需要将盐酸和氢氧化钠溶液快速混合 |
| D.实验(d)在滴定过程中,将标准盐酸溶液装入如图酸式滴定管(下端为橡胶管)进行滴定 |
您最近一年使用:0次

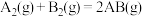 的能量变化如图所示,则下列说法中正确的是
的能量变化如图所示,则下列说法中正确的是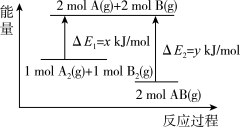
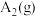 、
、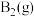 、
、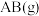 中,最稳定的物质一定是
中,最稳定的物质一定是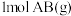 放出
放出 的能量
的能量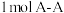 键和
键和 键要吸收
键要吸收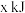 的能量
的能量

