下图是两个实验小组分别进行“加热硫酸铜和氢氧化钠溶液反应后生成物”的实验过程示意图
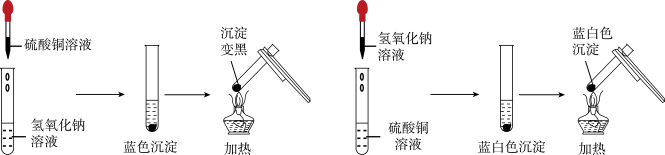
甲组 乙组
【甲组】氢氧化钠与硫酸铜反应的化学方程式为___________ ,加热后产生黑色的氧化铜。
【乙组】为寻找实验中没有产生氧化铜的原因,他们进行了以下实验探究:
【查阅资料】在酸性条件下,氢氧化钠与硫酸铜在溶液中可发生如下反应:6NaOH+4CuSO4=3Na2SO4+Cu4(OH)6SO4↓,生成的碱式硫酸铜是不溶于水的蓝白色固体,加热不易发生分解。
【提出猜想】根据资料分析,同学们针对试管中溶液呈酸性的原因做出了以下猜想:
猜想Ⅰ:硫酸铜溶液呈酸性 猜想Ⅱ:生成的硫酸钠使溶液呈酸性。
【实验与结论】
实验①:用pH试纸测定硫酸铜溶液的酸碱度,得出其pH______ 7(填“>”、“<”或“=”),硫酸铜溶液呈酸性,猜想Ⅰ成立。
实验②:向盛有硫酸钠溶液的试管中滴加石蕊溶液,观察到溶液显紫色,硫酸钠溶液呈______ (填“酸”、“中”或“碱”)性,猜想Ⅱ不成立。
【交流与反思】(1)乙同学认真分析甲组实验后,一致认为不需要通过实验就能判断猜想Ⅱ不成立,理由是_________ 。
(2)在化学反应中,相同的反应物因其质量比不同可能会导致生产物不同,请另举一例______ (写出反应物即可)。

甲组 乙组
【甲组】氢氧化钠与硫酸铜反应的化学方程式为
【乙组】为寻找实验中没有产生氧化铜的原因,他们进行了以下实验探究:
【查阅资料】在酸性条件下,氢氧化钠与硫酸铜在溶液中可发生如下反应:6NaOH+4CuSO4=3Na2SO4+Cu4(OH)6SO4↓,生成的碱式硫酸铜是不溶于水的蓝白色固体,加热不易发生分解。
【提出猜想】根据资料分析,同学们针对试管中溶液呈酸性的原因做出了以下猜想:
猜想Ⅰ:硫酸铜溶液呈酸性 猜想Ⅱ:生成的硫酸钠使溶液呈酸性。
【实验与结论】
实验①:用pH试纸测定硫酸铜溶液的酸碱度,得出其pH
实验②:向盛有硫酸钠溶液的试管中滴加石蕊溶液,观察到溶液显紫色,硫酸钠溶液呈
【交流与反思】(1)乙同学认真分析甲组实验后,一致认为不需要通过实验就能判断猜想Ⅱ不成立,理由是
(2)在化学反应中,相同的反应物因其质量比不同可能会导致生产物不同,请另举一例
更新时间:2019-10-15 09:14:32
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】已知Cu(OH)2沉淀在一定的条件下可以溶解在氨水中,有关反应的化学方程式为:Cu(OH)2+4NH3·H2O [Cu(NH3)4]2++2OH-+4H2O,有下列实验操作:
[Cu(NH3)4]2++2OH-+4H2O,有下列实验操作:
(1)操作1:在盛有3 mL 0.1 mol·L-1 CuSO4溶液的试管中滴加3 mL 0.2 mol·L-1 NaOH溶液,结果出现蓝色的悬浊液,有关反应的离子方程式为___________ 。
(2)操作2:在盛有3 mL 0.1 mol·L-1 CuSO4溶液的试管中滴加3 mL 0.2 mol·L-1氨水,结果也出现蓝色的悬浊液,有关反应的离子方程式为___________ 。
(3)在上述两种悬浊液中分别加入2 mol·L-1的氨水溶解,请从平衡移动的角度思考哪一种悬浊液更易溶解成为清液?__________ (填“操作1”或“操作2”);理由是_____________ 。
(4)请你设计一个简单的实验方案验证上述观点(或理由)的可靠性。实验方案:______ 。
 [Cu(NH3)4]2++2OH-+4H2O,有下列实验操作:
[Cu(NH3)4]2++2OH-+4H2O,有下列实验操作:(1)操作1:在盛有3 mL 0.1 mol·L-1 CuSO4溶液的试管中滴加3 mL 0.2 mol·L-1 NaOH溶液,结果出现蓝色的悬浊液,有关反应的离子方程式为
(2)操作2:在盛有3 mL 0.1 mol·L-1 CuSO4溶液的试管中滴加3 mL 0.2 mol·L-1氨水,结果也出现蓝色的悬浊液,有关反应的离子方程式为
(3)在上述两种悬浊液中分别加入2 mol·L-1的氨水溶解,请从平衡移动的角度思考哪一种悬浊液更易溶解成为清液?
(4)请你设计一个简单的实验方案验证上述观点(或理由)的可靠性。实验方案:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】兴趣小组通过实验探究溶解铜的方法和本质。
(1)将铜粉分别加到稍过量的氯化铁溶液和硫酸铁溶液中,铜粉溶解,溶液变成浅绿色,两个反应的共同点是(用离子方程式表示)_______ 。
(2)在热水浴中进行4个实验,部分实验报告如下表所示。
①实验操作Ⅲ是_______ 。
②实验I、Ⅱ、Ⅲ的目的是_______ 。
③实验Ⅳ中反应的本质是(用离子方程式表示)_______ 。
(3)将铜粉加到混有硫酸的过氧化氢溶液中,溶液逐渐变成蓝色,该反应的离子方程式是_______ 。
(1)将铜粉分别加到稍过量的氯化铁溶液和硫酸铁溶液中,铜粉溶解,溶液变成浅绿色,两个反应的共同点是(用离子方程式表示)
(2)在热水浴中进行4个实验,部分实验报告如下表所示。
| 序号 | 实验操作 | 实验现象 |
| Ⅰ | 稀硫酸中加入铜片 | 无明显变化 |
| Ⅱ | 硝酸钠溶液中加入铜片 | 无明显变化 |
| Ⅲ | 无明显变化 | |
| Ⅳ | 稀硫酸中加入硝酸钠溶液 | 无明显变化 |
| 再加入铜片 | 有无色气泡;溶液变蓝 |
②实验I、Ⅱ、Ⅲ的目的是
③实验Ⅳ中反应的本质是(用离子方程式表示)
(3)将铜粉加到混有硫酸的过氧化氢溶液中,溶液逐渐变成蓝色,该反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某中学有甲、乙两个探究性学习小组,他们拟用一定质量的纯铝片与足量稀硫酸的反应测定通常状况(约20℃,101kPa)下气体摩尔体积的方法.
(1)甲组同学拟选用下列实验装置完成实验(如图):
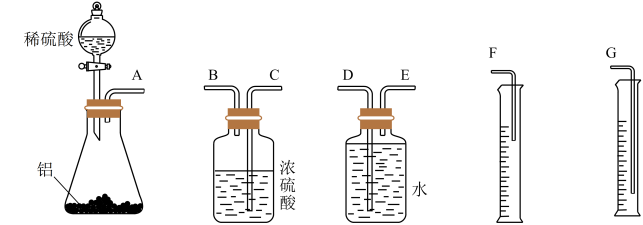
①该组同学必须选用的装置的连接顺序是A接______ 接 ______ 接_____ (填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.请你帮助分析原因______
③实验结束时,该组同学应怎样测量实验中生成氢气的体积?_______
(2)乙组同学仔细分析甲组同学的实验装置后,认为:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小.于是他们设计了如图所示的实验装置.装置中导管a的作用是______
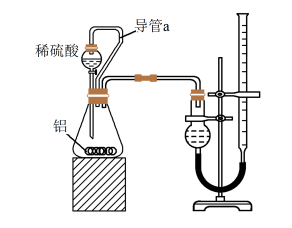
(1)甲组同学拟选用下列实验装置完成实验(如图):

①该组同学必须选用的装置的连接顺序是A接
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.请你帮助分析原因
③实验结束时,该组同学应怎样测量实验中生成氢气的体积?
(2)乙组同学仔细分析甲组同学的实验装置后,认为:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小.于是他们设计了如图所示的实验装置.装置中导管a的作用是

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】全球对锂资源的需求不断增长,从海水、盐湖中提取锂越来越受到重视。金属锂(Li)的化学性质与镁相似,在加热的条件下锂能与氮气反应生成氮化锂( ,遇水剧烈反应)。某课题组设计了如图实验装置制备氮化锂(部分夹持装置省略)并测定其纯度。回答下列问题:
,遇水剧烈反应)。某课题组设计了如图实验装置制备氮化锂(部分夹持装置省略)并测定其纯度。回答下列问题:
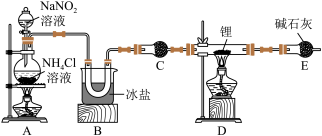
已知:实验室可用饱和亚硝酸钠 溶液与饱和氯化铵
溶液与饱和氯化铵 溶液经加热后反应制取氮气,该反应为放热反应。
溶液经加热后反应制取氮气,该反应为放热反应。
(1)盛装 溶液的仪器名称为
溶液的仪器名称为_______ 。
(2)实验开始先点燃_______ (填“A”或“D”)处酒精灯,这样做的目的是_______ 。
(3)经查阅资料得知,装置 处不需要持续加热,分析可能原因:
处不需要持续加热,分析可能原因:_______ ;装置 的作用是
的作用是_______ ;装置C中盛装的试剂为碱石灰,其作用为_______ 。
(4)测定 产品纯度:取
产品纯度:取 产品于蒸馏烧瓶中,打开止水夹,通过安全漏斗向蒸馏烧瓶中加入足量的水,装置如图。
产品于蒸馏烧瓶中,打开止水夹,通过安全漏斗向蒸馏烧瓶中加入足量的水,装置如图。 遇水发生反应的化学方程式为
遇水发生反应的化学方程式为_______ ;G中的液体可选择_______ (填标号)。

A.蒸馏水 B.煤油 C.石蜡油 D.饱和食盐水
(5)当反应完全后,测得 体积为
体积为 (已折合成标准状况)。该
(已折合成标准状况)。该 产品的纯度为
产品的纯度为_______ %。
 ,遇水剧烈反应)。某课题组设计了如图实验装置制备氮化锂(部分夹持装置省略)并测定其纯度。回答下列问题:
,遇水剧烈反应)。某课题组设计了如图实验装置制备氮化锂(部分夹持装置省略)并测定其纯度。回答下列问题:
已知:实验室可用饱和亚硝酸钠
 溶液与饱和氯化铵
溶液与饱和氯化铵 溶液经加热后反应制取氮气,该反应为放热反应。
溶液经加热后反应制取氮气,该反应为放热反应。(1)盛装
 溶液的仪器名称为
溶液的仪器名称为(2)实验开始先点燃
(3)经查阅资料得知,装置
 处不需要持续加热,分析可能原因:
处不需要持续加热,分析可能原因: 的作用是
的作用是(4)测定
 产品纯度:取
产品纯度:取 产品于蒸馏烧瓶中,打开止水夹,通过安全漏斗向蒸馏烧瓶中加入足量的水,装置如图。
产品于蒸馏烧瓶中,打开止水夹,通过安全漏斗向蒸馏烧瓶中加入足量的水,装置如图。 遇水发生反应的化学方程式为
遇水发生反应的化学方程式为
A.蒸馏水 B.煤油 C.石蜡油 D.饱和食盐水
(5)当反应完全后,测得
 体积为
体积为 (已折合成标准状况)。该
(已折合成标准状况)。该 产品的纯度为
产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】劳动实践课上同学们用草木灰给农作物施肥。课后同学查阅资料,得知草木灰是一种重要的农家肥,碳酸钾含量高。
【提出问题】
如何测定草木灰中碳酸钾的含量?
【查阅资料】
1.常见草木灰钾含量(以碳酸钾表示)如下表:
2.提取碳酸钾主要过程是:秸秆→草木灰→滤液→固体
(1)表格中钾含量最高的草木灰是_______ ,同学们选用这种秸秆灰提取碳酸钾。
【设计与实验】
实验一:提取碳酸钾
第一步:燃烧秸秆,收集草木灰,称取20.00g。
第二步:用60℃水浸洗草木灰(如图1)并过滤,浸洗滤渣2次,合并滤液。
第三步:蒸发滤液,烘干得到9.90g固体。
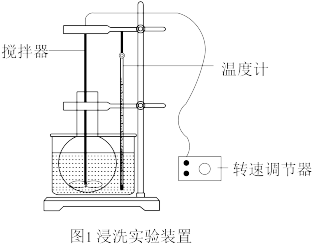
(2)图1实验中,用60℃的温水而不用冷水浸洗的原因是_______ 。
(3)根据图2,搅拌器转速控制在每分钟_______ 转,浸取时间为_______ 分钟,比较适宜。
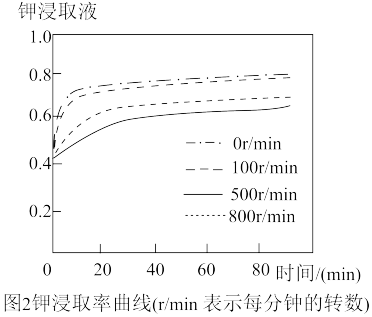
实验二:测定碳酸钾含量
取实验一中所得固体3.30g进行图3实验。
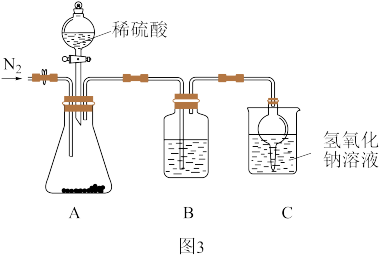
(4)实验中需缓慢滴入稀硫酸,原因是_______ 。
(5)装置B的作用是_______ 。
【数据与解释】
(6)称量图3中反应前后烧杯和其中溶液的总质量,增重0.92g。计算草木灰中碳酸钾的质量分数为_______ %,与表格中数据相比明显偏低,原因可能是_______ (填序号)。
a.烧杯中溶液与空气接触 b.固体含有其它钾盐 c.固体含有氯化钠
【反思与评价】
(7)我国秸秆产量巨大,可作为生物质发电的原料,还可利用其燃烧发电产生的草木灰提取碳酸钾,其优点有_______ (写一条)。
【提出问题】
如何测定草木灰中碳酸钾的含量?
【查阅资料】
1.常见草木灰钾含量(以碳酸钾表示)如下表:
| 草木灰种类 | 小灌木灰 | 稻草灰 | 小麦秆灰 | 棉壳灰 | 棉秆灰 | 向日葵杆灰 |
 (%) (%) | 8.66 | 2.63 | 20.26 | 32.28 | 16.44 | 51.97 |
(1)表格中钾含量最高的草木灰是
【设计与实验】
实验一:提取碳酸钾
第一步:燃烧秸秆,收集草木灰,称取20.00g。
第二步:用60℃水浸洗草木灰(如图1)并过滤,浸洗滤渣2次,合并滤液。
第三步:蒸发滤液,烘干得到9.90g固体。

(2)图1实验中,用60℃的温水而不用冷水浸洗的原因是
(3)根据图2,搅拌器转速控制在每分钟

实验二:测定碳酸钾含量
取实验一中所得固体3.30g进行图3实验。

(4)实验中需缓慢滴入稀硫酸,原因是
(5)装置B的作用是
【数据与解释】
(6)称量图3中反应前后烧杯和其中溶液的总质量,增重0.92g。计算草木灰中碳酸钾的质量分数为
a.烧杯中溶液与空气接触 b.固体含有其它钾盐 c.固体含有氯化钠
【反思与评价】
(7)我国秸秆产量巨大,可作为生物质发电的原料,还可利用其燃烧发电产生的草木灰提取碳酸钾,其优点有
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】同学们正在进行氢氧化钙与各种盐反应的探究实验。用A、B、C、D四支试管各取室温下等体积的氢氧化钙饱和溶液,再向A试管中滴加碳酸钠溶液、B试管中滴加氯化铜溶液、C试管中滴加氯化铵溶液、D试管中滴加氯化钠溶液,振荡。
(1)表达与交流:阳阳同学根据D试管中有没有看到现象,判断D试管无化学反应。你认为此判断的依据是否合理___________ (填”合理”或”不合理”),并解释其原因是___________ ;
(2)同学们对B试管中反应后得到的无色溶液,继续进行探究,他们选用两种不同类别的物质进行以下两个实验,请填写下列实验报告。
(1)表达与交流:阳阳同学根据D试管中有没有看到现象,判断D试管无化学反应。你认为此判断的依据是否合理
(2)同学们对B试管中反应后得到的无色溶液,继续进行探究,他们选用两种不同类别的物质进行以下两个实验,请填写下列实验报告。
| 实验内容 | 实验现象 | 实验结论 |
| 方案一:取少量滤液加入试管,向其中通入二氧化碳气体。 | ||
| 方案二:取少量滤液加入试管中,向其中 | 滤液中含有的两种溶质,分别是 |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】某玻璃粉末的主要成分有GeO2、Al2O3和SiO2等物质。下图为玻璃粉末的回收利用工艺流程:

已知:①GeO2是一种难溶于水的偏弱酸性的两性氧化物
②GeCl4的熔点为-49.5℃,沸点是84℃。
(1)焙烧时发生多个反应,写出GeO2与Na2CO3发生反应的化学方程式___________ 。
(2)为了提高含锗化合物的浸出率,除了延长浸取时间,还可采取的措施有__________ (答两条)。
(3)“滤渣”的主要成分是___________ (填化学式)。
(4)调节pH时,盐酸与硅的化合物反应的离子方程式为___________ 。
(5)“滤液”与7mol∙L−1盐酸反应生成四氯化锗,写出该反应的化学方程式_________ 。
(6)操作“X”的名称为___________ 。

已知:①GeO2是一种难溶于水的偏弱酸性的两性氧化物
②GeCl4的熔点为-49.5℃,沸点是84℃。
(1)焙烧时发生多个反应,写出GeO2与Na2CO3发生反应的化学方程式
(2)为了提高含锗化合物的浸出率,除了延长浸取时间,还可采取的措施有
(3)“滤渣”的主要成分是
(4)调节pH时,盐酸与硅的化合物反应的离子方程式为
(5)“滤液”与7mol∙L−1盐酸反应生成四氯化锗,写出该反应的化学方程式
(6)操作“X”的名称为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】20.6gNH4HCO3和NaHSO3的干燥粉状混合物,用加热分解的实验方法来测定NH4HCO3的质量分数。已知:NaHSO3加热时会产生SO2。根据下图所示的仪器和所盛试剂填空:
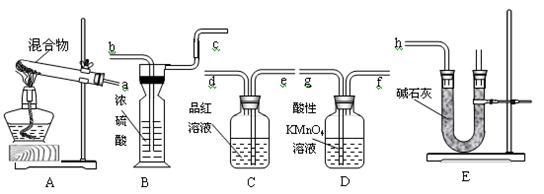
(1)按照气流由左→右的方向连接仪器的顺序(用a~h表示)为____________________ 。
(2)仪器B的名称为_________ ,E装置中放碱石灰的仪器名称为________ ,A和E装置中都用到的仪器名称为__________ 。
(3)D的作用是_______________________________________________________ 。
(4)C的作用是_________________________________ ;若C瓶中溶液颜色有变化,则测定结果可能会偏__________ 。
(5)B的作用是_____________________________________ 。

(1)按照气流由左→右的方向连接仪器的顺序(用a~h表示)为
(2)仪器B的名称为
(3)D的作用是
(4)C的作用是
(5)B的作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】为探究铜与浓硫酸的反应,甲、乙两同学分别设计了图1、图2所示装置,将足量铜和10mL18mol•L-1`的浓硫酸共热,直到无气体生成为止(假定反应前后试管中溶液的体积不变)。

(1)比较两实验装置,图2装置的优点是①__ ;②__ 。
(2)甲同学依据所学的化学知识认为还有一定量的H2SO4剩余,其理论依据是__ 。
(3)乙同学在实验结束后拆除图2装置时,在不打开橡胶塞的情况下,为使装置中的残留气体完全被吸收,应采取的操作是__ 。
(4)为测定铜与H2SO4停止反应时剩余H2SO4的浓度,甲同学进行了如下实验:将反应产生的气体(不含水蒸气)缓慢通过预先称量过的盛有__ 的干燥管,反应结束后再次称量,干燥管质量增加mg。则反应后的溶液中H2SO4的物质的量浓度为__ 。

(1)比较两实验装置,图2装置的优点是①
(2)甲同学依据所学的化学知识认为还有一定量的H2SO4剩余,其理论依据是
(3)乙同学在实验结束后拆除图2装置时,在不打开橡胶塞的情况下,为使装置中的残留气体完全被吸收,应采取的操作是
(4)为测定铜与H2SO4停止反应时剩余H2SO4的浓度,甲同学进行了如下实验:将反应产生的气体(不含水蒸气)缓慢通过预先称量过的盛有
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】下面所示是实验室制取SO2,并验证SO2的某些性质的装置图。试回答:
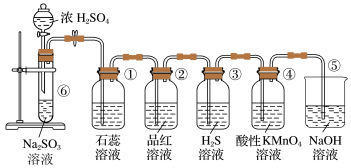
(1)②可证明SO2有___ 性;③可证明SO2有___ 性。
(2)④中的实验现象是__ ,证明SO2有___ 性。
(3)⑤的作用是___ 。

(1)②可证明SO2有
(2)④中的实验现象是
(3)⑤的作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】如图是实验室制取 并验证
并验证 的某些性质的装置,试回答下列问题:
的某些性质的装置,试回答下列问题:
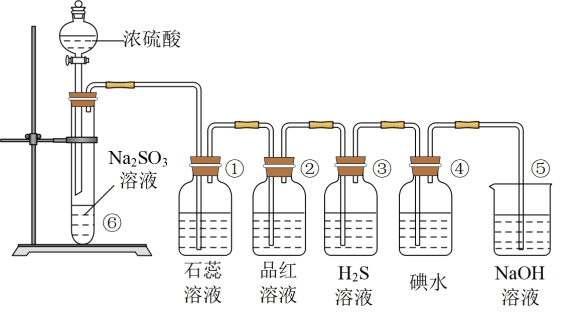
(1)在⑥中发生反应的化学方程式_______ 。
(2)①中的实验现象为_______ ,此实验证明 是
是_______ (填“酸性”或“碱性”)气体。
(3)②中的实验现象_______ ,证明 有
有_______ (填“漂白”“氧化”或“还原”)性。
(4)④中的实验现象是_______ ,证明 有
有_______ (填“漂白”“氧化”或“还原”)性。
(5)⑤的作用是_______ (用离子方程式表示)
 并验证
并验证 的某些性质的装置,试回答下列问题:
的某些性质的装置,试回答下列问题:
(1)在⑥中发生反应的化学方程式
(2)①中的实验现象为
 是
是(3)②中的实验现象
 有
有(4)④中的实验现象是
 有
有(5)⑤的作用是
您最近一年使用:0次

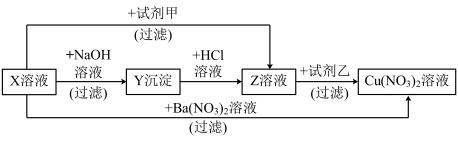
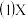 、Z的化学式分别为:X
、Z的化学式分别为:X 试剂甲为
试剂甲为

