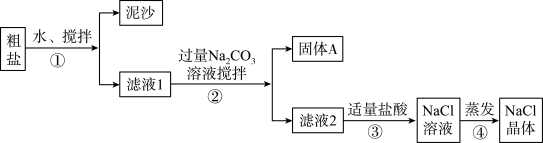
某同学用某种粗盐进行提纯实验,步骤见下图.
请回答:
(1)步骤①和②的操作名称是________ .
(2)步骤③判断加入盐酸“适量”的方法是_____ ;
步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止___________ ,当蒸发皿中有较多量固体出现时,应___________ ,用余热使水分蒸干.
(3)猜想和验证:
请写出猜想Ⅲ验证过程中发生的化学反应方程式_____

请回答:
(1)步骤①和②的操作名称是
(2)步骤③判断加入盐酸“适量”的方法是
步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止
(3)猜想和验证:
| 猜想 | 验证的方法 | 现象 | 结论 |
| 猜想Ⅰ:固体A中含 CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | 猜想Ⅰ成立 | |
| 猜想Ⅱ:固体A中含 BaCO3 | 取少量固体A于试管中,先滴入 | 有气泡放出,无白色沉淀 | |
| 猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水, | 猜想Ⅲ成立 |
请写出猜想Ⅲ验证过程中发生的化学反应方程式
更新时间:2019-10-15 09:14:32
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】下图是实验室加热氯酸钾和高锰酸钾的混合物制取和收集氧气的装置图:

⑴指出图中有标号的仪器名称:
a:_______ b:_______ c:_______ d:_______
⑵实验时应注意:
①实验前要检查装置的_______ 性,其方法是___________________ 。
②试管口要_________________ ,其目的是_________________ 。
③给试管加热时____________ 。
④停止加热时,先要____________ ,然后__________ 。

⑴指出图中有标号的仪器名称:
a:
⑵实验时应注意:
①实验前要检查装置的
②试管口要
③给试管加热时
④停止加热时,先要
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】今有下列六组仪器:①牛角管 ②锥形瓶 ③温度计 ④冷凝管 ⑤已组装固定好的铁架台、酒精灯和蒸馏烧瓶(垫有石棉网) ⑥带附件的铁架台。现要进行酒精(沸点为78.5℃)和水混合物的分离实验,试回答下列问题:
(1)按仪器的安装先后顺序排列以上提供的各组仪器(填序号):____ →____ →____ →____ →____ →_____ 。
(2)冷凝管的两端有大口和小口之分,靠近大口的小弯管用于___ 冷却水,靠近小口的小弯管用于___ 冷却水(填“引入”或“流出”)。
(3)蒸馏时,温度计水银球应位于____ 。
(4)在蒸馏烧瓶中注入液体混合物后,加几片碎瓷片的目的是___ 。
(1)按仪器的安装先后顺序排列以上提供的各组仪器(填序号):
(2)冷凝管的两端有大口和小口之分,靠近大口的小弯管用于
(3)蒸馏时,温度计水银球应位于
(4)在蒸馏烧瓶中注入液体混合物后,加几片碎瓷片的目的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】苯甲酸的提纯实验基本操作如下:①将粗苯甲酸1g加到100mL的烧杯中,再加入50mL蒸馏水,在石棉网上边搅拌边加热,使粗苯甲酸溶解;②全溶后再加入少量蒸馏水并搅拌;③然后,使用短颈玻璃漏斗趁热将溶液过滤到另一100mL烧杯中,将滤液静置,使其缓慢冷却结晶;④滤出晶体。
回答下列问题:
(1)请用6个字概括过滤的实验操作步骤:____________________________ ;
(2)步骤②的加入少量水的目的是 :
: ___________________________ ;
(3)步骤④滤出晶体还有少量杂质,为了进一步得到更纯的晶体还要进行的操作是______ ;
(4)温度越低苯甲酸的溶解度越小,为了得到更多的苯甲酸结晶体,是不是结晶时的温度越低越好?请用简明的语言说明。________________________________________________ 。
回答下列问题:
(1)请用6个字概括过滤的实验操作步骤:
(2)步骤②的加入少量水的目的是
 :
: (3)步骤④滤出晶体还有少量杂质,为了进一步得到更纯的晶体还要进行的操作是
(4)温度越低苯甲酸的溶解度越小,为了得到更多的苯甲酸结晶体,是不是结晶时的温度越低越好?请用简明的语言说明。
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】氢氧化铈是黄色难溶于水、可溶于酸的常用化学试剂。以氟碳铈矿(主要成分为 CeFCO3) 为原料提取氢氧化铈的工艺流程如图所示:

请回答下列问题:
(1)CeFCO3中 Ce 的化合价为_______ 。“酸浸” 时,为提高矿石的浸出率,下列措施可采取的是_______ (填标号)。
A.提高浸出温度 B.延长浸出时间 C.用 98%的硫酸
(2)氧化焙烧发生的反应方程式为_______ 。
(3)H2O2的作用是_______ 。
(4)HT 是一种难溶于水的有机溶剂,它能将 Ce3+从水溶液中萃取出来,该过程可表示为Ce3+(水层)+3HT(有机层)⇌CeT3(有机层)+3H+(水层) 。操作I 的名称是_______ ,操作 III 的步骤是_______ 。

请回答下列问题:
(1)CeFCO3中 Ce 的化合价为
A.提高浸出温度 B.延长浸出时间 C.用 98%的硫酸
(2)氧化焙烧发生的反应方程式为
(3)H2O2的作用是
(4)HT 是一种难溶于水的有机溶剂,它能将 Ce3+从水溶液中萃取出来,该过程可表示为Ce3+(水层)+3HT(有机层)⇌CeT3(有机层)+3H+(水层) 。操作I 的名称是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】蒸馏实验装置如下图所示:

(1)蒸馏实验操作可简记为隔网加热冷管倾,上缘下缘两相平;需加碎瓷防暴沸,热气冷水逆向行。其中“热气冷水逆向行”的含义是___________________________________ 。
(2)在蒸馏实验中,使用温度计的原因是________________________________________ 。
(3)温度计水银球的位置是________________________________________________ 。
(4)制取蒸馏水时可以不使用温度计的原因是______________________________________ 。

(1)蒸馏实验操作可简记为隔网加热冷管倾,上缘下缘两相平;需加碎瓷防暴沸,热气冷水逆向行。其中“热气冷水逆向行”的含义是
(2)在蒸馏实验中,使用温度计的原因是
(3)温度计水银球的位置是
(4)制取蒸馏水时可以不使用温度计的原因是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】实验室里需要纯净的NaCl溶液,但手边只有混有Na2SO4、NH4HCO3的NaCl。某学生设计了如图所示方案提取纯净的NaCl溶液。(已知:NH4HCO3 NH3↑+CO2↑+H2O)
NH3↑+CO2↑+H2O)

如果此方案正确,那么:
(1)操作①可选择________ 仪器。
(2)操作②为什么不用硝酸钡溶液,其理由是___________________________ 。
(3)进行操作②后,如何判断 已除尽,方法是
已除尽,方法是_____________________ 。
(4)操作③的目的是_______________________________________________ ,为什么不先过滤后加碳酸钠溶液?理由是_________________________ 。
(5)操作④的目的是______________________________________________ 。
 NH3↑+CO2↑+H2O)
NH3↑+CO2↑+H2O)
如果此方案正确,那么:
(1)操作①可选择
(2)操作②为什么不用硝酸钡溶液,其理由是
(3)进行操作②后,如何判断
 已除尽,方法是
已除尽,方法是(4)操作③的目的是
(5)操作④的目的是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
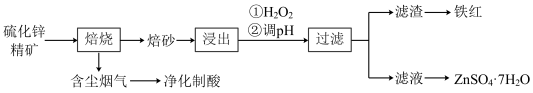
【推荐1】某硫化锌精矿的主要成分为ZnS(还含一定量FeS),以其为原料制备七水合硫酸锌(ZnSO4·7H2O)与铁红的工艺流程如图所示:
①焙砂的成分是ZnO和FeO
②相关金属离子形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)“焙烧”时为了加快反应速率,可以采取的措施是_______ ,其中ZnS发生反应的化学方程式为_______ 。“净化制酸”所得的产品可用于后续的_______ 操作。
(2)“浸出”后加入H2O2发生反应的离子方程式为_______ ,调pH的目的是将Fe3+完全转化为Fe(OH)3沉淀并与Zn2+分离,为达到该目的,调节pH的范围是_______ 。
(3)“滤渣”的化学式是_______ ,由“滤液”得到ZnSO4·7H2O的操作是蒸发浓缩、_______ 、过滤洗涤。
①焙砂的成分是ZnO和FeO
②相关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 |
(1)“焙烧”时为了加快反应速率,可以采取的措施是
(2)“浸出”后加入H2O2发生反应的离子方程式为
(3)“滤渣”的化学式是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】已知某工业废水中含有大量FeSO4,较多的Cu2+,以及部分污泥,通过下列流程可从该废水中回收FeSO4·7H2O晶体及金属Cu.
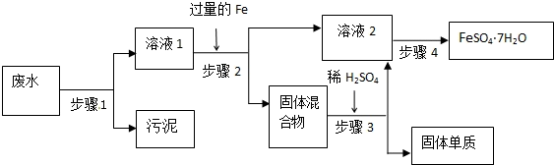
(1)步骤1的主要操作是_____ ,(填操作名称)需用到的玻璃仪器除烧杯外有_____
(2)步骤2中发生反应的离子方程式为_____ .
(3)步骤3中发生反应的化学方程式为______ .
(4)步骤4中涉及的操作是:蒸发浓缩、_____ 、过滤、洗涤、烘干。

(1)步骤1的主要操作是
(2)步骤2中发生反应的离子方程式为
(3)步骤3中发生反应的化学方程式为
(4)步骤4中涉及的操作是:蒸发浓缩、
您最近一年使用:0次




