O2和O3是氧元素的两种单质,根据其分子式完成下列各题:
(1)等质量的O2和O3所含分子个数比为____ ,原子个数比为_____ ,分子的物质的量之比为____ 。
(2)等温等压下,等体积的O2和O3所含分子个数比为___ ,原子个数比为_____ ,质量比为___ 。
(3)设NA为阿伏加 德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是__ (用含NA的式子表示)。
(4)配制100 mL 1 mol/L的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84 g·mL-1,质量分数为98%)的体积为____ mL。
(1)等质量的O2和O3所含分子个数比为
(2)等温等压下,等体积的O2和O3所含分子个数比为
(3)设NA为阿伏加 德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是
(4)配制100 mL 1 mol/L的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84 g·mL-1,质量分数为98%)的体积为
更新时间:2019-10-16 13:56:24
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】(1)在标准状况下①6.72L CH4②3.01×1023个HCl分子③ 13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达正确的是_____
a.体积②>③>①>④ b.密度②>③>④>①
c.质量②>③>①>④ d.氢原子个数①>③>④>②
(2)在标准状况下,CO和CO2的混合气体共39.2 L,质量为61 g。则其中CO2为________ mol, CO占总体积的______ (保留一位小数),混合气体的摩尔质量为_______ (保留一位小数)。
(3)某混合气体中各气体的质量分数为:O232%,N228%,CO222%,CH416%,H22%,则此混合气体的平均摩尔质量为______ (保留两位小数)。
a.体积②>③>①>④ b.密度②>③>④>①
c.质量②>③>①>④ d.氢原子个数①>③>④>②
(2)在标准状况下,CO和CO2的混合气体共39.2 L,质量为61 g。则其中CO2为
(3)某混合气体中各气体的质量分数为:O232%,N228%,CO222%,CH416%,H22%,则此混合气体的平均摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某状况下,2g二氧化碳气体的体积是 1120 mL,2g A 气体的体积是 770 mL,A的摩尔质量是__________ 。 某金属氯化物 MCl240.5 g含 0.6 mol Cl-,则该氯化物的摩尔质量为__________ ,金属M的相对原子质量为__________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】填写下列空白:
(1)______  中含有的氧原子数与
中含有的氧原子数与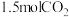 中含有的氧原子数相等。
中含有的氧原子数相等。
(2)将等物质的量的 和
和 混合,混合气体中
混合,混合气体中 与
与 的质量比为
的质量比为______ ;要使 与
与 含相同数目的H原子,则
含相同数目的H原子,则 和
和 的物质的量之比为
的物质的量之比为______ 。
(3)某结晶水合物的化学式为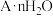 ,A的相对分子质量为M。如将
,A的相对分子质量为M。如将 该结晶水合物加热至结晶水全部失去,剩余的残渣为
该结晶水合物加热至结晶水全部失去,剩余的残渣为 ,则
,则
______ 。
(5)已知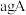 和
和 恰好完全反应生成
恰好完全反应生成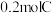 和
和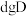 ,则C的摩尔质量为
,则C的摩尔质量为_____ 。
(1)
 中含有的氧原子数与
中含有的氧原子数与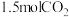 中含有的氧原子数相等。
中含有的氧原子数相等。(2)将等物质的量的
 和
和 混合,混合气体中
混合,混合气体中 与
与 的质量比为
的质量比为 与
与 含相同数目的H原子,则
含相同数目的H原子,则 和
和 的物质的量之比为
的物质的量之比为(3)某结晶水合物的化学式为
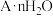 ,A的相对分子质量为M。如将
,A的相对分子质量为M。如将 该结晶水合物加热至结晶水全部失去,剩余的残渣为
该结晶水合物加热至结晶水全部失去,剩余的残渣为 ,则
,则
(5)已知
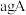 和
和 恰好完全反应生成
恰好完全反应生成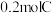 和
和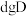 ,则C的摩尔质量为
,则C的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】向500mL氢氧化钠溶液中投入10.8g铝,二者恰好完全反应,计算回答下列问题:
(1)参加反应的铝的物质的量是_______ mol。
(2)分别求氧氧化钠溶液的物质的量浓度和在标准状况下反应生成氢气的体积_____ (请写出计算过程)。
(1)参加反应的铝的物质的量是
(2)分别求氧氧化钠溶液的物质的量浓度和在标准状况下反应生成氢气的体积
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】将一定量的氧化铜加入到10.0mL2.50mol/L的稀硫酸中,待其完全溶解后,再向蓝色溶液中加入2.06g铁粉,经搅拌、过滤、洗涤、干燥等操作,最后得到固体的质量为1.94g。通过数据的比较说明干燥后得到的固体是什么物质?____ 求原氧化铜的质量___ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】同温同压下,氧气(O2)和臭氧(O3)的体积比是3:2,则它们的物质的量之比是______ ,原子个数之比是______ ,一定条件下氧气转化为臭氧的反应______ 氧化还原反应(填“是”或“不是”).
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】根据要求回答下列问题。
(1)相同质量的SO2气体和SO3气体,其分子数之比为_____ ,氧原子数之比为_____ ,相同条件下(同温同压)的体积之比为_____ ,密度之比为_____ 。
(2)SO2与O2的混合气体中,氧元素的质量分数为70%,则SO2与O2的物质的量之比是_____ ,这种混合气体的密度是同温同压下氧气密度的_____ 倍。
(3)用2.4 mol·L-1的H2SO4溶液配制100 mL浓度为0.2 mol·L-1的稀硫酸,需量取2.4 mol·L-1的H2SO4溶液的体积是_____ mL。
(4)试分析下列操作对所配溶液的浓度有何影响(填“偏高”“偏低”或“无影响”)。
①未洗涤烧杯和玻璃棒,使所配溶液浓度_____ ;
②定容时俯视刻度线,使所配溶液浓度_____ ;
③摇匀后,发现液面低于刻度线,又滴加蒸馏水,使所配溶液浓度_____ 。
(1)相同质量的SO2气体和SO3气体,其分子数之比为
(2)SO2与O2的混合气体中,氧元素的质量分数为70%,则SO2与O2的物质的量之比是
(3)用2.4 mol·L-1的H2SO4溶液配制100 mL浓度为0.2 mol·L-1的稀硫酸,需量取2.4 mol·L-1的H2SO4溶液的体积是
(4)试分析下列操作对所配溶液的浓度有何影响(填“偏高”“偏低”或“无影响”)。
①未洗涤烧杯和玻璃棒,使所配溶液浓度
②定容时俯视刻度线,使所配溶液浓度
③摇匀后,发现液面低于刻度线,又滴加蒸馏水,使所配溶液浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】请根据物质的量相关计算填空
(1)19.6 g 硫酸是_____ mol H2SO4 ,1.7 gNH3 在同温同压下与_____ g H2S 气体含有的氢原子数相同。
(2)在标准状况下,1.6 g 某气态氧化物 RO2 体积为 0.56L,该气体的物质的量是_____ ,R 的相 对原子量为_____ 。
(3)已知 Wg 气体 A 含有 a 个分子,那么在标准状况下,bg 气体 A 所占的体积是_____ L (其中阿 伏加德罗常数用 NA 表示)
(4)标准状况下,密度为 0.75g/L 的 NH3 与 CH4 组成的混合气体中,NH3 的体积分数_______________ , 混合气体的平均摩尔质量为_____ , 该气体对氢气的相对密度为__________________ 。
(1)19.6 g 硫酸是
(2)在标准状况下,1.6 g 某气态氧化物 RO2 体积为 0.56L,该气体的物质的量是
(3)已知 Wg 气体 A 含有 a 个分子,那么在标准状况下,bg 气体 A 所占的体积是
(4)标准状况下,密度为 0.75g/L 的 NH3 与 CH4 组成的混合气体中,NH3 的体积分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)实验室常用浓硫酸的质量分数为98%,密度为1.80 g·mL−1,其物质的量浓度是_______ 。
(2)标准状况下,将V L A气体(摩尔质量为M g/mol)完全溶于0.1 L水(密度1 g/cm3)中,所得溶液的密度为d g/mL,则此溶液的物质的量浓度为_______ mol/L。
A.Vd/(MV+2240) B.1000Vd/(MV+2240) C.1000VdM/(MV+2240) D.MV/22.4(V+0.1)d
(2)标准状况下,将V L A气体(摩尔质量为M g/mol)完全溶于0.1 L水(密度1 g/cm3)中,所得溶液的密度为d g/mL,则此溶液的物质的量浓度为
A.Vd/(MV+2240) B.1000Vd/(MV+2240) C.1000VdM/(MV+2240) D.MV/22.4(V+0.1)d
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】欲使100g 9.32 % 的NaOH溶液溶质的质量分数增大到20%
(1)需往溶液中加入多少克金属钠?
(2)若20%NaOH溶液的密度为1.066 g/cm3,计算物质的量浓度。
(1)需往溶液中加入多少克金属钠?
(2)若20%NaOH溶液的密度为1.066 g/cm3,计算物质的量浓度。
您最近一年使用:0次



