通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能.下列是一些化学键的键能.根据键能数据估算下列反应的反应热,CH4(g)+4F2(g)=CF4(g)+4HF(g)的△H为
化学键 | C-H | C-F | H-F | F-F |
键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A.﹣1940 kJ/mol | B.+1940 kJ/mol | C.﹣485 kJ/mol | D.+485 kJ/mol |
更新时间:2019-10-20 12:18:02
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知:2H2(g) +O2(g)=2H2O(g) ΔH =-483.6 kJ·mol−1
下列说法不正确 的是

下列说法
| A.该反应可作为氢氧燃料电池的反应原理 |
| B.破坏1 mol H-O键需要的能量是463.4 kJ |
| C.H2的燃烧热ΔH<-241.8 kJ·mol−1 |
| D.H2(g)中的H-H键比H2O(g)中的H-O键牢固 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列与化学反应能量变化相关的叙述正确的是
A.当 时,表示该反应为吸热反应 时,表示该反应为吸热反应 |
B.相同条件下, 氢原子所具有的能量小于 氢原子所具有的能量小于 氢分子所具有的能量 氢分子所具有的能量 |
| C.应用盖斯定律,可以计算某些难以直接测量的反应焓变 |
D.同温同压下, 在光照和点燃条件的 在光照和点燃条件的 不同 不同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】乙烯与氢气在Ni催化作用下加热可发生加成反应得到乙烷:C2H4(g)+H2(g)=C2H6(g) △H=-137.0 kJ/mol,已知: H-H键的键能为436 kJ/mol,C-H键的键能为413kJ/mol,则碳碳双键的键能与碳碳单键的键能之差为
| A.160 kJ/mol | B.506 kJ/mol |
| C.255 kJ/mol | D.253 kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下图是在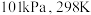 下,有关水分子断键过程的能量变化:下列说法正确的是
下,有关水分子断键过程的能量变化:下列说法正确的是

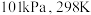 下,有关水分子断键过程的能量变化:下列说法正确的是
下,有关水分子断键过程的能量变化:下列说法正确的是
A. ,且 ,且 | B. 是 是 的键能 的键能 |
C.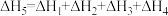 | D.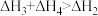 |
您最近一年使用:0次

 、
、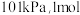 液态水汽化时需要吸收
液态水汽化时需要吸收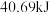 的热量,则
的热量,则 的
的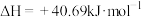
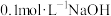 溶液反应的热化学方程式为:
溶液反应的热化学方程式为: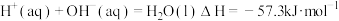

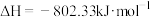 ,则
,则 的燃烧热为
的燃烧热为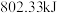


 ,则
,则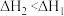
 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是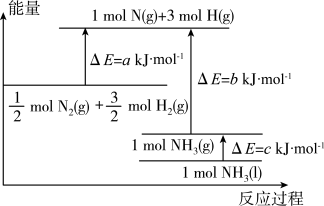
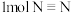 键和
键和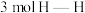 键,吸收
键,吸收 热量
热量
 与
与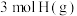 形成
形成 ,放出
,放出 热量
热量

