根据 A-I 在周期表中的位置,用元素符号或化学式回答下列问题。
(1)表中元素,化学性质最不活泼的是_____ ,只有负价而无正价的是_____ ,氧化性最强的单质是____ ;
(2)最高价氧化物的水化物碱性最强的是_____ ,酸性最强的是_____ ,呈两性的是_____ ;
(3)A 分别与 D、E、F、G、H 形成的化合物中,最稳定的是_____ ;
(4)在 B、C、D、E、F、G、H 中,原子半径最大的是_____ ;
(5)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外 M 电子层与 K 电子层上的电子数相等,甲、乙两元素相比较,金属性较强的是_______ 可以验证该结论的实验是_ 。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(1)表中元素,化学性质最不活泼的是
(2)最高价氧化物的水化物碱性最强的是
(3)A 分别与 D、E、F、G、H 形成的化合物中,最稳定的是
(4)在 B、C、D、E、F、G、H 中,原子半径最大的是
(5)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外 M 电子层与 K 电子层上的电子数相等,甲、乙两元素相比较,金属性较强的是
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
更新时间:2019-10-25 14:10:29
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】下图表示各物质之间的转化关系。已知:
Ⅰ. A是无色液体,L是不溶于稀硝酸的白色沉淀,E、F、H、J、X、Y、Z是气体;
Ⅱ. G、X、Y、Z是单质,其他是化合物,其中Y呈黄绿色、H呈红棕色,E和F都极易溶解于水,二者相遇会有白烟生成;
Ⅲ. B和C都是由一种金属与一种非金属元素组成的化合物,其中非金属元素相同且质量分数B中是28%,组成B的金属元素原子核外的K层和M层电子数相同。
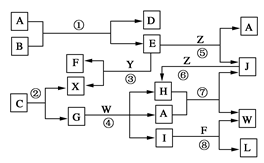
请按要求填空:
(1)写出下列物质的电子式:A______________ ,X______________ 。
(2)上述反应中属于工业上制取硝酸的反应有(填写反应代号)_______________ 。
(3)写出下列物质的化学式:B______________ ,C______________ 。
(4)反应④的化学方程式为______________________ 。
(5)保持容器的温度和体积不变,在反应③刚好完全反应时,反应前后容器的压强之比为__________ 。
Ⅰ. A是无色液体,L是不溶于稀硝酸的白色沉淀,E、F、H、J、X、Y、Z是气体;
Ⅱ. G、X、Y、Z是单质,其他是化合物,其中Y呈黄绿色、H呈红棕色,E和F都极易溶解于水,二者相遇会有白烟生成;
Ⅲ. B和C都是由一种金属与一种非金属元素组成的化合物,其中非金属元素相同且质量分数B中是28%,组成B的金属元素原子核外的K层和M层电子数相同。

请按要求填空:
(1)写出下列物质的电子式:A
(2)上述反应中属于工业上制取硝酸的反应有(填写反应代号)
(3)写出下列物质的化学式:B
(4)反应④的化学方程式为
(5)保持容器的温度和体积不变,在反应③刚好完全反应时,反应前后容器的压强之比为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】下表列出了A~R 9种元素在周期表中的位置:

(1)F元素的名称为__________ ;画出B的原子结构示意图:__________________ 。
(2)这9种元素中,化学性质最不活泼的是_______ ;既具有非金属元素的某些性质,又可能具有金属元素的某些性质的元素是___________ 。(填元素符号)
(3)A、D、E三种元素的最高价氧化物形成的晶体中属于分子晶体的是______ ,A、B两元素的氧化物中熔点较高的是________________ ,C、D、F形成的氢化物分子中共价键的极性由强到弱的顺序为____________________________ 。(填化学式)
(4)工业上用D的一种单质为原料生产E单质粗品的化学方程式为___________________ 。
(5)G和H的原子序数相差___________ 。(填数字)
(6)写出一个能证明G比H活泼的化学方程式______________________________________ 。

(1)F元素的名称为
(2)这9种元素中,化学性质最不活泼的是
(3)A、D、E三种元素的最高价氧化物形成的晶体中属于分子晶体的是
(4)工业上用D的一种单质为原料生产E单质粗品的化学方程式为
(5)G和H的原子序数相差
(6)写出一个能证明G比H活泼的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】中学常见物质A~L的转化关系如下图:(无关产物已略去)

①A、B、H均为单质,A、B有金属光泽,A可以在常温下溶于L的浓溶液,H为黄色固体,向由A、B粉未组成的均匀混合物中加入无色纯液体C(少量)后,产生大量紫色蒸气。
②D、E、F、I、L都是无色溶液,G是无色气体。
③K是一种白色沉淀,J是一种黄色沉淀,将G通入E后可以产生一种黑色沉淀和L。
(1)写出下列物质的名称:B________ H_________
(2)写出试题中出现的几种沉淀的化学式:黄色沉淀_______ ;黑色沉淀_________ 。
(3)写出B和G反应的离子方程式__________________________ 。
(4)写出电解E溶液的电极反应式: 阳极:_______________ ;阴极:________________ 。

①A、B、H均为单质,A、B有金属光泽,A可以在常温下溶于L的浓溶液,H为黄色固体,向由A、B粉未组成的均匀混合物中加入无色纯液体C(少量)后,产生大量紫色蒸气。
②D、E、F、I、L都是无色溶液,G是无色气体。
③K是一种白色沉淀,J是一种黄色沉淀,将G通入E后可以产生一种黑色沉淀和L。
(1)写出下列物质的名称:B
(2)写出试题中出现的几种沉淀的化学式:黄色沉淀
(3)写出B和G反应的离子方程式
(4)写出电解E溶液的电极反应式: 阳极:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】五种短周期元素A、B、C、D、E的原子序数依次增大,其中只有C为金属元素。A和C同主族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是__________ ,非金属性最强的是__________ (填元素符号);
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是__________ (用化学式表示);
(3)D在周期表的位置为__________
(4)A和B形成的化合物与A和E形成的化合物反应,产物的化学式为__________ ,该化合物溶于水,显__________ 性(填“酸”、“碱”、“中”)原因是__________ (用离子方程式表示);
(5)D和E可形成一种所有原子都满足8电子结构的化合物,其化学式为__________ 。
(1)五种元素中,原子半径最大的是
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是
(3)D在周期表的位置为
(4)A和B形成的化合物与A和E形成的化合物反应,产物的化学式为
(5)D和E可形成一种所有原子都满足8电子结构的化合物,其化学式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】(I)俄美科学家联合小组宣布合成出114号元素(Fl)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中的位置为:_______ ,属于_______ 元素(填“金属”或“非金属”)。
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
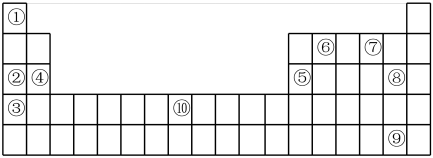
(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是_______ (填化学式)。
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为_______ ;
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为_______ ;
(5)元素⑩的名称为_______ ,其单质与⑧的单质反应的化学方程式为_______ ;
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是_______
A.L2+、R2-的核外电子数相等
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物具有两性
D.简单氢化物的沸点为HnT>HnR
E.T与R可形成的化合物TR2、TR3
F.Q与M的单质均能与盐酸、NaOH溶液反应放出氢气
(1)该元素在周期表中的位置为:
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:

(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为
(5)元素⑩的名称为
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物具有两性
D.简单氢化物的沸点为HnT>HnR
E.T与R可形成的化合物TR2、TR3
F.Q与M的单质均能与盐酸、NaOH溶液反应放出氢气
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】锰(25Mn)及其化合物是目前前沿科学研究的热点。按要求回答下列问题。
(1)锰元素在元素周期表中的位置是___________ 。
(2)某晶体锰的面心立方晶胞如图所示。
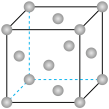
①该晶胞中含Mn原子的个数为___________ ;
②晶体锰中每个Mn原子距离最近的Mn原子数目为___________ 。
③设该晶胞参数棱长为 。则晶体锰的密度为
。则晶体锰的密度为___________  (列算式)
(列算式)
(3)锰的冶炼有多种方法,其中以某锰矿(主要成分为 ,主要杂质有
,主要杂质有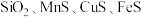 )为原料,设计如下流程可制得金属Mn。
)为原料,设计如下流程可制得金属Mn。
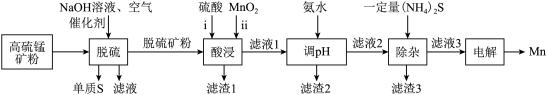
已知:金属硫化物的溶度积常数如下表。
①脱硫步骤:硫化物均转化为单质S,其反应中的氧化剂为___________ ; 能被部分反应而得到的产物为
能被部分反应而得到的产物为___________ 。
②酸浸步骤:ⅰ反应后的溶液中含 ,写出ⅱ反应的离子方程式:
,写出ⅱ反应的离子方程式:___________ ;滤渣1含有的物质有___________ 。若未经脱硫直接酸浸,不利的方面是___________ 。
③调 的目的为去除铁元素,则产生滤渣2的离子方程式:
的目的为去除铁元素,则产生滤渣2的离子方程式:___________ ;
④除杂步骤:滤渣3中主要有___________ 。
⑤电解步骤:惰性阳极产生 的反应式为
的反应式为___________ 。
(1)锰元素在元素周期表中的位置是
(2)某晶体锰的面心立方晶胞如图所示。

①该晶胞中含Mn原子的个数为
②晶体锰中每个Mn原子距离最近的Mn原子数目为
③设该晶胞参数棱长为
 。则晶体锰的密度为
。则晶体锰的密度为 (列算式)
(列算式)(3)锰的冶炼有多种方法,其中以某锰矿(主要成分为
 ,主要杂质有
,主要杂质有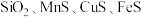 )为原料,设计如下流程可制得金属Mn。
)为原料,设计如下流程可制得金属Mn。
已知:金属硫化物的溶度积常数如下表。
| 物质 | CuS | MnS | FeS |
 |  | 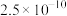 |  |
 能被部分反应而得到的产物为
能被部分反应而得到的产物为②酸浸步骤:ⅰ反应后的溶液中含
 ,写出ⅱ反应的离子方程式:
,写出ⅱ反应的离子方程式:③调
 的目的为去除铁元素,则产生滤渣2的离子方程式:
的目的为去除铁元素,则产生滤渣2的离子方程式:④除杂步骤:滤渣3中主要有
⑤电解步骤:惰性阳极产生
 的反应式为
的反应式为
您最近一年使用:0次



