锰(25Mn)及其化合物是目前前沿科学研究的热点。按要求回答下列问题。
(1)锰元素在元素周期表中的位置是___________ 。
(2)某晶体锰的面心立方晶胞如图所示。
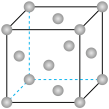
①该晶胞中含Mn原子的个数为___________ ;
②晶体锰中每个Mn原子距离最近的Mn原子数目为___________ 。
③设该晶胞参数棱长为 。则晶体锰的密度为
。则晶体锰的密度为___________  (列算式)
(列算式)
(3)锰的冶炼有多种方法,其中以某锰矿(主要成分为 ,主要杂质有
,主要杂质有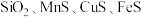 )为原料,设计如下流程可制得金属Mn。
)为原料,设计如下流程可制得金属Mn。
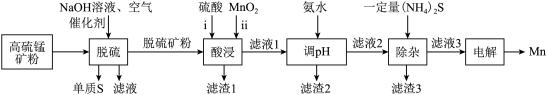
已知:金属硫化物的溶度积常数如下表。
①脱硫步骤:硫化物均转化为单质S,其反应中的氧化剂为___________ ; 能被部分反应而得到的产物为
能被部分反应而得到的产物为___________ 。
②酸浸步骤:ⅰ反应后的溶液中含 ,写出ⅱ反应的离子方程式:
,写出ⅱ反应的离子方程式:___________ ;滤渣1含有的物质有___________ 。若未经脱硫直接酸浸,不利的方面是___________ 。
③调 的目的为去除铁元素,则产生滤渣2的离子方程式:
的目的为去除铁元素,则产生滤渣2的离子方程式:___________ ;
④除杂步骤:滤渣3中主要有___________ 。
⑤电解步骤:惰性阳极产生 的反应式为
的反应式为___________ 。
(1)锰元素在元素周期表中的位置是
(2)某晶体锰的面心立方晶胞如图所示。

①该晶胞中含Mn原子的个数为
②晶体锰中每个Mn原子距离最近的Mn原子数目为
③设该晶胞参数棱长为
 。则晶体锰的密度为
。则晶体锰的密度为 (列算式)
(列算式)(3)锰的冶炼有多种方法,其中以某锰矿(主要成分为
 ,主要杂质有
,主要杂质有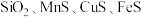 )为原料,设计如下流程可制得金属Mn。
)为原料,设计如下流程可制得金属Mn。
已知:金属硫化物的溶度积常数如下表。
| 物质 | CuS | MnS | FeS |
 |  | 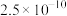 |  |
 能被部分反应而得到的产物为
能被部分反应而得到的产物为②酸浸步骤:ⅰ反应后的溶液中含
 ,写出ⅱ反应的离子方程式:
,写出ⅱ反应的离子方程式:③调
 的目的为去除铁元素,则产生滤渣2的离子方程式:
的目的为去除铁元素,则产生滤渣2的离子方程式:④除杂步骤:滤渣3中主要有
⑤电解步骤:惰性阳极产生
 的反应式为
的反应式为
更新时间:2023-04-26 22:58:49
|
相似题推荐
【推荐1】氮及其化合物在生产生活中有广泛应用.
 已知:CO可将部分氮的氧化物还原为
已知:CO可将部分氮的氧化物还原为 .
.
反应Ⅰ:
反应Ⅱ: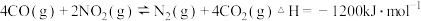
写出CO将 还原为NO的热化学方程式
还原为NO的热化学方程式 ______ .
 在密闭容器中充入5mol CO和4mol NO,发生上述反应I,图1为平衡时NO的体积分数与温度、压强的关系.
在密闭容器中充入5mol CO和4mol NO,发生上述反应I,图1为平衡时NO的体积分数与温度、压强的关系.
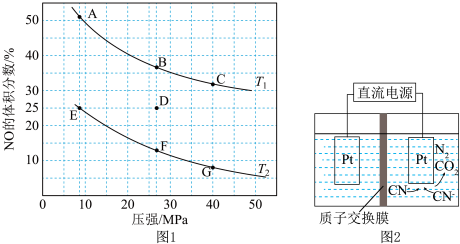
回答下列问题:
 温度:
温度:
______ 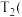 填“
填“ ”或“
”或“ ”
” .
.
 某温度下,在体积为2L的密闭容器中,反应进行10分钟放出热量373kJ,用CO的浓度变化表示的平均反应速率
某温度下,在体积为2L的密闭容器中,反应进行10分钟放出热量373kJ,用CO的浓度变化表示的平均反应速率
______ .
 某温度下,反应达到平衡状态D点时,容器体积为2L,此时的平衡常数
某温度下,反应达到平衡状态D点时,容器体积为2L,此时的平衡常数
______  结果精确到
结果精确到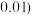 ;若在D点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中
;若在D点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中 点中的
点中的 ______ 点
 某温度时,亚硝酸银
某温度时,亚硝酸银 的
的  、
、 的
的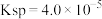 ,当向含
,当向含 、
、 混合溶液中加入
混合溶液中加入 溶液至
溶液至 恰好完全沉淀
恰好完全沉淀 即
即 浓度等于
浓度等于
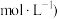 时,
时,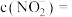
______ .
 如图2,在酸性条件下,电解水中
如图2,在酸性条件下,电解水中 可转化为
可转化为 和
和 ,请写出阳极的电极反应式
,请写出阳极的电极反应式 ______ .
 已知:CO可将部分氮的氧化物还原为
已知:CO可将部分氮的氧化物还原为 .
. 反应Ⅰ:

反应Ⅱ:
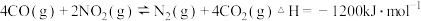
写出CO将
 还原为NO的热化学方程式
还原为NO的热化学方程式  在密闭容器中充入5mol CO和4mol NO,发生上述反应I,图1为平衡时NO的体积分数与温度、压强的关系.
在密闭容器中充入5mol CO和4mol NO,发生上述反应I,图1为平衡时NO的体积分数与温度、压强的关系. 
回答下列问题:
 温度:
温度:
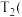 填“
填“ ”或“
”或“ ”
” .
. 某温度下,在体积为2L的密闭容器中,反应进行10分钟放出热量373kJ,用CO的浓度变化表示的平均反应速率
某温度下,在体积为2L的密闭容器中,反应进行10分钟放出热量373kJ,用CO的浓度变化表示的平均反应速率
 某温度下,反应达到平衡状态D点时,容器体积为2L,此时的平衡常数
某温度下,反应达到平衡状态D点时,容器体积为2L,此时的平衡常数
 结果精确到
结果精确到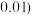 ;若在D点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中
;若在D点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中 点中的
点中的  某温度时,亚硝酸银
某温度时,亚硝酸银 的
的  、
、 的
的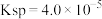 ,当向含
,当向含 、
、 混合溶液中加入
混合溶液中加入 溶液至
溶液至 恰好完全沉淀
恰好完全沉淀 即
即 浓度等于
浓度等于
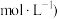 时,
时,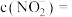
 如图2,在酸性条件下,电解水中
如图2,在酸性条件下,电解水中 可转化为
可转化为 和
和 ,请写出阳极的电极反应式
,请写出阳极的电极反应式
您最近一年使用:0次
【推荐2】溶解硝态氮( 、
、 采用等)是水体物质,可多种方法将其去除。
采用等)是水体物质,可多种方法将其去除。
(1)有效反硝化作用下,有效( )将酸性废水中的
)将酸性废水中的 、
、 除去,同时产生了无污染的气体。
除去,同时产生了无污染的气体。 反应的离子方程式为
反应的离子方程式为_______ 。
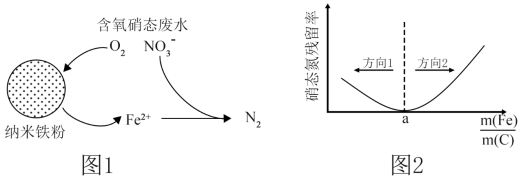
(2)纳米铁粉可用于排放废水中的硝态氮 表示),反应如图1所示。
表示),反应如图1所示。
①有研究发现,在铁粉总量一定的条件下,水中的溶解氧过多不利于硝态氮去除。其原因是_______ 。
②利用纳米铁粉与活性炭可提升硝态废水中炭硝态的除害效果。控制铁粉与活性炭态反应的总质量,一定时间不同,测得中氮态氮排放率与中氮硝态氮氧化物 的关系如图2所示,
的关系如图2所示, 过大和过小都会导致硝态氮残留率上升,但方向1上升幅度小于方向2。硝态氮残留率呈现如此变化的原因是
过大和过小都会导致硝态氮残留率上升,但方向1上升幅度小于方向2。硝态氮残留率呈现如此变化的原因是_______ 。
(3)用含为(主要是化合价) 、
、 )溶液作吸收液处理烟气中氮氧化物时,
)溶液作吸收液处理烟气中氮氧化物时, 被打包
被打包 。用电解法可将处理烟气后溶液中的
。用电解法可将处理烟气后溶液中的 变成无毒物质,同时使吸收液再生。
变成无毒物质,同时使吸收液再生。
①写出电解时阴极的电极反应式:_______ 。
②若完全电解后阴极生成1mol还原产物,阳极生成气体在标准状况下体积是_______ 。
 、
、 采用等)是水体物质,可多种方法将其去除。
采用等)是水体物质,可多种方法将其去除。(1)有效反硝化作用下,有效(
 )将酸性废水中的
)将酸性废水中的 、
、 除去,同时产生了无污染的气体。
除去,同时产生了无污染的气体。 反应的离子方程式为
反应的离子方程式为(2)纳米铁粉可用于排放废水中的硝态氮
 表示),反应如图1所示。
表示),反应如图1所示。①有研究发现,在铁粉总量一定的条件下,水中的溶解氧过多不利于硝态氮去除。其原因是
②利用纳米铁粉与活性炭可提升硝态废水中炭硝态的除害效果。控制铁粉与活性炭态反应的总质量,一定时间不同,测得中氮态氮排放率与中氮硝态氮氧化物
 的关系如图2所示,
的关系如图2所示, 过大和过小都会导致硝态氮残留率上升,但方向1上升幅度小于方向2。硝态氮残留率呈现如此变化的原因是
过大和过小都会导致硝态氮残留率上升,但方向1上升幅度小于方向2。硝态氮残留率呈现如此变化的原因是
(3)用含为(主要是化合价)
 、
、 )溶液作吸收液处理烟气中氮氧化物时,
)溶液作吸收液处理烟气中氮氧化物时, 被打包
被打包 。用电解法可将处理烟气后溶液中的
。用电解法可将处理烟气后溶液中的 变成无毒物质,同时使吸收液再生。
变成无毒物质,同时使吸收液再生。①写出电解时阴极的电极反应式:
②若完全电解后阴极生成1mol还原产物,阳极生成气体在标准状况下体积是
您最近一年使用:0次
【推荐3】研究催化去除汽车尾气、工业烟气中的氮及硫的化化物是环境保护、促进社会可持续发展的重要课题。
(1)汽车尾气主要含CO2、N2、CO、SO2、NOx等。
①用Na2CO3溶液能吸收SO2的原因是_______ 。
②汽车尾气中形成硝酸型酸雨的物质是_______ 。
(2)NOx储存还原技术可有效降低柴油发动机在空气过量条件下NOx的排放。如下图所示NOx的储存和还原在不同时段交替进行,通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。
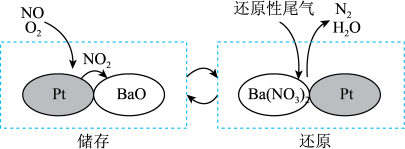
①储存NOx的物质是_______ (填写化学式)。
②与Ba(NO3)2反应生成1molN2需要还原性尾气H2_______ mol。
(3)生物法脱H2S的原理为:
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 2Fe2(S04)3+2H2O
2Fe2(S04)3+2H2O
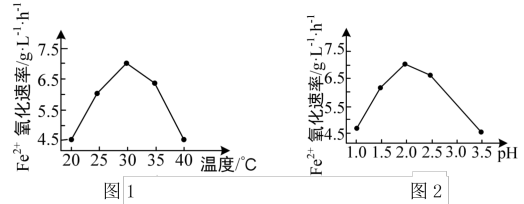
①硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是_______ 。
②由图1和图2判断使用硫杆菌的最佳条件为_______ 。
(4)太阳能光电催化—化学耦合分解H2S的装置如图所示。
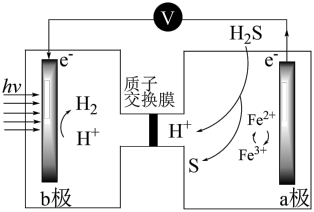
该太阳能光电催化—化学耦合分解H2S的过程可描述为_______ 。
(1)汽车尾气主要含CO2、N2、CO、SO2、NOx等。
①用Na2CO3溶液能吸收SO2的原因是
②汽车尾气中形成硝酸型酸雨的物质是
(2)NOx储存还原技术可有效降低柴油发动机在空气过量条件下NOx的排放。如下图所示NOx的储存和还原在不同时段交替进行,通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。

①储存NOx的物质是
②与Ba(NO3)2反应生成1molN2需要还原性尾气H2
(3)生物法脱H2S的原理为:
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4
 2Fe2(S04)3+2H2O
2Fe2(S04)3+2H2O①硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是
②由图1和图2判断使用硫杆菌的最佳条件为

(4)太阳能光电催化—化学耦合分解H2S的装置如图所示。

该太阳能光电催化—化学耦合分解H2S的过程可描述为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】砷 在元素周期表中与氮同主族,砷及其化合物被运用在农药、医药和染料等领域中。某含砷工业废水经处理可转化为粗
在元素周期表中与氮同主族,砷及其化合物被运用在农药、医药和染料等领域中。某含砷工业废水经处理可转化为粗 ,流程如下:
,流程如下:
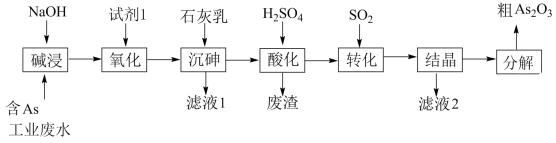
已知:
①含 工业废水主要以亚砷酸(
工业废水主要以亚砷酸( )形式存在,
)形式存在, 为三元弱酸,受热分解为
为三元弱酸,受热分解为 ;
;
② 微溶于水,
微溶于水, 难溶于水。
难溶于水。
回答下列问题:
(1)砷元素在元素周期表中的位置为_______ 。
(2)“碱浸”中发生反应的离子方程式为_______ 。
(3)从绿色化学角度考虑,“试剂1”可以选择_______ (填化学式)。
(4)“沉砷”在流程中的目的是_______ ;“沉砷”的最佳温度是 ,温度高于
,温度高于 时,随温度升高转化率下降,可能的原因是
时,随温度升高转化率下降,可能的原因是_______ 。
(5)“废渣”的主要成分是_______ ,“转化”中发生反应的化学方程式为_______ 。
(6)从综合利用的角度考虑“滤液2”可返回_______ 步骤中循环再利用。
 在元素周期表中与氮同主族,砷及其化合物被运用在农药、医药和染料等领域中。某含砷工业废水经处理可转化为粗
在元素周期表中与氮同主族,砷及其化合物被运用在农药、医药和染料等领域中。某含砷工业废水经处理可转化为粗 ,流程如下:
,流程如下:
已知:
①含
 工业废水主要以亚砷酸(
工业废水主要以亚砷酸( )形式存在,
)形式存在, 为三元弱酸,受热分解为
为三元弱酸,受热分解为 ;
;②
 微溶于水,
微溶于水, 难溶于水。
难溶于水。回答下列问题:
(1)砷元素在元素周期表中的位置为
(2)“碱浸”中发生反应的离子方程式为
(3)从绿色化学角度考虑,“试剂1”可以选择
(4)“沉砷”在流程中的目的是
 ,温度高于
,温度高于 时,随温度升高转化率下降,可能的原因是
时,随温度升高转化率下降,可能的原因是(5)“废渣”的主要成分是
(6)从综合利用的角度考虑“滤液2”可返回
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。请用相关的化学术语回答下列问题:
(1) 在这些元素中,最不活泼的是 ,非金属性最强的是___________,金属性最强的是___________;(填元素符号或化学式,下同。)
(2) 这些元素形成的最高价氧化物对应的水化物中碱性最强的 ,酸性最强的__________;
(3) ①、②、③、④、⑤这五种元素的原子半径由大到小的顺序为 ;
(4) ⑥的氢化物的电子式为 ,① 在空气中燃烧后生成产物的电子式 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA[ | 0 |
| 2 | ⑤ | ⑥ | ⑦ | |||||
| 3 | ① | ③ | ④ | ⑧ | ⑨ | |||
| 4 | ② |
(2) 这些元素形成的最高价氧化物对应的水化物中碱性最强的 ,酸性最强的__________;
(3) ①、②、③、④、⑤这五种元素的原子半径由大到小的顺序为 ;
(4) ⑥的氢化物的电子式为 ,① 在空气中燃烧后生成产物的电子式 。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】下表是元素周期表的一部分。

已知A、B、C、D、E、X、Y是由表中给出元素组成的常见单质或化合物,并存在如图所示的转化关系(部分生成物和反应条件已略去):
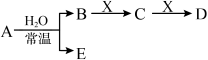
(1)⑧的元素符号是______ 。
(2)⑤与As两种元素中,非金属性较强的是______ (填元素符号)。
(3)用化学符号表示②⑤⑥⑦四种元素的简单离子半径由大到小是______________________ 。
(4)元素③与②的最高价氧化物对应的水化物反应的化学方程式是________ 。
(5)若A为红棕色气体,则A、X、D的化学式分别为________ 、________ 、________ 。

已知A、B、C、D、E、X、Y是由表中给出元素组成的常见单质或化合物,并存在如图所示的转化关系(部分生成物和反应条件已略去):
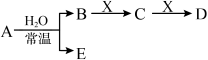
(1)⑧的元素符号是
(2)⑤与As两种元素中,非金属性较强的是
(3)用化学符号表示②⑤⑥⑦四种元素的简单离子半径由大到小是
(4)元素③与②的最高价氧化物对应的水化物反应的化学方程式是
(5)若A为红棕色气体,则A、X、D的化学式分别为
您最近一年使用:0次
【推荐1】NaCl是重要的化工原料。回答下列问题:
(1)元素Na的焰色反应呈___________ 色。价电子被激发到相邻高能级后形成的激发态Na原子,其价电了轨道表示式为___________ 。
(2)KBr具有NaCl型的晶体结构,但其熔点比NaCl低,原因是___________ 。
(3)在适当的条件下,电解NaCl水溶液可制得 NaClO3。
①NaCl水溶液中,不存在的微粒间作用力有___________ (填序号)。
A.离子键 B.极性键 C.配位键 D.氢键 E.范德华力
②ClO3-离子的几何构型为___________ ,中心原子的杂化方式为___________ 。
(4)NaCl晶体在50~300GPa的高压下和Cl2反应,可以形成一种新晶体,其立方晶胞如下图所示(大球为Cl,小球为Na)。

①若A的原子坐标为(0,0,0),B的原子坐标为( ,0,
,0, ),则C的原子坐标为
),则C的原子坐标为__________ 。
②晶体中,Cl构成的多面体包含___________ 个三角形的面,与Cl紧邻的Na个数为___________ 。
③已知晶胞参数为apm,阿伏伽德罗常数的值为NA,则该晶体的密度为_________ g·cm-3(列出计算式)。
(1)元素Na的焰色反应呈
(2)KBr具有NaCl型的晶体结构,但其熔点比NaCl低,原因是
(3)在适当的条件下,电解NaCl水溶液可制得 NaClO3。
①NaCl水溶液中,不存在的微粒间作用力有
A.离子键 B.极性键 C.配位键 D.氢键 E.范德华力
②ClO3-离子的几何构型为
(4)NaCl晶体在50~300GPa的高压下和Cl2反应,可以形成一种新晶体,其立方晶胞如下图所示(大球为Cl,小球为Na)。

①若A的原子坐标为(0,0,0),B的原子坐标为(
 ,0,
,0, ),则C的原子坐标为
),则C的原子坐标为②晶体中,Cl构成的多面体包含
③已知晶胞参数为apm,阿伏伽德罗常数的值为NA,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】X、Y、Z、W、Q为原子序数依次增大的前四周期元素,X核外未成对电子数有2个,与其他元素均能形成二元化合物;Y是地壳中含量最多的金属元素;Z是遗传物质的组成元素之一;W内层电子数是最外层电子数的9倍;Q基态原子价层电子排布中成对电子数和未成对电子数相同。据此回答下列问题:
(1)Q的基态原子的价层电子排布式为____________________ 。
(2)电负性最大的是_________________ ,第一电离能介于Y和Z之间的同周期元素有__________ (填元素符号)。
(3)Y和W的氯化物熔点高的是_________ (填化学式),原因是____________________________ ;与Z的低价氯化物互为等电子体的离子是_____________ 。
(4)咖啡因对中枢神经有兴奋作用,其结构简式如图。常温下,咖啡因在水中的溶解度为2g,加适量水杨酸钠[C6H4(OH)(COONa)]可使其溶解度增大,其原因可能是_____________________ ,分子中氮原子的杂化类型有_______________ 。

(5)已知WX的密度为3.25g/cm3,单元晶胞边长481pm,试
确定该单元晶胞中含有______ 个WX,属于__________ 立方结构(填写面心、简单或体心),晶胞中距离W最近的X有________ 个。
(1)Q的基态原子的价层电子排布式为
(2)电负性最大的是
(3)Y和W的氯化物熔点高的是
(4)咖啡因对中枢神经有兴奋作用,其结构简式如图。常温下,咖啡因在水中的溶解度为2g,加适量水杨酸钠[C6H4(OH)(COONa)]可使其溶解度增大,其原因可能是

(5)已知WX的密度为3.25g/cm3,单元晶胞边长481pm,试
确定该单元晶胞中含有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】氢燃料的储存是氢燃料电池应用的关键,储氢材料能可逆地大量吸放氢,在氢的储存与输送过程中是一种重要载体。回答下列问题:
(1)某种镧镍合金储氢材料的晶体结构单元如图所示。La为第六周期元素,与Sc(钪)元素同一纵列,则基态La原子的价电子排布式为__________ ,基态Ni原子核外有__________ 个未成对电子。

(2)晶体结构单元中La原子的配位数为__________ 个,该合金的密度约为 ,则该晶体结构单元的体积为
,则该晶体结构单元的体积为__________  (保留两位有效数字)。
(保留两位有效数字)。
(3)钠铝合金储氢后的化学式为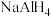 ,其阴离子的中心原子的价电子对数为
,其阴离子的中心原子的价电子对数为__________ 对,该离子的空间构型是__________ 。
(4)十二氢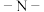 乙基咔唑(
乙基咔唑( )是一种有机储氢材料,该材料储氢后的脱氢是技术关键,
)是一种有机储氢材料,该材料储氢后的脱氢是技术关键, 合金催化剂能在较低温度下使其达到脱氢的目的。脱氢机理如图:
合金催化剂能在较低温度下使其达到脱氢的目的。脱氢机理如图:
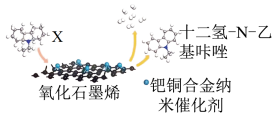
储氢后的十二氢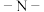 乙基咔唑为图中的X,则X中碳原子的杂化方式有
乙基咔唑为图中的X,则X中碳原子的杂化方式有__________ 种,钯铜合金纳米催化剂中微粒之间的作用力是__________ ,脱氢的化学方程式是__________ 。
(1)某种镧镍合金储氢材料的晶体结构单元如图所示。La为第六周期元素,与Sc(钪)元素同一纵列,则基态La原子的价电子排布式为

(2)晶体结构单元中La原子的配位数为
 ,则该晶体结构单元的体积为
,则该晶体结构单元的体积为 (保留两位有效数字)。
(保留两位有效数字)。(3)钠铝合金储氢后的化学式为
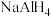 ,其阴离子的中心原子的价电子对数为
,其阴离子的中心原子的价电子对数为(4)十二氢
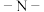 乙基咔唑(
乙基咔唑( )是一种有机储氢材料,该材料储氢后的脱氢是技术关键,
)是一种有机储氢材料,该材料储氢后的脱氢是技术关键, 合金催化剂能在较低温度下使其达到脱氢的目的。脱氢机理如图:
合金催化剂能在较低温度下使其达到脱氢的目的。脱氢机理如图:
储氢后的十二氢
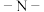 乙基咔唑为图中的X,则X中碳原子的杂化方式有
乙基咔唑为图中的X,则X中碳原子的杂化方式有
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】磷酸二氢钾( )广泛用于工农业生产中,以磷灰石为原料生产磷酸二氢钾的工业流程为:
)广泛用于工农业生产中,以磷灰石为原料生产磷酸二氢钾的工业流程为:
I.制备磷酸
方法1——热法(如图)
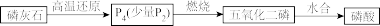
方法2——湿法(如图)

已知:①磷灰石的主要成分是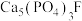 ,还含有铝、铁、镁、硅等元素。
,还含有铝、铁、镁、硅等元素。
②白磷( )常温下为固体,易升华。
)常温下为固体,易升华。
③除了钾、钠、铵外的磷酸盐、磷酸一氢盐往往难溶于水;磷酸二氢盐绝大多数都易溶于水。
(1)热法和湿法都需要先将磷灰石粉碎,目的是___________ 。
(2)“高温还原”是在石英砂(主要成分 )存在下,用焦炭将
)存在下,用焦炭将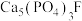 还原,反应过程中同时有CO和两种钙盐生成,主要反应的化学方程式为
还原,反应过程中同时有CO和两种钙盐生成,主要反应的化学方程式为___________ 。
(3)“酸浸”时,用两酸(硫酸和磷酸)分步浸取比只用硫酸浸取率更高,先加入的酸为___________ 。酸浸时会产生一种能腐蚀玻璃的物质,这种物质的分子式为___________ 。
(4)“脱硫”时,用 除去粗磷酸中少量的
除去粗磷酸中少量的 ,其离子方程式为
,其离子方程式为___________ 。
(5)与湿法相比,热法制备磷酸的缺点是___________ 。(列一条)
II.制备磷酸二氢钾
向原料液(含等物质的量KCl与 的水溶液)加入正三丁胺(难溶于水的无色液体、弱碱),保持30℃一个小时,抽滤,滤饼经洗涤、干燥得磷酸二氢钾,滤液中加入氨水再生有机相,并生成副产物。
的水溶液)加入正三丁胺(难溶于水的无色液体、弱碱),保持30℃一个小时,抽滤,滤饼经洗涤、干燥得磷酸二氢钾,滤液中加入氨水再生有机相,并生成副产物。
(6)正三丁胺在制备过程中的作用为___________ 。
(7)副产物的化学式为___________ 。
(8)若制备磷酸过程中磷元素损失a%,制备磷酸二氢钾时原料的转化率为b%,则1吨含“ ”(类似于盐可写成氧化物的形式)28.4%的磷灰石可生产磷酸二氢钾
”(类似于盐可写成氧化物的形式)28.4%的磷灰石可生产磷酸二氢钾___________ g。
 )广泛用于工农业生产中,以磷灰石为原料生产磷酸二氢钾的工业流程为:
)广泛用于工农业生产中,以磷灰石为原料生产磷酸二氢钾的工业流程为:I.制备磷酸
方法1——热法(如图)
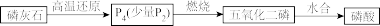
方法2——湿法(如图)

已知:①磷灰石的主要成分是
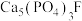 ,还含有铝、铁、镁、硅等元素。
,还含有铝、铁、镁、硅等元素。②白磷(
 )常温下为固体,易升华。
)常温下为固体,易升华。③除了钾、钠、铵外的磷酸盐、磷酸一氢盐往往难溶于水;磷酸二氢盐绝大多数都易溶于水。
(1)热法和湿法都需要先将磷灰石粉碎,目的是
(2)“高温还原”是在石英砂(主要成分
 )存在下,用焦炭将
)存在下,用焦炭将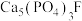 还原,反应过程中同时有CO和两种钙盐生成,主要反应的化学方程式为
还原,反应过程中同时有CO和两种钙盐生成,主要反应的化学方程式为(3)“酸浸”时,用两酸(硫酸和磷酸)分步浸取比只用硫酸浸取率更高,先加入的酸为
(4)“脱硫”时,用
 除去粗磷酸中少量的
除去粗磷酸中少量的 ,其离子方程式为
,其离子方程式为(5)与湿法相比,热法制备磷酸的缺点是
II.制备磷酸二氢钾
向原料液(含等物质的量KCl与
 的水溶液)加入正三丁胺(难溶于水的无色液体、弱碱),保持30℃一个小时,抽滤,滤饼经洗涤、干燥得磷酸二氢钾,滤液中加入氨水再生有机相,并生成副产物。
的水溶液)加入正三丁胺(难溶于水的无色液体、弱碱),保持30℃一个小时,抽滤,滤饼经洗涤、干燥得磷酸二氢钾,滤液中加入氨水再生有机相,并生成副产物。(6)正三丁胺在制备过程中的作用为
(7)副产物的化学式为
(8)若制备磷酸过程中磷元素损失a%,制备磷酸二氢钾时原料的转化率为b%,则1吨含“
 ”(类似于盐可写成氧化物的形式)28.4%的磷灰石可生产磷酸二氢钾
”(类似于盐可写成氧化物的形式)28.4%的磷灰石可生产磷酸二氢钾
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】氯化亚铜(化学式可表示为CuCl)常用作有机合成工业中的催化剂,微溶于水、不溶于乙醇,在潮湿空气中易水解、易被氧化。某学习小组用工业废渣(主要成分为Cu2S和Fe2O3)制取CuCl并同时得到电路板蚀刻液,实验步骤如图:
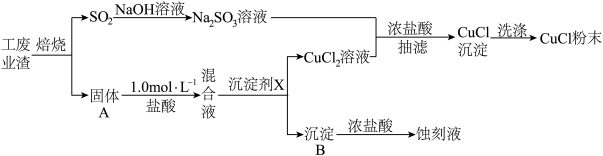
已知:
根据以上信息回答下列问题:
(1)写出焙烧过程中产生SO2的化学方程式:______ ;实验室中常用亚硫酸钠固体与70%的浓硫酸制备二氧化硫,若要达到控制反应速率的目的,图中可选用的装置是_____ (填标号)。
A.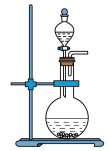 B.
B.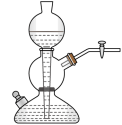 C.
C.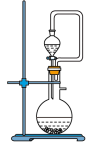 D.
D.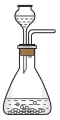
(2)混合液中加入的沉淀剂X可为______ ;(填化学式),调节溶液的pH至______ ,过滤得到CuCl2溶液。
(3)①向Na2SO3溶液中逐滴加入CuCl2溶液,再加入少量浓盐酸,混匀后倾倒出清液,抽滤、洗涤、干燥获得CuCl产品,该反应的离子方程式为______ 。
②抽滤也称减压过滤,请选择合适的仪器并组装抽滤的装置从溶液中得到CuCl产品,装置连接顺序为_____→_____→E→_____(填标号)。______
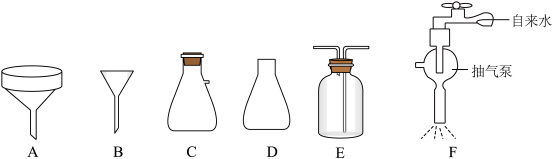
下列有关抽滤的说法错误的是_____ (填标号)。
A.原理为利用抽气泵使抽滤瓶中的压强降低,以达到固液分离的目的
B.过滤速度快,可得到较干燥的沉淀
C.实验结束后,先关抽气泵,后拔开抽滤瓶接管
③抽滤过程中先用“去氧水”作洗涤剂洗涤产品,然后立即用无水酒精洗涤,并在70℃真空下干燥2h,冷却后密封包装,密封包装的原因是______ 。
(4)实验测得氯化亚铜蒸气的相对分子质量为199,则氯化亚铜的分子式为_____ ;氯化亚铜定量吸收CO后形成配合物Cu2(CO)2Cl2·2H2O(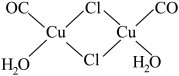 ),则Cu2(CO)2Cl2·2H2O中的配位体为
),则Cu2(CO)2Cl2·2H2O中的配位体为_____ (填化学式)。

已知:
| 金属阳离子 | 开始沉淀的pH | 完全沉淀的pH |
| Cu2+ | 4.8 | 6.4 |
| Fe3+ | 2.7 | 3.7 |
(1)写出焙烧过程中产生SO2的化学方程式:
A.
 B.
B. C.
C. D.
D.
(2)混合液中加入的沉淀剂X可为
(3)①向Na2SO3溶液中逐滴加入CuCl2溶液,再加入少量浓盐酸,混匀后倾倒出清液,抽滤、洗涤、干燥获得CuCl产品,该反应的离子方程式为
②抽滤也称减压过滤,请选择合适的仪器并组装抽滤的装置从溶液中得到CuCl产品,装置连接顺序为_____→_____→E→_____(填标号)。

下列有关抽滤的说法错误的是
A.原理为利用抽气泵使抽滤瓶中的压强降低,以达到固液分离的目的
B.过滤速度快,可得到较干燥的沉淀
C.实验结束后,先关抽气泵,后拔开抽滤瓶接管
③抽滤过程中先用“去氧水”作洗涤剂洗涤产品,然后立即用无水酒精洗涤,并在70℃真空下干燥2h,冷却后密封包装,密封包装的原因是
(4)实验测得氯化亚铜蒸气的相对分子质量为199,则氯化亚铜的分子式为
 ),则Cu2(CO)2Cl2·2H2O中的配位体为
),则Cu2(CO)2Cl2·2H2O中的配位体为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】废锂离子电池回收是对“城市矿产”的资源化利用,可促进新能源产业链闭环。废磷酸铁锂粉主要成分为LiFePO4,还含有的杂质为Al、Cu、Mg.回收LiCl的工艺流程如下:
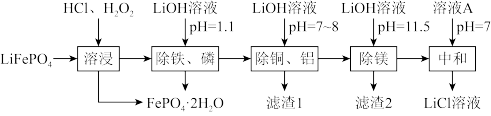
已知:①LiFePO4难溶于水;
②Ksp(FePO4)=1.0×10-22,Ksp(Li3PO4)=2.5×10-3,Ksp[Fe(OH)3]=4.0×10-38。
回答下列问题:
(1)LiFePO4中Fe的化合价为_______ ,Fe在周期表中的位置为_______ 。
(2)“溶浸”可得到含氯化锂的浸出液,材料中的铝、铜、镁等金属杂质也会溶入浸出液,生成CuCl2的离子反应方程式:_______ ;生成FePO4·2H2O的离子反应方程式:_______ 。
(3)该法实现了定向除杂,溶浸后不可直接将浸出液的pH调至11.5,其原因之一是:FePO4(s)+3Li+(aq)+3OH—(aq)=Fe(OH)3(s)+Li3PO4(s),该反应的平衡常数表达式为K=_______ ,若溶液中的c(Li+)=1mol/L,不考虑其他离子参与反应,为使Li+不转化为Li3PO4沉淀,则pH需小于_______ 。
(4)溶液A为_______ ,若最终获得LiCl溶液的体积为aL,其中Li+的密度为pg·L-1,废磷酸铁锂粉中Li元素的质量为mg,三次加入的LiOH溶液中溶质LiOH的总质量为m1g,其利用率为α,求废磷酸铁锂粉中Li元素的回收率x(Li)=_______ ×100%。(列出计算式即可,不用化简)

已知:①LiFePO4难溶于水;
②Ksp(FePO4)=1.0×10-22,Ksp(Li3PO4)=2.5×10-3,Ksp[Fe(OH)3]=4.0×10-38。
回答下列问题:
(1)LiFePO4中Fe的化合价为
(2)“溶浸”可得到含氯化锂的浸出液,材料中的铝、铜、镁等金属杂质也会溶入浸出液,生成CuCl2的离子反应方程式:
(3)该法实现了定向除杂,溶浸后不可直接将浸出液的pH调至11.5,其原因之一是:FePO4(s)+3Li+(aq)+3OH—(aq)=Fe(OH)3(s)+Li3PO4(s),该反应的平衡常数表达式为K=
(4)溶液A为
您最近一年使用:0次



