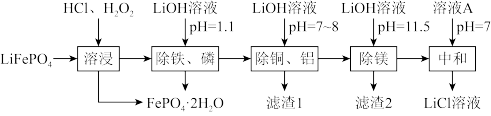
废锂离子电池回收是对“城市矿产”的资源化利用,可促进新能源产业链闭环。废磷酸铁锂粉主要成分为LiFePO4,还含有的杂质为Al、Cu、Mg.回收LiCl的工艺流程如下:
已知:①LiFePO4难溶于水;
②Ksp(FePO4)=1.0×10-22,Ksp(Li3PO4)=2.5×10-3,Ksp[Fe(OH)3]=4.0×10-38。
回答下列问题:
(1)LiFePO4中Fe的化合价为_______ ,Fe在周期表中的位置为_______ 。
(2)“溶浸”可得到含氯化锂的浸出液,材料中的铝、铜、镁等金属杂质也会溶入浸出液,生成CuCl2的离子反应方程式:_______ ;生成FePO4·2H2O的离子反应方程式:_______ 。
(3)该法实现了定向除杂,溶浸后不可直接将浸出液的pH调至11.5,其原因之一是:FePO4(s)+3Li+(aq)+3OH—(aq)=Fe(OH)3(s)+Li3PO4(s),该反应的平衡常数表达式为K=_______ ,若溶液中的c(Li+)=1mol/L,不考虑其他离子参与反应,为使Li+不转化为Li3PO4沉淀,则pH需小于_______ 。
(4)溶液A为_______ ,若最终获得LiCl溶液的体积为aL,其中Li+的密度为pg·L-1,废磷酸铁锂粉中Li元素的质量为mg,三次加入的LiOH溶液中溶质LiOH的总质量为m1g,其利用率为α,求废磷酸铁锂粉中Li元素的回收率x(Li)=_______ ×100%。(列出计算式即可,不用化简)

已知:①LiFePO4难溶于水;
②Ksp(FePO4)=1.0×10-22,Ksp(Li3PO4)=2.5×10-3,Ksp[Fe(OH)3]=4.0×10-38。
回答下列问题:
(1)LiFePO4中Fe的化合价为
(2)“溶浸”可得到含氯化锂的浸出液,材料中的铝、铜、镁等金属杂质也会溶入浸出液,生成CuCl2的离子反应方程式:
(3)该法实现了定向除杂,溶浸后不可直接将浸出液的pH调至11.5,其原因之一是:FePO4(s)+3Li+(aq)+3OH—(aq)=Fe(OH)3(s)+Li3PO4(s),该反应的平衡常数表达式为K=
(4)溶液A为
21-22高三下·湖北·阶段练习 查看更多[2]
更新时间:2022-03-22 19:14:29
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
【推荐1】铊(Tl)在工业中的用途非常广泛,其中铊锡合金可用作超导材料;铊镉合金是原子能工业中的重要材料。铊主要从铅精矿焙烧产生的富铊灰(主要成分PbO、ZnO、Fe2O3、FeO、Tl2O等)中提炼,具体工艺流程如图:
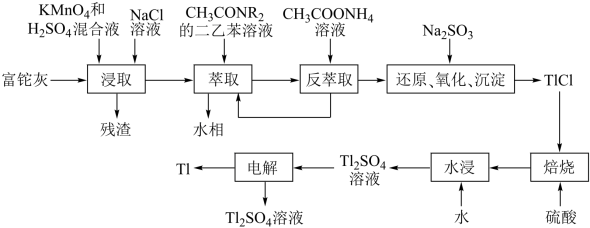
已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂CH3CONR2的二乙苯溶液,萃取过程的反应原理为H++CH3CONR2+TlCl
 [CH3CONR2H]TlCl4。
[CH3CONR2H]TlCl4。
(1)“浸取”过程中生成可溶性的TlCl ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(2)“反萃取”过程中发生反应的化学方程式为_______ 。
(3)“还原、氧化、沉淀”过程中TlCl 发生反应的离子方程式为
发生反应的离子方程式为_______ 。

已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂CH3CONR2的二乙苯溶液,萃取过程的反应原理为H++CH3CONR2+TlCl

 [CH3CONR2H]TlCl4。
[CH3CONR2H]TlCl4。(1)“浸取”过程中生成可溶性的TlCl
 ,该反应的离子方程式为
,该反应的离子方程式为(2)“反萃取”过程中发生反应的化学方程式为
(3)“还原、氧化、沉淀”过程中TlCl
 发生反应的离子方程式为
发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】向含有NaOH的NaClO溶液中逐滴滴入FeSO4溶液,滴加过程中溶液的pH随FeSO4溶液的体积的变化曲线及实验现象见表。
资料:i.饱和NaClO溶液的pH约为11
ii.Ksp[Fe(OH)3]=2.8×10-39
(1)Cl2和NaOH溶液制取NaClO的离子方程式是____ 。
(2)A点溶液的pH约为13,主要原因是____ 。
(3)结合离子方程式解释A→B溶液的pH显著下降的主要原因:____ 。
(4)NaClO溶液中含氯各微粒的物质的量分数与pH的关系如图。
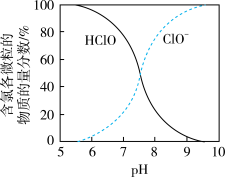
①M点溶液含氯的微粒有____ 。
②C点附近生成红褐色沉淀的主要反应的离子方程式是____ 。
(5)检验iv中气体的方法是____ 。
(6)A→D的过程中,溶液的pH一直下降,原因是____ 。
(7)整个滴加过程中发生的反应与____ 、微粒的浓度等有关。
| 变化曲线 | 实验现象 |
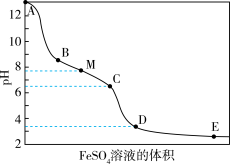 | i.A→B产生红褐色沉淀 ii.B→C红褐色沉淀的量增多 iii.C→D红褐色沉淀的量增多 iv.D点附近产生有刺激性气味的气体 v.D→E红褐色沉淀的量略有增多 |
ii.Ksp[Fe(OH)3]=2.8×10-39
(1)Cl2和NaOH溶液制取NaClO的离子方程式是
(2)A点溶液的pH约为13,主要原因是
(3)结合离子方程式解释A→B溶液的pH显著下降的主要原因:
(4)NaClO溶液中含氯各微粒的物质的量分数与pH的关系如图。

①M点溶液含氯的微粒有
②C点附近生成红褐色沉淀的主要反应的离子方程式是
(5)检验iv中气体的方法是
(6)A→D的过程中,溶液的pH一直下降,原因是
(7)整个滴加过程中发生的反应与
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】某补铁剂的主要成分是硫酸亚铁( ),说明书中建议“本品与维生素C同服”。为探究其原理,用放置7天的
),说明书中建议“本品与维生素C同服”。为探究其原理,用放置7天的 溶液(pH略大于3)进行下列实验。
溶液(pH略大于3)进行下列实验。
资料:维生素C( )又称抗坏血酸,将溶于水,其溶液呈酸性
)又称抗坏血酸,将溶于水,其溶液呈酸性
Ⅰ.检验铁元素的价态
(1)ⅰ中观察到_____________ ,说明溶液中存在 。由ⅱ中溶液近乎无色可以推测维生素C与
。由ⅱ中溶液近乎无色可以推测维生素C与 发生了反应:
发生了反应: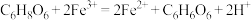 ,该反应的还原剂是
,该反应的还原剂是_____________ 。
(2)ⅰ中与 溶液滴加KSCN溶液后变浅红色相关的2个离子反应方程式为
溶液滴加KSCN溶液后变浅红色相关的2个离子反应方程式为__________ 。
(3)经分析ⅱ中检验方案不严谨,应考虑pH对反应的影响,依据是_______________ 。
Ⅱ.探究pH对ⅱ中反应的影响
补充实验如下,继续探究pH对ⅱ中反应的影响。
(4)试剂a为_____________ ,由实验现象可得结论:pH对 与SCN的显色反应有影响。
与SCN的显色反应有影响。
(5)分析实验ⅰ~ⅲ,下列说法合理的是_____________ (填序号)。
a.维生素C具有氧化性和酸性
b.同服维生素C可减缓补铁剂中 被氧化
被氧化
c.使用KSCN检验 时,宜先将溶液酸化
时,宜先将溶液酸化
 ),说明书中建议“本品与维生素C同服”。为探究其原理,用放置7天的
),说明书中建议“本品与维生素C同服”。为探究其原理,用放置7天的 溶液(pH略大于3)进行下列实验。
溶液(pH略大于3)进行下列实验。资料:维生素C(
 )又称抗坏血酸,将溶于水,其溶液呈酸性
)又称抗坏血酸,将溶于水,其溶液呈酸性Ⅰ.检验铁元素的价态
| 实验序号 | 试管中的试剂 | 实验操作及现象 |
ⅰ | 2mL放置后的 | 滴加5滴KSCN溶液后,溶液变为浅红色 | |
ⅱ | 2mL放置后的 溶液,0.1g维生素C 溶液,0.1g维生素C | 维生素C溶解,溶液 ,滴加5滴KSCN溶液后,溶液近乎无色 ,滴加5滴KSCN溶液后,溶液近乎无色 |
 。由ⅱ中溶液近乎无色可以推测维生素C与
。由ⅱ中溶液近乎无色可以推测维生素C与 发生了反应:
发生了反应: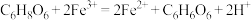 ,该反应的还原剂是
,该反应的还原剂是(2)ⅰ中与
 溶液滴加KSCN溶液后变浅红色相关的2个离子反应方程式为
溶液滴加KSCN溶液后变浅红色相关的2个离子反应方程式为(3)经分析ⅱ中检验方案不严谨,应考虑pH对反应的影响,依据是
Ⅱ.探究pH对ⅱ中反应的影响
补充实验如下,继续探究pH对ⅱ中反应的影响。
实验序号 | 试剂 | 实验操作及现象 |
ⅲ |
| 滴加5滴KSCN溶液后,溶液变为浅红色,浅红色比ⅰ中加深 |
 与SCN的显色反应有影响。
与SCN的显色反应有影响。(5)分析实验ⅰ~ⅲ,下列说法合理的是
a.维生素C具有氧化性和酸性
b.同服维生素C可减缓补铁剂中
 被氧化
被氧化c.使用KSCN检验
 时,宜先将溶液酸化
时,宜先将溶液酸化
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】镍的单质及氧化物常用作催化剂。以含镍废渣(主要含Ni,还含少量NiO、 和
和 )为原料可通过如下过程制取高纯度NiO。
)为原料可通过如下过程制取高纯度NiO。

已知①常温时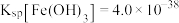 ,
,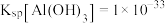 ,
,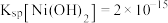 ,溶液中离子的浓度小于
,溶液中离子的浓度小于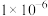 可认为已除尽。
可认为已除尽。
② 难溶于水。
难溶于水。
(1)“浸取”时,当加料完成后,提高镍元素浸出速率的方法有___________ 、___________ 。
(2)“浸取”后,测得溶液中 、
、 和
和 的物质的量浓度分别为
的物质的量浓度分别为 、
、 和
和 ,则“除铝铁”时应控制溶液的
,则“除铝铁”时应控制溶液的 范围为
范围为___________ (设加入氨水时溶液体积不发生变化) 。
(3)“沉镍”后所得 中可能吸附含有少量
中可能吸附含有少量 ,若“沉镍”时使用
,若“沉镍”时使用 溶液,则所得
溶液,则所得 中可能吸附含有少量
中可能吸附含有少量 ,实际生产流程中用
,实际生产流程中用 而不用
而不用 的原因是
的原因是___________ 。
(4)雷尼镍是一种多孔的单质镍,可用作催化剂,工业上可由镍铝合金制得。选择合适的试剂,补充完整制取雷尼镍的方法:取粉碎后的镍铝合金,___________ ,真空干燥得到雷尼镍。(实验中可选用的试剂:10%的稀硫酸、20%的 溶液)
溶液)
(5)为测定某 产品的纯度,现进行如下实验:准确取
产品的纯度,现进行如下实验:准确取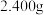 样品,用足量硫酸溶解后,加水稀释到
样品,用足量硫酸溶解后,加水稀释到 ,取
,取 所配溶液于锥形瓶中,加入
所配溶液于锥形瓶中,加入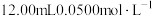 标准
标准 溶液,振荡使其充分反应;向反应后的溶液滴加
溶液,振荡使其充分反应;向反应后的溶液滴加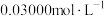 的
的 标准溶液与过量的
标准溶液与过量的 反应,恰好完全反应时消耗
反应,恰好完全反应时消耗 标准溶液体积为
标准溶液体积为 ,计算
,计算 产品的纯度
产品的纯度___________ (写出计算过程,杂质不参与反应),实验过程中反应如下: (未配平);
(未配平);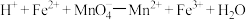 (未配平)。
(未配平)。
 和
和 )为原料可通过如下过程制取高纯度NiO。
)为原料可通过如下过程制取高纯度NiO。
已知①常温时
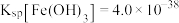 ,
,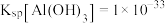 ,
,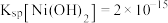 ,溶液中离子的浓度小于
,溶液中离子的浓度小于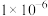 可认为已除尽。
可认为已除尽。②
 难溶于水。
难溶于水。(1)“浸取”时,当加料完成后,提高镍元素浸出速率的方法有
(2)“浸取”后,测得溶液中
 、
、 和
和 的物质的量浓度分别为
的物质的量浓度分别为 、
、 和
和 ,则“除铝铁”时应控制溶液的
,则“除铝铁”时应控制溶液的 范围为
范围为(3)“沉镍”后所得
 中可能吸附含有少量
中可能吸附含有少量 ,若“沉镍”时使用
,若“沉镍”时使用 溶液,则所得
溶液,则所得 中可能吸附含有少量
中可能吸附含有少量 ,实际生产流程中用
,实际生产流程中用 而不用
而不用 的原因是
的原因是(4)雷尼镍是一种多孔的单质镍,可用作催化剂,工业上可由镍铝合金制得。选择合适的试剂,补充完整制取雷尼镍的方法:取粉碎后的镍铝合金,
 溶液)
溶液)(5)为测定某
 产品的纯度,现进行如下实验:准确取
产品的纯度,现进行如下实验:准确取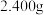 样品,用足量硫酸溶解后,加水稀释到
样品,用足量硫酸溶解后,加水稀释到 ,取
,取 所配溶液于锥形瓶中,加入
所配溶液于锥形瓶中,加入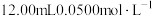 标准
标准 溶液,振荡使其充分反应;向反应后的溶液滴加
溶液,振荡使其充分反应;向反应后的溶液滴加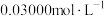 的
的 标准溶液与过量的
标准溶液与过量的 反应,恰好完全反应时消耗
反应,恰好完全反应时消耗 标准溶液体积为
标准溶液体积为 ,计算
,计算 产品的纯度
产品的纯度 (未配平);
(未配平);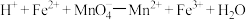 (未配平)。
(未配平)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】碱性锌锰电池是日常生活中消耗量最大的电池,其构造如图所示。
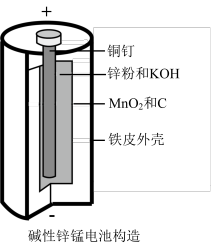
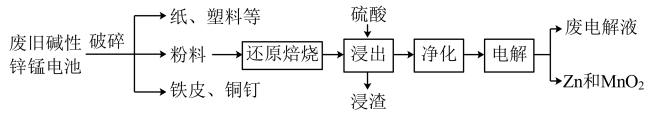
放电时总反应为Zn+2H2O+2MnO2=Zn(OH)2+2MnOOH。从废旧碱性锌锰电池中回收Zn和MnO2的工艺如图:
回答下列问题:
(1)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中MnOOH、MnO2被还原成MnO),主要原因是“粉料”中含有________ 。
(2)“净化”是为了除去浸出液中的Fe2+,方法是:加入________ (填化学式)溶液将Fe2+氧化为Fe3+,再调节pH使Fe3+完全沉淀。已知浸出液中Mn2+、Zn2+的浓度约为0.1 mol·L-1,根据下列数据计算,调节pH的合理范围是________ 至________ 。
(离子浓度小于1×10-5 mol·L-1即为沉淀完全)
(3)“电解”时,阳极的电极反应式为__________ 。本工艺中应循环利用的物质是________ (填化学式)。
(4)若将“粉料”直接与盐酸共热反应后过滤,滤液的主要成分是ZnCl2和MnCl2。“粉料”中的MnOOH与盐酸反应的化学方程式为_________ 。
(5)某碱性锌锰电池维持电流强度0.5A(相当于每秒通过5×10-6 mol电子),连续工作80min即接近失效。如果制造一节电池所需的锌粉为6 g,则电池失效时仍有________ %的金属锌未参加反应。

放电时总反应为Zn+2H2O+2MnO2=Zn(OH)2+2MnOOH。从废旧碱性锌锰电池中回收Zn和MnO2的工艺如图:

回答下列问题:
(1)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中MnOOH、MnO2被还原成MnO),主要原因是“粉料”中含有
(2)“净化”是为了除去浸出液中的Fe2+,方法是:加入
| 化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-13 | 10-17 | 10-38 |
(离子浓度小于1×10-5 mol·L-1即为沉淀完全)
(3)“电解”时,阳极的电极反应式为
(4)若将“粉料”直接与盐酸共热反应后过滤,滤液的主要成分是ZnCl2和MnCl2。“粉料”中的MnOOH与盐酸反应的化学方程式为
(5)某碱性锌锰电池维持电流强度0.5A(相当于每秒通过5×10-6 mol电子),连续工作80min即接近失效。如果制造一节电池所需的锌粉为6 g,则电池失效时仍有
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】钴的氧化物可用作化学工业中的催化剂和染料。利用铜铁钴合金渣制备的酸性电解造液(含大量Co2+及少量的Fe2+、Cu2+、Ca2+、Mg2+、Ni2+杂质)为原料制备CoO的工艺流程如图:
①电解后电解液中还剩余少量的Cu2+
②酸性条件下,Co3+可将Cl-氧化为Cl2
③常温下,相关物质的Ksp如表所示:
回答下列问题:
(1)基态钻原子的价电子轨道表示式为_______ 。
(2)“电解”时,电解装置中_______ 极析出铜。
(3)“除铜”时,发生反应的离子方程式为_______ 。
(4)常温下,加入足量NaF可除去Ca2+和Mg2+,当两者完全沉淀时F—浓度至少为_______ 。
(5)“析钴”的目的除了得到Co(OH)3沉淀外,还有_______ 。
(6)“沉钴”时,不使用饱和草酸钠溶液的原因是_______ 。
(7)空气氛围下加热CoC2O4•2H2O[M(CoC2O4•2H2O)=183g/mol]固体样品时,其分解过程分3个阶段,对应温度范围和失重率(失重率= )如表所示:
)如表所示:
第ii阶段生成的固体氧化物仅有一种,该固体氧化物为_______ (填化学式)。
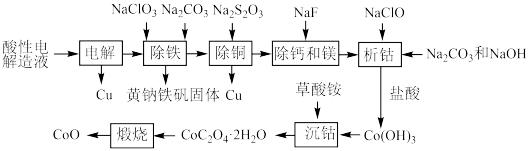
①电解后电解液中还剩余少量的Cu2+
②酸性条件下,Co3+可将Cl-氧化为Cl2
③常温下,相关物质的Ksp如表所示:
| Co(OH)3 | Co(OH)2 | CaF2 | MgF2 |
| 1.6×10-44 | 6.3×10-15 | 4.0×10-11 | 9.0×10-11 |
(1)基态钻原子的价电子轨道表示式为
(2)“电解”时,电解装置中
(3)“除铜”时,发生反应的离子方程式为
(4)常温下,加入足量NaF可除去Ca2+和Mg2+,当两者完全沉淀时F—浓度至少为
(5)“析钴”的目的除了得到Co(OH)3沉淀外,还有
(6)“沉钴”时,不使用饱和草酸钠溶液的原因是
(7)空气氛围下加热CoC2O4•2H2O[M(CoC2O4•2H2O)=183g/mol]固体样品时,其分解过程分3个阶段,对应温度范围和失重率(失重率=
 )如表所示:
)如表所示:| 热分解阶段 | i | ii | iii |
| 热分解温度/℃ | l50~210 | 290~320 | 890~920 |
| 失重率/% | 19.67 | 36.43 | 2.91 |
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
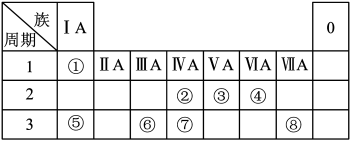
(1)地壳中含量居于第二位的元素在周期表中的位置是___________ 。
(2)②的最高价氧化物的分子式为___________ ;⑦的最高价氧化物对应水化物的分子式为___________ 。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:___________ 、___________ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
(5)半径大小比较:③___________ ④;金属性强弱比较:⑤___________ ⑥(填“>”、“<”或“=”)。
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为___________ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)②的最高价氧化物的分子式为
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
| A.最高正化合价为+6 | B.气态氢化物比 稳定 稳定 |
| C.最高价氧化物对应水化物的酸性比硫酸弱 | D.单质在常温下可与氢气化合 |
(5)半径大小比较:③
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】下表中的实线表示元素周期表的部分边界。①~⑤分别表示元素周期表中对应位置的元素。

(1)元素③④⑤的氢化物的稳定性由强到弱的顺序是____________________ (用氢化物的化学式表示)。
(2)元素③一般在化合物中显________ 价,但在与______ 形成化合物时,所显示的价态正好相反。
(3)M、N两种化合物均由①②③④四种元素组成,写出此两种化合物在水溶液中发生反应的离子方程式:____________________________________ 。
(4)X、Y、Z代表原子序数依次增大的三种短周期元素。在周期表中,Y与X相邻,Y与Z也相邻;X、Y和Z三种元素原子的最外层电子数之和为17;X、Y、Z三种元素有的是上表中编号①~⑤的元素,有的不是,请在上表中用元素符号标出不是①~⑤元素的相应位置。___________
(5)某同学受镧系、锕系元素排列方式的启发,将元素周期表设计成下列更简明的形式,把118种元素全部排列在内,表中除A、B、C、D外每个位置只表示一种元素。则该表中的A位置包含________ (填数字)种元素。C位置中的元素是否全部是金属元素________ (填“是”或“否”)。


(1)元素③④⑤的氢化物的稳定性由强到弱的顺序是
(2)元素③一般在化合物中显
(3)M、N两种化合物均由①②③④四种元素组成,写出此两种化合物在水溶液中发生反应的离子方程式:
(4)X、Y、Z代表原子序数依次增大的三种短周期元素。在周期表中,Y与X相邻,Y与Z也相邻;X、Y和Z三种元素原子的最外层电子数之和为17;X、Y、Z三种元素有的是上表中编号①~⑤的元素,有的不是,请在上表中用元素符号标出不是①~⑤元素的相应位置。
(5)某同学受镧系、锕系元素排列方式的启发,将元素周期表设计成下列更简明的形式,把118种元素全部排列在内,表中除A、B、C、D外每个位置只表示一种元素。则该表中的A位置包含

您最近一年使用:0次
【推荐3】下图表示元素周期表的前三周期,表中的字母各代表一种元素,请回答下列问题:
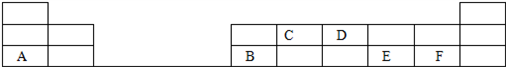
①写出D单质的电子式____________ ;A与E的上一周期同主族元素形成的原子个数比为1:1的化合物的电子式_______________ 。
②E和F分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)_____________ ;
③A的最高价氧化物对应的水化物中所含化学键为___________________ ,其水溶液与B单质反应的离子方程式为___________________________ ;
④写出实验室制备F单质的化学方程式______________________________________ 。
⑤将Fe与C的一种单质(导体)用导线连接,共同浸入到食盐水中构成闭合回路,其中C极为_____ 极(填正或负),该电极反应式为:____________________ 。
⑥以D2H4和O2为原料,与KOH溶液形成的原燃料电池中,负极反应式为___________ ,
(生成物对环境友好无污染)
当外电路转移0.2 mol电子时,消耗的O2在标准状况下的体积为___________ 。

①写出D单质的电子式
②E和F分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)
③A的最高价氧化物对应的水化物中所含化学键为
④写出实验室制备F单质的化学方程式
⑤将Fe与C的一种单质(导体)用导线连接,共同浸入到食盐水中构成闭合回路,其中C极为
⑥以D2H4和O2为原料,与KOH溶液形成的原燃料电池中,负极反应式为
(生成物对环境友好无污染)
当外电路转移0.2 mol电子时,消耗的O2在标准状况下的体积为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】金属镓(Ga)应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。
(1)镓(Ga)的原子结构示意图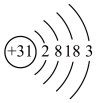 ,镓元素在周期表中的位置是
,镓元素在周期表中的位置是__________ 。
(2)GaN是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。一种镍催化法生产GaN的工艺如图:
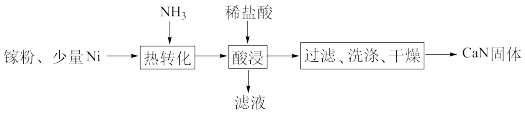
①“热转化”时Ga转化为GaN的化学方程式是__________ 。
②“酸浸”操作的目的是__________ 。
③某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:
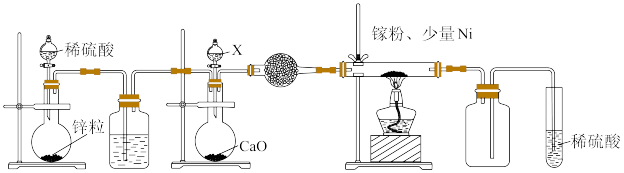
仪器X中的试剂是__________ (写名称)。加热前需先通入H2的作用是__________ 。
(3)As与N同主族,GaAs也是一种重要的半导体材料。
①下列事实不能用元素周期律解释的__________ (填字母)。
a.碱性:Ga(OH)3>Al(OH)3 b.非金属性:As>Ga c. 酸性:H3AsO4>H3AsO3
②废弃含GaAs的半导体材料可以用浓硝酸溶解,生成H3AsO4和Ga(NO3)3,写出该反应的化学方程式__________
(1)镓(Ga)的原子结构示意图
 ,镓元素在周期表中的位置是
,镓元素在周期表中的位置是(2)GaN是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。一种镍催化法生产GaN的工艺如图:

①“热转化”时Ga转化为GaN的化学方程式是
②“酸浸”操作的目的是
③某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:

仪器X中的试剂是
(3)As与N同主族,GaAs也是一种重要的半导体材料。
①下列事实不能用元素周期律解释的
a.碱性:Ga(OH)3>Al(OH)3 b.非金属性:As>Ga c. 酸性:H3AsO4>H3AsO3
②废弃含GaAs的半导体材料可以用浓硝酸溶解,生成H3AsO4和Ga(NO3)3,写出该反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】 (钉)被广泛用于制笔。某小组以某含
(钉)被广泛用于制笔。某小组以某含 废料[主要成分是
废料[主要成分是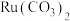 ,含
,含 (其中
(其中 为+6价)、
为+6价)、 、
、 、
、 和
和 等]为原料制备
等]为原料制备 的流程如图所示:
的流程如图所示:
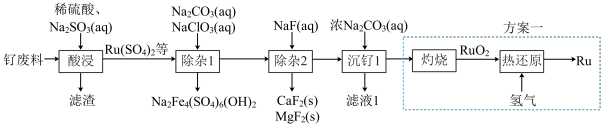
已知:常温下, ,
, ;离子浓度小于或等于
;离子浓度小于或等于 时认为该离子已被完全除去。
时认为该离子已被完全除去。
回答下列问题:
(1)滤渣主要成分是___________ (填化学式)。
(2)“酸浸”中 转化成
转化成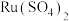 的离子方程式为
的离子方程式为___________ 。
(3)“除杂1”中氯元素被还原成最低价态,若只氧化 ,生成
,生成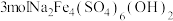 理论上需要
理论上需要___________ 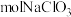 。
。
(4)“除杂1”之后,若滤液中 ,则“除杂2”中先生成的沉淀是
,则“除杂2”中先生成的沉淀是___________ (填化学式)。“除杂2”的滤液中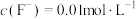 ,则
,则 和
和 是否除尽?
是否除尽?___________ (填“是”或“否”)。
(5)“除杂2”宜选择的容器有___________(填标号)。
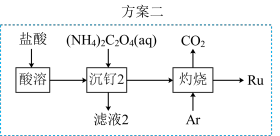
(6)该小组设计方案2优化方案1,从安全角度分析,方案2优于方案1,其理由是___________ 。
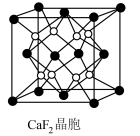
(7) 晶胞如图所示,晶胞中,钙离子将晶胞切割成8个小空隙,
晶胞如图所示,晶胞中,钙离子将晶胞切割成8个小空隙, 可以看成是填充在
可以看成是填充在 割切的空隙中,则
割切的空隙中,则 填充在
填充在 构成的
构成的___________ (填“正八面体形”“正方形”或“正四面体形”)空隙中,其填充率为___________ 。
 (钉)被广泛用于制笔。某小组以某含
(钉)被广泛用于制笔。某小组以某含 废料[主要成分是
废料[主要成分是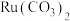 ,含
,含 (其中
(其中 为+6价)、
为+6价)、 、
、 、
、 和
和 等]为原料制备
等]为原料制备 的流程如图所示:
的流程如图所示:
已知:常温下,
 ,
, ;离子浓度小于或等于
;离子浓度小于或等于 时认为该离子已被完全除去。
时认为该离子已被完全除去。回答下列问题:
(1)滤渣主要成分是
(2)“酸浸”中
 转化成
转化成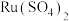 的离子方程式为
的离子方程式为(3)“除杂1”中氯元素被还原成最低价态,若只氧化
 ,生成
,生成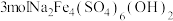 理论上需要
理论上需要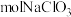 。
。(4)“除杂1”之后,若滤液中
 ,则“除杂2”中先生成的沉淀是
,则“除杂2”中先生成的沉淀是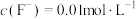 ,则
,则 和
和 是否除尽?
是否除尽?(5)“除杂2”宜选择的容器有___________(填标号)。
| A.陶瓷 | B.铁质 | C.石英 | D.氧化铝 |
(6)该小组设计方案2优化方案1,从安全角度分析,方案2优于方案1,其理由是

(7)
 晶胞如图所示,晶胞中,钙离子将晶胞切割成8个小空隙,
晶胞如图所示,晶胞中,钙离子将晶胞切割成8个小空隙, 可以看成是填充在
可以看成是填充在 割切的空隙中,则
割切的空隙中,则 填充在
填充在 构成的
构成的
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】镉( )可用于制作发光电子组件。以铜镉废渣(含
)可用于制作发光电子组件。以铜镉废渣(含 、
、 、
、 、
、 等单质)为原料制备镉的工艺流程如下:
等单质)为原料制备镉的工艺流程如下:

浸出后的溶液中含有 、
、 、
、 等金属离子,相关金属离子形成氢氧化物沉淀的
等金属离子,相关金属离子形成氢氧化物沉淀的 (开始沉淀的
(开始沉淀的 按金属离子浓度为
按金属离子浓度为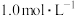 计算)如下表:
计算)如下表:
(1)“浸出”时通入氮气而不是通入空气进行搅拌的原因是___________ 。
(2)“氧化”时发生反应的离子方程式为___________ 。 也能氧化
也能氧化 ,工业生产中不选用
,工业生产中不选用 的原因是
的原因是___________ 。
(3)“调 ”时控制溶液
”时控制溶液 在3.3~5.9之间,“滤渣”的主要成分是
在3.3~5.9之间,“滤渣”的主要成分是___________ (填化学式)。
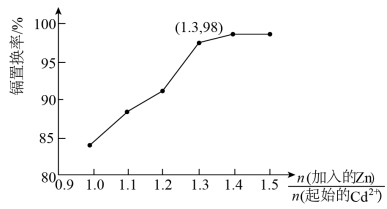
(4)“置换”时发生的反应为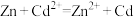 。
。
镉置换率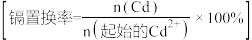 与
与 的关系如图所示。实际生产中选择
的关系如图所示。实际生产中选择 的原因是
的原因是___________ 。
(5) 和
和 同族且相邻,部分金属水合离子的颜色如下表所示:
同族且相邻,部分金属水合离子的颜色如下表所示:
①金属水合离子是否有颜色与金属离子的结构间的关系可描述为___________ 。
②硫酸酸化的硫酸铁溶液中铁元素以 形式存在而使溶液呈浅紫色,向其中滴入几滴
形式存在而使溶液呈浅紫色,向其中滴入几滴 溶液,因生成
溶液,因生成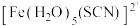 、
、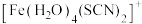 等离子而使溶液呈红色,能发生上述反应的原因是
等离子而使溶液呈红色,能发生上述反应的原因是___________ 。
 )可用于制作发光电子组件。以铜镉废渣(含
)可用于制作发光电子组件。以铜镉废渣(含 、
、 、
、 、
、 等单质)为原料制备镉的工艺流程如下:
等单质)为原料制备镉的工艺流程如下:
浸出后的溶液中含有
 、
、 、
、 等金属离子,相关金属离子形成氢氧化物沉淀的
等金属离子,相关金属离子形成氢氧化物沉淀的 (开始沉淀的
(开始沉淀的 按金属离子浓度为
按金属离子浓度为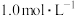 计算)如下表:
计算)如下表:| 氢氧化物 |  |  | 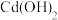 |
开始沉淀的 | 1.5 | 5.9 | 7.2 |
沉淀完全的 | 3.3 | 8.9 | 9.9 |
(2)“氧化”时发生反应的离子方程式为
 也能氧化
也能氧化 ,工业生产中不选用
,工业生产中不选用 的原因是
的原因是(3)“调
 ”时控制溶液
”时控制溶液 在3.3~5.9之间,“滤渣”的主要成分是
在3.3~5.9之间,“滤渣”的主要成分是(4)“置换”时发生的反应为
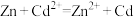 。
。镉置换率
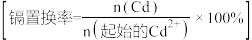 与
与 的关系如图所示。实际生产中选择
的关系如图所示。实际生产中选择 的原因是
的原因是
(5)
 和
和 同族且相邻,部分金属水合离子的颜色如下表所示:
同族且相邻,部分金属水合离子的颜色如下表所示:| 离子 | 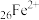 |  | 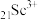 | 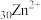 | 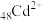 |
| 颜色 | 浅绿色 | 蓝色 | 无色 | 无色 | 无色 |
②硫酸酸化的硫酸铁溶液中铁元素以
 形式存在而使溶液呈浅紫色,向其中滴入几滴
形式存在而使溶液呈浅紫色,向其中滴入几滴 溶液,因生成
溶液,因生成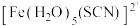 、
、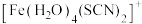 等离子而使溶液呈红色,能发生上述反应的原因是
等离子而使溶液呈红色,能发生上述反应的原因是
您最近一年使用:0次