下列依据热化学方程式得出的结论正确的是
| A.已知2C(s)+2O2(g)=2CO2(g) ΔH=a kJ·mol-1,2C(s)+O2(g)=2CO(g) ΔH=b kJ·mol-1,则a>b |
| B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH= -57.3 kJ·mol-1,则含1mol NaOH的稀溶液与足量稀醋酸完全中和,放出的热量等于57.3kJ |
| C.已知P(白磷,s)=P(红磷,s) ΔH<0,则白磷比红磷稳定 |
D.已知H2(g)+I2(g) 2HI(g) ΔH= -a kJ·mol-1向密闭容器中加入2mol H2和2mol I2(g),充分反应后放出的热量小于2a kJ 2HI(g) ΔH= -a kJ·mol-1向密闭容器中加入2mol H2和2mol I2(g),充分反应后放出的热量小于2a kJ |
19-20高二上·辽宁盘锦·阶段练习 查看更多[10]
河南省驻马店市环际大联考2023-2024学年高二上学期11月期中考试化学试题山东省威海乳山市第一中学2022-2023学年高二下学期开学考试化学试题山东省潍坊第一中学2022-2023学年高二上学期期末考试化学试题甘肃省金昌市永昌县第一高级中学2022-2023学年高二上学期第一次月考化学试题辽宁省部分高中2021-2022学年高三上学期期中评测化学试题重庆市第一中学校2021-2022学年高一下学期期末考试化学试题黑龙江省哈尔滨市第六中学2021-2022学年高二上学期期中考试化学试题山东省实验中学2019-2020学年高二上学期期中考试化学试题山东省师范大学附属中学2019-2020学年高二上学期第五次学分认定考试化学试题辽宁省盘锦市第二高级中学2019-2020学年高二10月月考化学试题
更新时间:2019-10-31 19:42:03
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】将V1mL 1.00 mol·L-1HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是( )
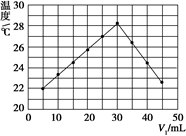

| A.做该实验时环境温度为22 ℃ |
| B.该实验可分多次把NaOH溶液倒入盛有盐酸的小烧杯中 |
| C.NaOH溶液的浓度约为1.50 mol·L-1 |
| D.该实验表明有水生成的反应都是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】强酸与强碱的稀溶液发生中和反应的热效应为H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1。分别向1 L1.0 mol·L-1的NaOH溶液中加入足量①浓硫酸、②稀硫酸、③稀盐酸,恰好完全反应的热效应分别为ΔH1、ΔH2、ΔH3,下列关系正确的是
| A.ΔH1>ΔH2>ΔH3 | B.ΔH1<ΔH2=ΔH3 |
| C.ΔH1<ΔH2<ΔH3 | D.ΔH1=ΔH2<ΔH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=﹣Q1kJ•mol﹣1
2H2(g)+O2(g)=2H2O(g) ΔH2=﹣Q2kJ•mol﹣1
2H2(g)+O2(g)=2H2O(l) ΔH3=﹣Q3kJ•mol﹣1
现取体积比1∶4的甲烷和氢气的混合气体11.2 L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为( )
2H2(g)+O2(g)=2H2O(g) ΔH2=﹣Q2kJ•mol﹣1
2H2(g)+O2(g)=2H2O(l) ΔH3=﹣Q3kJ•mol﹣1
现取体积比1∶4的甲烷和氢气的混合气体11.2 L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为( )
| A.0.1Q1+0.2Q2 | B.0.1Q1+0.2Q3 | C.0.1Q1+0.4Q3 | D.0.1Q1+0.4Q2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知25°C、101 kPa时,
①C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol;
②2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol;
③2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol;
下列判断不正确的是
①C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol;
②2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol;
③2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol;
下列判断不正确的是
| A.6 g碳完全燃烧时放出热量196.75 kJ |
| B.反应②可以自发进行 |
| C.H2的燃烧热ΔH= -241.8 kJ/mol |
| D.制备水煤气的热化学反应方程式为:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.3 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某温度下,在体积为5 L的密闭容器中,充入1molA气体,发生如下可逆反应: 2A(g) B(g)+C(g);ΔH=+akJ·mol-1 (a>0),2min后反应达到平衡,A为0.4 mol。下列叙述中不正确的是
B(g)+C(g);ΔH=+akJ·mol-1 (a>0),2min后反应达到平衡,A为0.4 mol。下列叙述中不正确的是
 B(g)+C(g);ΔH=+akJ·mol-1 (a>0),2min后反应达到平衡,A为0.4 mol。下列叙述中不正确的是
B(g)+C(g);ΔH=+akJ·mol-1 (a>0),2min后反应达到平衡,A为0.4 mol。下列叙述中不正确的是| A.充分反应后,反应吸收的热量为0.5a kJ |
| B.0-2 min时间内B物质的平均反应速率为0.03 mol/(L·min) |
| C.达平衡后,保持温度和容器体积不变,再充入1 mol A,平衡向正反应方向移动 |
| D.若温度和容器体积不变,起始时充入B和C各0.5 mol,则达平衡时,n(A)等于0.4 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】有关能量的判断或表示方法正确的是( )
| A.需要加热才能发生的反应一定是吸热反应 |
B.从C(石墨, 金刚石, 金刚石,  ,可知:金刚石比石墨更稳定 ,可知:金刚石比石墨更稳定 |
| C.等质量的硫蒸气和硫固体分别完全燃烧,前者放出热量更多 |
D.若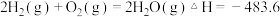  ,则 ,则 燃烧热为 燃烧热为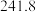  |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知ROH(R=Na、K)固体溶于水放热,有关过程能量变化如图
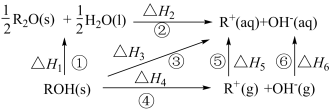
| A.反应①:ΔH1<0,ΔS<0 |
| B.ΔH4(NaOH<ΔH4(KOH) |
| C.ΔH3>ΔH2 |
| D.ΔH4=ΔH1+ΔH2+ΔH5+ΔH6 |
您最近一年使用:0次


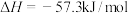 。现分别取50mL 0.50mol/L醋酸溶液与50mL 0.55mo/L NaOH溶液进行反应,用如图实验装置测定该反应的反应热
。现分别取50mL 0.50mol/L醋酸溶液与50mL 0.55mo/L NaOH溶液进行反应,用如图实验装置测定该反应的反应热 ,下列说法错误的是
,下列说法错误的是