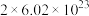已知25°C、101 kPa时,
①C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol;
②2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol;
③2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol;
下列判断不正确的是
①C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol;
②2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol;
③2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol;
下列判断不正确的是
| A.6 g碳完全燃烧时放出热量196.75 kJ |
| B.反应②可以自发进行 |
| C.H2的燃烧热ΔH= -241.8 kJ/mol |
| D.制备水煤气的热化学反应方程式为:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.3 kJ/mol |
更新时间:2022-01-18 12:47:09
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列热化学方程式及有关应用的叙述中,正确的是
A. 的燃烧热为 的燃烧热为 ,则 ,则 燃烧热的热化学方程式可表示为 燃烧热的热化学方程式可表示为 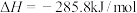 |
B.取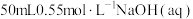 和 和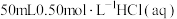 进行中和反应反应热的测定,用温度计测定 进行中和反应反应热的测定,用温度计测定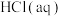 起始温度后,直接测定 起始温度后,直接测定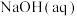 的温度,会使中和反应反应热 的温度,会使中和反应反应热 偏小 偏小 |
C.已知 、101KPa条件下: 、101KPa条件下: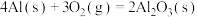  , ,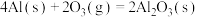 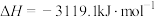 ,则 ,则 比 比 稳定 稳定 |
D. 、30MPa下,将 、30MPa下,将 和 和 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学方程式可表示为 ,放热19.3kJ,其热化学方程式可表示为 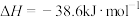 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知: 键的键能为
键的键能为 ;
; 键的键能为
键的键能为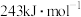 ;
; 键的键能为
键的键能为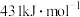 。下列说法中
。下列说法中不正确 的是
 键的键能为
键的键能为 ;
; 键的键能为
键的键能为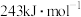 ;
; 键的键能为
键的键能为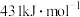 。下列说法中
。下列说法中A. 中的化学键断裂时需要吸收 中的化学键断裂时需要吸收 的能量 的能量 |
B. 分子中的化学键形成时要释放 分子中的化学键形成时要释放 的能量 的能量 |
C.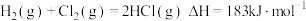 |
D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下图是反应CO(g)+2H2(g)  CH3OH(g)进行过程中的能量变化曲线。曲线a 表示不使用催化剂时反应的能量变化,曲线 b 表示使用催化剂后的能量变化。下列相关说法正确的是
CH3OH(g)进行过程中的能量变化曲线。曲线a 表示不使用催化剂时反应的能量变化,曲线 b 表示使用催化剂后的能量变化。下列相关说法正确的是

 CH3OH(g)进行过程中的能量变化曲线。曲线a 表示不使用催化剂时反应的能量变化,曲线 b 表示使用催化剂后的能量变化。下列相关说法正确的是
CH3OH(g)进行过程中的能量变化曲线。曲线a 表示不使用催化剂时反应的能量变化,曲线 b 表示使用催化剂后的能量变化。下列相关说法正确的是
| A.升高温度,能提高 CO 的转化率 |
| B.使用催化剂后反应热减小,能耗降低 |
| C.生成物的总键能小于反应物的总键能 |
D.热化学方程式为CO(g)+2H2(g)  CH3OH(g) △H =—91 kJ/mol CH3OH(g) △H =—91 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述正确的是
A.将0. 5mol N2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3 H2(g)  2 NH3(g) ΔH=-38.6kJ•mol-1 2 NH3(g) ΔH=-38.6kJ•mol-1 |
| B.C(石墨)=C(金刚石) ΔH=+1.9kJ•mol-1,说明金刚石比石墨稳定 |
| C.甲烷的燃烧热△H=-890. 3 kJ•mol-1,甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890. 3 kJ•mol-1 |
| D.已知H+(aq)+OH-(aq)=H2O(l) △H=-57.4 kJ•mol-1,20g氢氧化钠固体溶于稀盐酸中恰好完全反应时放出的热量大于28.7kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知反应:①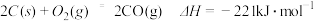 ,②
,②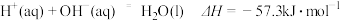 。下列结论正确的是
。下列结论正确的是
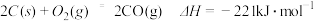 ,②
,②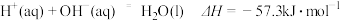 。下列结论正确的是
。下列结论正确的是A.碳的摩尔燃烧焓大于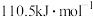 |
B.①的焓变为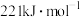 |
C.稀硫酸与稀 溶液反应的中和热为 溶液反应的中和热为 |
D.稀醋酸与稀 溶液反应生成 溶液反应生成 水,放出 水,放出 热量 热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏加德罗常数的数值,下列有关叙述正确的是
| A.1mol的CO2和H2O(g)的混合气体与过量Na2O2充分反应转移的电子数为2NA |
| B.0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10NA |
C.已知反应2SO2(g)+O2(g) 2SO3(g) △H=−a kJ/mol,当生成NA个SO3分子时,反应放出的热量大于0.5a kJ 2SO3(g) △H=−a kJ/mol,当生成NA个SO3分子时,反应放出的热量大于0.5a kJ |
| D.常温下,2.7g铝与足量氢氧化钠溶液反应,失去的电子数为0.3NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】以NA代表阿伏伽德罗常数,则关于热化学方程式:C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l) △H=-1300.0kJ·mol-1的说法中,正确的是
| A.当有10NA个电子转移时,该反应就放出1300kJ的能量 |
| B.当有NA个水分子生成且为液态时,吸收1300kJ的能量 |
| C.当有22.4LC2H2(乙炔)完全燃烧生成CO2和液态H2O(l)时,该反应就放出1300kJ的能量 |
| D.当有8NA个碳氧共用电子对生成时,该反应就吸收1300kJ的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知:
①CH4 ( g )+4NO2( g )=4NO( g ) +CO2( g )+2H2O( g ) △H=一574 kJ·mol-1
②CH4 ( g )+4NO( g )=2N2( g )+CO2( g )+2H2O( g ) △H=一1160 kJ·mol一1
下列正确的选项是
①CH4 ( g )+4NO2( g )=4NO( g ) +CO2( g )+2H2O( g ) △H=一574 kJ·mol-1
②CH4 ( g )+4NO( g )=2N2( g )+CO2( g )+2H2O( g ) △H=一1160 kJ·mol一1
下列正确的选项是
| A.CH4 ( g )+2NO2 ( g )= N2( g )+CO2 ( g )+2H2O ( l)△H=一867 kJ·mol-1 |
| B.CH4 ( g )+2NO2 ( g )= N2( g )+CO2 ( g )+2H2O ( g)△H=一867 kJ·mol-1 |
| C.CH4 ( g )+2NO2 ( g )= N2( g )+CO2 ( g )+2H2O ( g)△H=一586kJ·mol-1 |
| D.CH4 ( g )+2NO2 ( g )= N2( g )+CO2 ( g )+2H2O ( g)△H=+586kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.放热反应都能自发进行,吸热反应都不能自发进行 |
| B.熵增加且吸热的反应一定是自发反应 |
| C.常温下,反应C(s)+CO2(g) =2CO(g)不能自发进行,则该反应的ΔH>0 |
| D.活化分子间的碰撞一定是有效碰撞 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】X(g) +Y(g)⇌Z(g) + W(g)反应过程中能量变化如图,下列说法正确的是
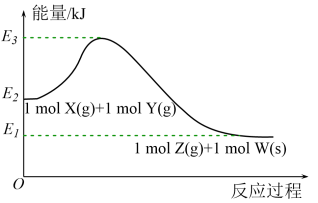

| A.任何条件下,该反应一定能自发进行 |
| B.该反应的△H=(E1-E2)kJ·mol-1 |
| C.若加入催化剂,(E3-E2)的值变化 |
| D.高温下有利于该反应正向进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】汽车尾气净化器中发生的反应为 2NO(g)+2CO(g) N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0L的恒容密闭容器中发生上述反应,测得有关实验数据如表:下列说法正确的是
N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0L的恒容密闭容器中发生上述反应,测得有关实验数据如表:下列说法正确的是
 N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0L的恒容密闭容器中发生上述反应,测得有关实验数据如表:下列说法正确的是
N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0L的恒容密闭容器中发生上述反应,测得有关实验数据如表:下列说法正确的是| 容器 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | ||||
| NO | CO | N2 | CO2 | N2 | CO2 | ||
| I | 400 | 0.2 | 0.2 | 0 | 0 | 0.12 | |
| II | 400 | 0.4 | 0.4 | 0 | 0 | ||
| III | 300 | 0 | 0 | 0.1 | 0.2 | 0.075 | |
| A.该反应的△S<0、△H>0 |
| B.容器I中达到平衡所需时间2s,则v(N2)=0.06mol/(L·s) |
| C.若起始时向I中充入NO、CO、N2、CO2各0.1mol,开始时v(正)>v(逆) |
| D.达到平衡时,体系中c(CO)关系: c(CO,容器Ⅱ)>2 c(CO,容器Ⅰ) |
您最近一年使用:0次

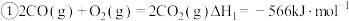
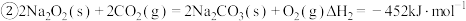 根据以上热化学方程式,下列判断
根据以上热化学方程式,下列判断 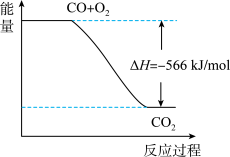
 的反应过程和能量关系
的反应过程和能量关系

 与
与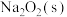 反应放出
反应放出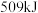 热量时,电子转移数为
热量时,电子转移数为