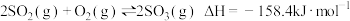下列有关中和热实验的说法正确的是
| A.用铜丝替代环形玻璃搅拌棒,测得ΔH偏高 |
| B.强酸与强碱反应生成1 mol水的ΔH都约为-57.3 kJ·mol-1 |
| C.测定中和热实验中,读取混合溶液不再变化的温度为终止温度 |
| D.某同学通过实验测出稀盐酸和稀NaOH溶液反应的中和热ΔH=-52.3 kJ·mol-1,造成这一结果的原因不可能是:用测量盐酸的温度计直接测定NaOH溶液的温度 |
19-20高二上·浙江杭州·阶段练习 查看更多[8]
浙江省杭州市西湖高级中学2019-2020学年高二10月月考化学试题人教版(2019)高二化学选择性必修1第一章 化学反应的热效应 第一节 反应热 课时1 反应热 焓变河南省原阳县第三高级中学2020-2021学年高二上学期第一次月考化学试题(已下线)高中化学《新教材变化解读与考法剖析》第一章 化学反应的热效应(人教版2019选择性必修1)宁夏石嘴山市第三中学2022-2023学年高二下学期第一次月考化学(理)试题河南省信阳高级中学2023-2024学年高二上学期开学考试化学试题浙江省杭州市四校2023-2024学年高二上学期10月联考化学试题云南省曲靖市第一中学2023-2024学年高二上学期11月期中考试化学试题
更新时间:2019-11-02 22:13:41
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法正确的是
A.在中性溶液中能大量共存: 、 、 、 、 、 、 |
B.含有大量 能大量共存: 能大量共存: 、 、 、 、 、 、 |
C.已知辛烷的燃烧热为5518KJ/mol,则辛烷燃烧的热化学方程式: , ,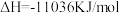 |
| D.已知中和热为57.3KJ/mol,则稀氨水与盐酸反应生成1mol水时放出的热量小于57.3KJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知 H+(aq)+ OH-(aq)→H2O(l)+ Q(Q>0)。若向三份等体积、0.1000 mol/LNaOH溶液中分别加入:①稀醋酸 ②浓硫酸 ③稀硝酸,至恰好完全反应,并将上述过程中放出的热量分别记为Q1、Q2、Q3(单位:kJ)。下列关系式中正确的是
| A.Q1>Q3>Q2 |
| B.Q1>Q2>Q3 |
| C.Q2>Q3>Q1 |
| D.Q3=Q2>Q1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】某实验小组学生用50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量计算中和热。下列说法正确的是
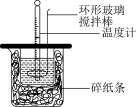

| A.烧杯间填满碎纸条的作用是固定小烧杯 |
| B.若不在烧杯上加盖硬纸板则所测中和热偏低 |
| C.若只将上述实验中的酸碱浓度相互调换,从理论上讲所测得的中和热不相等 |
| D.若用浓硫酸代替盐酸(其他不变),则测得的中和热不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】在中和热的实验测定中,下列操作中使结果偏高的是
| A.实验装置保温、隔热效果差 |
| B.量取酸碱溶液的体积时仰视读数 |
| C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中 |
| D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列有关测定中和反应反应热实验的说法正确的是
| A.所有酸的稀溶液与所有碱的稀溶液反应生成1molH2O的ΔH均为-57.3kJ•mol-1 |
| B.中和热的测定实验中,氢氧化钠分批加入,反应更充分,测定的中和热数值误差更小 |
| C.测定中和反应反应热的实验中,混合溶液的温度不再变化时,该温度为终止温度 |
| D.某同学通过实验测出稀盐酸和稀NaOH溶液反成1molH2O反应热ΔH=-52.3kJ•mol-1,造成这一结果的原因可能是用铜丝代替玻璃搅拌器 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法正确的是
| A.浓硫酸与NaOH溶液反应生成1mol水时放出57.3kJ热量 |
| B.稀硫酸和稀Ba(OH)2反应生成1mol水时放出57.3kJ热量 |
| C.1L 1mol/L稀硫酸被NaOH溶液恰好完全中和放出57.3kJ热量 |
| D.0.1mol/L HCl和0.2mol/L NaOH溶液反应的中和热的焓变(ΔH)为-57.3kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列反应中反应热的数值为-53.7kJ的是( )
| A.H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l) ΔH= -a kJ⋅mol-1 |
| B.H2SO4(aq)+Ba(OH)2(aq)=BaSO4(aq)+2H2O(l) ΔH= -b kJ⋅mol-1 |
| C.HCl(aq)+NH3⋅H2O(aq)=NH4Cl(aq)+H2O(l) ΔH= -c kJ⋅mol-1 |
| D.HCl(aq)+NaOH(aq)=NaCl (aq)+ H2O(l) ΔH= -d kJ⋅mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可测定中和热。下列关于该实验的说法正确的是( )
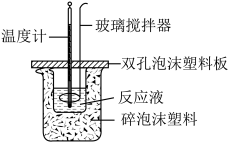

| A.烧杯间的碎泡沫塑料的作用是固定烧杯的位置 |
| B.如果没有环形玻璃搅拌棒,酸碱混合后可用温度计轻轻搅拌 |
| C.做完一次完整的中和热测定实验,温度计需要使用2次,混合液的初始温度和反应最高温度 |
| D.由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ•mol-l可知,1mol稀H2SO4溶液与2molNaOH溶液反应的中和热为57.3kJ•mol-l |
您最近一年使用:0次

 的燃烧热:
的燃烧热: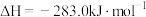 ,则
,则 反应的
反应的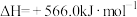
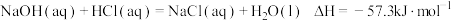 ,则含
,则含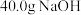 的稀溶液与稀醋酸完全中和,放出
的稀溶液与稀醋酸完全中和,放出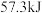 的热量
的热量
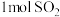 和
和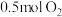 置于密闭容器中充分反应,放出热量
置于密闭容器中充分反应,放出热量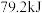 ,则:
,则: