下列对化学反应方向的叙述正确的是
| A.室温下不能自发进行的反应,在高温下有可能自发进行 |
| B.熵增加有利于反应的自发进行,熵减小的反应常温下都不会自发进行 |
| C.非自发反应在任何情况下都不会发生 |
| D.凡是放热反应都是自发的,吸热反应都是非自发的 |
更新时间:2019/11/02 21:24:56
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列有关说法正确的是
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B.已知C(石墨,s)=C(金刚石,s) ΔH>0,故金刚石比石墨稳定 |
| C.放热且熵增加的反应不一定能正向自发进行 |
| D.升高温度能增大单位体积内的活化分子数,加快反应速率 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列各项操作中,会出现“先沉淀后溶解”现象的是( )
| A.向氯化铝溶液中滴加氢氧化钠至过量 |
| B.向饱和的Na2CO3溶液中通入CO2气体直至过量 |
| C.向Na2SiO3溶液中通入氯化氢气体直至过量 |
| D.向CaCl2溶液中通入CO2气体直至过量 |
您最近半年使用:0次
【推荐1】用一种较活泼的金属把另一种金属从化合物中还原出来的方法称为金属热还原法。钠、镁、铝是常用的还原剂。一些常见的金属热还原反应如下:
下列说法不正确的是
| 序号 | 反应 | △H/kJ/mol | △S/J/(mol·K) |
| ① | 2Al(l) + 3BaO(s)=3Ba(g) +Al2O3(s) | 487 | 207.53 |
| ② | 2Al(s) + 3BaO(s)=3Ba(s)+Al2O3(s) | 4 | -15.70 |
| ③ | Mg(l) + 2RbCl(s)=2Rb(g)+MgCl2(s) | 381.77 | 223.06 |
| ④ | 4Na(l)+TiCl4(g)=Ti(s)+4NaCl(s) | -899.8 | -291 |
| A.反应①表明金属沸点:Al>Ba |
| B.对于反应:2Ba(s)+O2(g)=2BaO(s) △H1,4Al(s)+3O2(g)=2Al2O3(s) △H2,由反应②可以推出3△H1≈△H2 |
| C.反应③说明金属活动性顺序:Mg>Rb |
| D.对于反应④: |△H|>>|T△S|说明焓变对该反应的自发性起主要影响作用 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】通过以下反应均可制备 :
:
①煤炭与水反应制氢: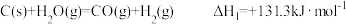
②甲烷与水反应制氢:
③太阳光催化分解水制氢:
下列有关说法正确的是
 :
:①煤炭与水反应制氢:
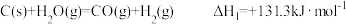
②甲烷与水反应制氢:

③太阳光催化分解水制氢:

下列有关说法正确的是
| A.通过反应①可以将煤转化为清洁燃料 |
B.若反应②使用催化剂,则 减小 减小 |
| C.反应③在低温下可以自发进行 |
D.制备等物质的量的 需要吸收的能量:①<②<③ 需要吸收的能量:①<②<③ |
您最近半年使用:0次

 2H2O(1)
2H2O(1) 

