实验室里用加热正丁醇、溴化钠和浓硫酸的混合物的方法制备1-溴丁烷,还会有烯、醚和溴等产物生成,反应结束后将反应混合物蒸馏分离得到1-溴丁烷。已知有关物质的性质如下:
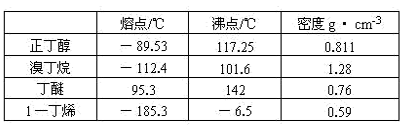
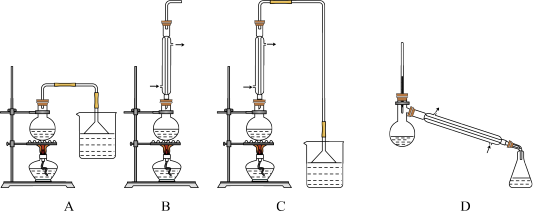
(1)生成1-溴丁烷的反应化学方程式为_____ 。
(2)反应中由于发生副反应而生成副产物烯、醚的反应类型依次为_____ 、_____ 。
(3)生成1-溴丁烷的反应装置应选用图中的______ (填序号),反应加热时的温度t1应控制在_____ 100℃(填“ ”或“”)。
(4)反应结束后,将反应混合物中 l-溴丁烷分离出来,应选用的装置是_____ ,该操作应控制的温度t2范围是_____ 。


(1)生成1-溴丁烷的反应化学方程式为
(2)反应中由于发生副反应而生成副产物烯、醚的反应类型依次为
(3)生成1-溴丁烷的反应装置应选用图中的
(4)反应结束后,将反应混合物中 l-溴丁烷分离出来,应选用的装置是
更新时间:2019-11-06 13:27:36
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室制备1,2-溴乙烷的反应原理如下:CH3CH2OH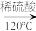 CH2=CH2+H2O CH2=CH2+Br2
CH2=CH2+H2O CH2=CH2+Br2 BrCH2CH2Br可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
BrCH2CH2Br可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
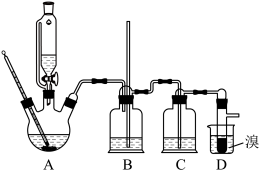
有关数据列表如下:
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是______ (填正确选项前的字母)。
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)装置B的作用是______ 。
(3)在装置c中应加入____ (填正确选项前的字母),其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断该制备反应已经结束的最简单方法是_______ 。
(5)将1, 2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在____ 层(填“上”、“下”)。
(6)若产物中有少量未反应的Br2,最好用______ (填正确选项前的字母)洗涤除去。
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(7)若产物中有少量副产物乙醚,可用________ 的方法除去。
(8)反应过程中应用冷水冷却装置D,其主要目的是_________ ;但又不过度冷却(如用冰水),其原因是______________________ 。
 CH2=CH2+H2O CH2=CH2+Br2
CH2=CH2+H2O CH2=CH2+Br2 BrCH2CH2Br可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
BrCH2CH2Br可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度(g/cm3) | 0.79 | 2.2 | 0.71 |
| 沸点(℃) | 78.5 | 132 | 34.6 |
| 熔点(℃) | -130 | 9 | -116 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)装置B的作用是
(3)在装置c中应加入
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断该制备反应已经结束的最简单方法是
(5)将1, 2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在
(6)若产物中有少量未反应的Br2,最好用
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(7)若产物中有少量副产物乙醚,可用
(8)反应过程中应用冷水冷却装置D,其主要目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:实验室用少量的溴和足量的乙醇、浓硫酸制备1,2﹣二溴乙烷的装置如图所示,其中可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。有关数据列表如下:
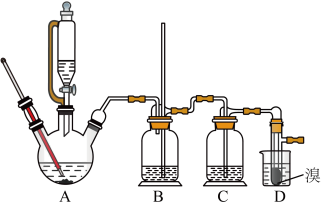
回答下列问题:
(1)用少量的溴和足量的乙醇、浓硫酸制备1,2﹣二溴乙烷的需分两步进行,第一步需要在冰水浴下混合浓硫酸和乙醇,混合时加入试剂的顺序是___ ,使用冰水浴降温的目的是___ ,第二步反应的化学方程式___ 。
(2)在此实验中,要在A中加入___ ,防止___ ,反应温度提高到170℃左右,其最主要目的是___ (填正确选项前的字母)。
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)装置B的作用是___ ,在装置C中应加入__ ,其目的是吸收反应中可能生成的酸性气体(填正确选项前的字母)。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断D中反应结束的方法是___ ,将D中1,2﹣二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___ 层(填“上”、“下”)。
(5)若产物中有少量副产物乙醚,可用___ 的方法除去。
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是__ 。

| 乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm﹣3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)用少量的溴和足量的乙醇、浓硫酸制备1,2﹣二溴乙烷的需分两步进行,第一步需要在冰水浴下混合浓硫酸和乙醇,混合时加入试剂的顺序是
(2)在此实验中,要在A中加入
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)装置B的作用是
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断D中反应结束的方法是
(5)若产物中有少量副产物乙醚,可用
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】在实验室制取乙烯时,其反应为CH3CH2OH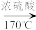 CH2=CH2↑+H2O,该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如图实验装置以验证上述反应生成的混合气体中含己烯、SO2和水蒸气。
CH2=CH2↑+H2O,该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如图实验装置以验证上述反应生成的混合气体中含己烯、SO2和水蒸气。
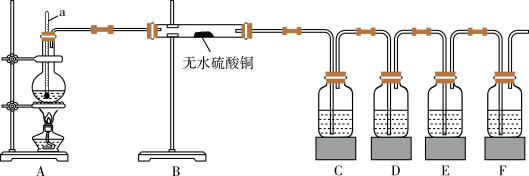
限用试剂(试剂均足量):乙醇、浓硫酸、品红溶液、氢氧化钠溶液、酸性高锰酸钾溶液、溴水。
(1)仪器a的名称为_________ 。
(2)请根据实验的要求完成下列填空:
①D中试剂的作用为_________ 。
②E中的试剂为_________ 。
③F中的试剂为_________ ,可能的实验现象为_________ 。
(3)简述装置B置于装置A、C之间的理由:_________ 。
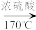 CH2=CH2↑+H2O,该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如图实验装置以验证上述反应生成的混合气体中含己烯、SO2和水蒸气。
CH2=CH2↑+H2O,该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如图实验装置以验证上述反应生成的混合气体中含己烯、SO2和水蒸气。
限用试剂(试剂均足量):乙醇、浓硫酸、品红溶液、氢氧化钠溶液、酸性高锰酸钾溶液、溴水。
(1)仪器a的名称为
(2)请根据实验的要求完成下列填空:
①D中试剂的作用为
②E中的试剂为
③F中的试剂为
(3)简述装置B置于装置A、C之间的理由:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
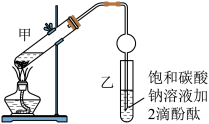
【推荐1】乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室制取乙酸乙酯的主要步骤如下:
①在甲试管(如图)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液。
②连接好装置(装置气密性良好),先加入几片碎瓷片,再加入混合液,小火均匀地加热3~5min。
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。___________ 。(填写序号)
①浓硫酸 ②乙醇 ③乙酸
(2)加入碎瓷片的作用是___________ 与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用除冷凝外,还可以___________ 。
(3)步骤②中需要用小火均匀加热,其主要原因是___________ 并加快反应速率。
(4)浓硫酸在该反应中起到的作用是___________ 。
(5)上述实验中饱和碳酸钠溶液的作用不包括___________(填字母代号)。
(6)若实验中用乙酸和含18O的乙醇作用,该反应的化学方程式是:___________ 。
①在甲试管(如图)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液。
②连接好装置(装置气密性良好),先加入几片碎瓷片,再加入混合液,小火均匀地加热3~5min。
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。
①浓硫酸 ②乙醇 ③乙酸
(2)加入碎瓷片的作用是
(3)步骤②中需要用小火均匀加热,其主要原因是
(4)浓硫酸在该反应中起到的作用是
(5)上述实验中饱和碳酸钠溶液的作用不包括___________(填字母代号)。
| A.反应乙酸 | B.吸收乙醇 |
| C.降低乙酸乙酯的溶解度,有利于分层析出 | D.促进乙酸乙酯的水解 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】乙酸乙酯是一种重要的有机化工原料和工业溶剂,具有低毒性,有甜味,浓度较高时有刺激性气味,易挥发,属于一级易燃品,应储存于低温通风处,远离火种火源。实验室一般通过乙酸和乙醇的酯化反应来制取,实验装置如图所示(夹持装置已省略),主要步骤如下:
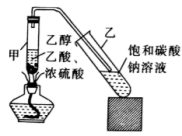
①在甲试管中加入2mL浓硫酸、2mL乙酸和3mL乙醇,再加入几片碎瓷片。
②按图连接好装置(装置的气密性良好),小火均匀地加热3~5min。
③待乙试管收集到一定量产物后停止加热,撤出乙试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层,洗涤、干燥,得乙酸乙酯产品。
(1)写出上述实验中生成乙酸乙酯反应的化学方程式:__________________ 。乙试管中长玻璃导管的作用是____________ 。
(2)甲试管中,混合溶液的加入顺序为_________ (填化学式)。
(3)步骤②中需要用小火均匀加热,其主要原因是________________ 。
(4)为了证明浓硫酸在该反应中起到催化剂和吸水剂的作用,某同学利用上述实验装置进行下列3组实验。实验开始时先用酒精灯微热甲试管中的试剂3min,再加热使之微微沸腾3min。实验结束后,充分振荡乙试管并测其有机层的厚度,实验数据记录如下:
①实验C中
____________ 。
②分析实验_____________ (填字母)的数据,可以推测出浓 的吸水性提高了乙酸乙酯的产率。
的吸水性提高了乙酸乙酯的产率。
③已知:乙酸的密度为1.05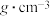 ,乙醇的密度为0.789
,乙醇的密度为0.789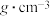 ,实验A收集到的乙酸乙酯的质量为2.464g。则该反应中产品的产率为
,实验A收集到的乙酸乙酯的质量为2.464g。则该反应中产品的产率为______________ 。( )
)

①在甲试管中加入2mL浓硫酸、2mL乙酸和3mL乙醇,再加入几片碎瓷片。
②按图连接好装置(装置的气密性良好),小火均匀地加热3~5min。
③待乙试管收集到一定量产物后停止加热,撤出乙试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层,洗涤、干燥,得乙酸乙酯产品。
(1)写出上述实验中生成乙酸乙酯反应的化学方程式:
(2)甲试管中,混合溶液的加入顺序为
(3)步骤②中需要用小火均匀加热,其主要原因是
(4)为了证明浓硫酸在该反应中起到催化剂和吸水剂的作用,某同学利用上述实验装置进行下列3组实验。实验开始时先用酒精灯微热甲试管中的试剂3min,再加热使之微微沸腾3min。实验结束后,充分振荡乙试管并测其有机层的厚度,实验数据记录如下:
实验组号 | 甲试管中试剂 | 乙试管中试剂 | 有机层的厚度/cm |
A | 3mL乙醇、3mL乙酸、3mL 18 | 饱和
| 3.0 |
B | 3mL乙醇、2mL乙酸、3mL | 0.1 | |
C | amL乙醇、2mL乙酸、2 | 0.6 |

②分析实验
 的吸水性提高了乙酸乙酯的产率。
的吸水性提高了乙酸乙酯的产率。③已知:乙酸的密度为1.05
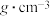 ,乙醇的密度为0.789
,乙醇的密度为0.789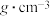 ,实验A收集到的乙酸乙酯的质量为2.464g。则该反应中产品的产率为
,实验A收集到的乙酸乙酯的质量为2.464g。则该反应中产品的产率为 )
)
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
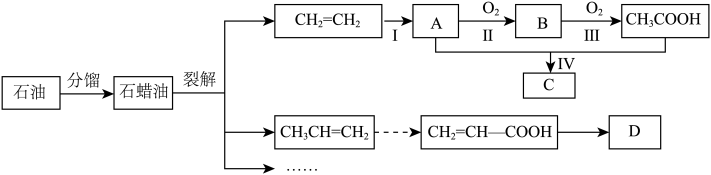
【推荐3】乙烯、乙醇是重要有机化工原料。回答下列问题:
已知: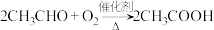
(1)石蜡油裂解产生的不饱和烃是重要的有机合成中间体。
①反应I的化学方程式是___________ 。
②D为高分子化合物,结构简式是___________ 。
③下列装置正确且能达到实验目的的是___________ (填序号)。
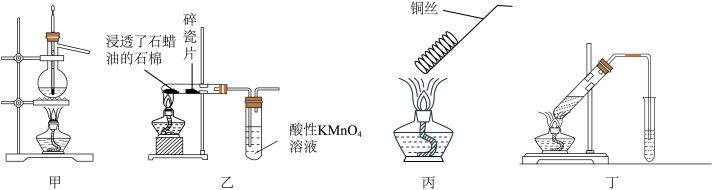
A.甲装置:从石油中分离石蜡油 B.乙装置:证明石蜡油分解生成乙烯
C.丙装置:完成乙醇的催化氧化 D.丁装置:制备乙酸乙酯
(2)已知:CaCl2与C2H5OH形成CaCl2·6C2H5OH.实验室制备乙酸乙酯粗产品并精制提纯,流程如下。
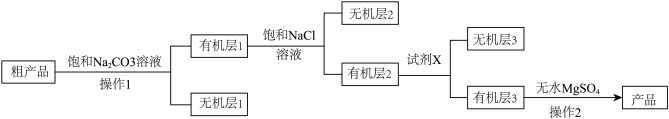
①制备乙酸乙酯的化学方程式为___________ 。
②饱和Na2CO3溶液的作用是___________ ;操作1的名称是___________ 。
③为除去有机层2中的乙醇,加入的试剂X为___________ 。
④选择合适的仪器组装完成操作2(夹持、加热及单孔、双孔橡胶塞、导管等连接仪器略),仪器的连接顺序为d→___________ 。
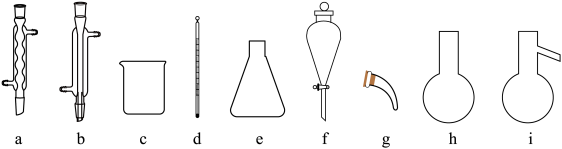

已知:
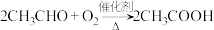
(1)石蜡油裂解产生的不饱和烃是重要的有机合成中间体。
①反应I的化学方程式是
②D为高分子化合物,结构简式是
③下列装置正确且能达到实验目的的是

A.甲装置:从石油中分离石蜡油 B.乙装置:证明石蜡油分解生成乙烯
C.丙装置:完成乙醇的催化氧化 D.丁装置:制备乙酸乙酯
(2)已知:CaCl2与C2H5OH形成CaCl2·6C2H5OH.实验室制备乙酸乙酯粗产品并精制提纯,流程如下。

①制备乙酸乙酯的化学方程式为
②饱和Na2CO3溶液的作用是
③为除去有机层2中的乙醇,加入的试剂X为
④选择合适的仪器组装完成操作2(夹持、加热及单孔、双孔橡胶塞、导管等连接仪器略),仪器的连接顺序为d→

您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,B、D是饮食中两种常见的有机物,F是一种有香味的物质,F中碳原子数是D的两倍。现以A为主要原料合成F和高聚物E,其合成路线如图所示。请回答下列问题
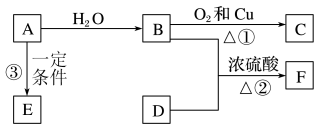
(1)A的结构式为____________ ,F的名称为____________ 。
(2)写出反应的化学方程式
①_____________________________________________ ,反应类型为____________ 。
②_____________________________________________ ,反应类型为____________ 。
③_____________________________________________
(3)实验室怎样鉴别B和D?___________________________________ 。
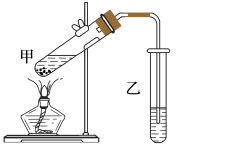
(4)在实验室里我们可以用如图所示的装置来制取F,乙中所盛的试剂为____________ ,该装置图中有一个明显的错误是__________________________________ 。
(5)写出F的同分异构体中与D互为同系物的有机物的所有结构简式:__________ 。

(1)A的结构式为
(2)写出反应的化学方程式
①
②
③
(3)实验室怎样鉴别B和D?
(4)在实验室里我们可以用如图所示的装置来制取F,乙中所盛的试剂为

(5)写出F的同分异构体中与D互为同系物的有机物的所有结构简式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】芳香化合物在一定条件下可与卤代烃发生取代反应。某科研小组以 、ClC(CH3)3为反应物,无水AlCl3为催化剂制备
、ClC(CH3)3为反应物,无水AlCl3为催化剂制备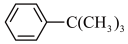 (叔丁基苯)。反应原理如下:
(叔丁基苯)。反应原理如下:

已知:
Ⅰ.实验室模拟制备无水AlCl3的实验装置如图甲所示。
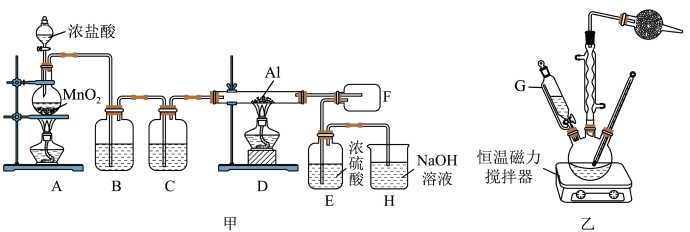
(1)装置B中的试剂为___________ 。
(2)加热顺序:应先点燃___________ (填“A”或“D”)处的酒精灯。
Ⅱ.实验室制取叔丁基苯的装置如图乙所示。
①将35 mL苯和足量的无水AlCl3,加入三颈烧瓶中;②滴加氯代叔丁烷ClC(CH3)3 10 mL;③打开恒温磁力搅拌器反应一段时间;④洗涤,将反应后的混合物依次用稀盐酸、Na2CO3溶液、H2O洗涤分离;⑤在所得产物中加入少量无水MgSO4固体,静置,过滤,蒸馏;⑥称量,得到叔丁基苯10.0 g。
(3)图乙中弯管G的作用为___________ 。
(4)用稀盐酸洗涤的目的是___________ 。
(5)加无水MgSO4固体的作用是___________ 。
 、ClC(CH3)3为反应物,无水AlCl3为催化剂制备
、ClC(CH3)3为反应物,无水AlCl3为催化剂制备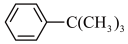 (叔丁基苯)。反应原理如下:
(叔丁基苯)。反应原理如下:
已知:
| 相对分子质量 | 密度/(g/cm3) | 沸点 | 溶解性 | |
| AlCl3 | 133.5 | 2.41 | 181 | 极易潮解并产生白色烟雾,微溶于苯 |
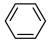 | 78 | 0.88 | 80.1 | 难溶于水 |
| ClC(CH3)3 | 92.5 | 0.85 | 51.6 | 难溶于水,可溶于苯 |
 | 134 | 0.87 | 169 | 难溶于水,易溶于苯 |

(1)装置B中的试剂为
(2)加热顺序:应先点燃
Ⅱ.实验室制取叔丁基苯的装置如图乙所示。
①将35 mL苯和足量的无水AlCl3,加入三颈烧瓶中;②滴加氯代叔丁烷ClC(CH3)3 10 mL;③打开恒温磁力搅拌器反应一段时间;④洗涤,将反应后的混合物依次用稀盐酸、Na2CO3溶液、H2O洗涤分离;⑤在所得产物中加入少量无水MgSO4固体,静置,过滤,蒸馏;⑥称量,得到叔丁基苯10.0 g。
(3)图乙中弯管G的作用为
(4)用稀盐酸洗涤的目的是
(5)加无水MgSO4固体的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
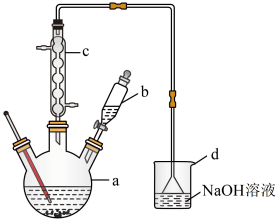
按下列合成步骤回答问题:
(1)在装置a中加入15mL无水苯和少量铁屑。在装置b中小心加入4.0mL液态溴。向装置a中滴入几滴溴,有白雾产生。继续滴加至液溴滴完。装置d的作用是吸收________ 和少量溴蒸汽。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是________________________ ;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入无水氯化钙的目的是________________________ 。
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为________ ,要进一步提纯,下列操作中必须的是________ (填字母代号)。
A.重结晶 B.过滤
C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是________ (填字母代号)。
A.25mL B.50mL
C.250mL D.500mL

| 苯 | 溴 | 溴苯 | |
| 密度/g/cm3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解性 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在装置a中加入15mL无水苯和少量铁屑。在装置b中小心加入4.0mL液态溴。向装置a中滴入几滴溴,有白雾产生。继续滴加至液溴滴完。装置d的作用是吸收
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入无水氯化钙的目的是
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为
A.重结晶 B.过滤
C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是
A.25mL B.50mL
C.250mL D.500mL
您最近一年使用:0次

 浓硫酸
浓硫酸 溶液
溶液


