工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) CH3OH(g),反应过程中的能量变化情况如图所示。
CH3OH(g),反应过程中的能量变化情况如图所示。
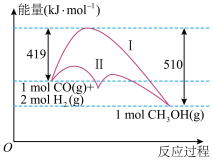
(1)曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。该反应是________ (填“吸热”或“放热”)反应。计算当反应生成1.5 mol CH3OH(g)时,能量变化是________ kJ。
(2)选择适宜的催化剂________ (填“能”或“不能”)改变该反应的反应热。
(3)推测反应CH3OH(g)⇌CO(g)+2H2(g)是________ (填“吸热”或“放热”)反应。
 CH3OH(g),反应过程中的能量变化情况如图所示。
CH3OH(g),反应过程中的能量变化情况如图所示。
(1)曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。该反应是
(2)选择适宜的催化剂
(3)推测反应CH3OH(g)⇌CO(g)+2H2(g)是
2019高一下·全国·专题练习 查看更多[4]
(已下线)2019年3月14日 《每日一题》 必修2 化学反应过程的能量变化图分析2020春(新教材)人教化学第二册第6章 化学反应与能量练习湖北省随州市曾都一中2019-2020学年高一下学期3月月考化学试题人教版2019必修第二册 第六章 本章复习提升
更新时间:2019-03-18 16:15:26
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】科学家盖斯曾提出:“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的。”利用盖斯定律可计算某些特殊反应的热效应。
(1)已知:①P4(s,白磷)+5O2(g)=P4O10(s) △H1=-2983.2kJ/mol;
②P(s,红磷)+ O2(g)=
O2(g)=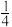 P4O10(s) △H2=-738.5kJ/mol。
P4O10(s) △H2=-738.5kJ/mol。
则白磷转化为红磷的热化学方程式____ ,相同的状况下,白磷的稳定性比红磷____ (填“高”或“低”)。
(2)红磷P(s)和Cl2发生反应生成PCl3和PCl5,反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
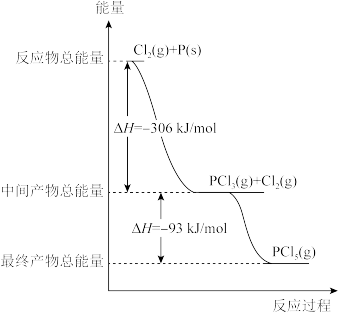
①PCl5分解生成PCl3和Cl2的热化学方程式____ 。
②P和Cl2分两步反应生成1molPCl5的△H3=____ 。
(1)已知:①P4(s,白磷)+5O2(g)=P4O10(s) △H1=-2983.2kJ/mol;
②P(s,红磷)+
 O2(g)=
O2(g)=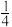 P4O10(s) △H2=-738.5kJ/mol。
P4O10(s) △H2=-738.5kJ/mol。则白磷转化为红磷的热化学方程式
(2)红磷P(s)和Cl2发生反应生成PCl3和PCl5,反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。

①PCl5分解生成PCl3和Cl2的热化学方程式
②P和Cl2分两步反应生成1molPCl5的△H3=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】为了探究化学反应的热效应,某兴趣小组进行了如下实验:
(1)将纯固体物质 分别装入有水的锥形瓶里(发生化学反应),立即塞紧带
分别装入有水的锥形瓶里(发生化学反应),立即塞紧带 形管的塞子,发现
形管的塞子,发现 形管内红墨水的液面高度如图所示。
形管内红墨水的液面高度如图所示。
①如图1所示,发生的反应(假设没有气体生成)是_______ (填“放热”或“吸热”)反应, 是
是_______ (填一种常见氧化物的化学式)。

②如图2所示,发生的反应(假设没有气体生成)是_______ (填“放热”或“吸热”)反应,以下选项中与其能量变化相同的是_______ (填序号)。
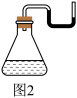
A.碳的燃烧反应 B.CaCO3的分解反应 C.盐酸与NaOH溶液的反应
(2)如下图所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,试管中开始放入几小块铝片,再滴入5mL稀NaOH溶液。试回答下列问题:
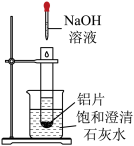
实验中观察到的现象是:铝片逐渐溶解、有大量气泡产生、_______ 。
(1)将纯固体物质
 分别装入有水的锥形瓶里(发生化学反应),立即塞紧带
分别装入有水的锥形瓶里(发生化学反应),立即塞紧带 形管的塞子,发现
形管的塞子,发现 形管内红墨水的液面高度如图所示。
形管内红墨水的液面高度如图所示。①如图1所示,发生的反应(假设没有气体生成)是
 是
是
②如图2所示,发生的反应(假设没有气体生成)是

A.碳的燃烧反应 B.CaCO3的分解反应 C.盐酸与NaOH溶液的反应
(2)如下图所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,试管中开始放入几小块铝片,再滴入5mL稀NaOH溶液。试回答下列问题:

实验中观察到的现象是:铝片逐渐溶解、有大量气泡产生、
您最近一年使用:0次
【推荐3】研究化学反应中的能量变化有利于更好的开发和使用化学能源。
(1)已知H2、CO、CH4的燃烧热分别为285.8kJ·mol-1、283.0kJ·mol-1、890.3kJ·mol-1。
①相同条件下,等质量的H2、CO、CH4分别完全燃烧,放出热量最多的是___________ 。
②2CH4(g)+3O2(g)=2CO(g)+4H2O(l) ΔH=___________ kJ·mol-1。
③等质量的甲烷按a、b两种途径完全转化,放出的热量:途径a___________ 途径b(填“>”、“<”或“=”)
途径a:CH4 CO+H2
CO+H2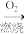 CO2+H2O
CO2+H2O
途径b:CH4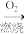 CO2+H2O
CO2+H2O
(2)已知白磷(P4)和P4O6的分子结构和部分化学键的键能分别如下图、表所示:

①写出白磷与氧气反应生成P4O6固体的热化学方程式:___________ 。
②已知P4(白磷,s)=4P(红磷,s)ΔH=-16.7kJ·mol-1。白磷和红磷互为___________ (填“同系物”、“同位素”、“同素异形体”或“同分异构体”),比较稳定的是___________ 。等质量的白磷、红磷分别完全燃烧,放出热量更多的是___________ 。
(1)已知H2、CO、CH4的燃烧热分别为285.8kJ·mol-1、283.0kJ·mol-1、890.3kJ·mol-1。
①相同条件下,等质量的H2、CO、CH4分别完全燃烧,放出热量最多的是
②2CH4(g)+3O2(g)=2CO(g)+4H2O(l) ΔH=
③等质量的甲烷按a、b两种途径完全转化,放出的热量:途径a
途径a:CH4
 CO+H2
CO+H2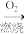 CO2+H2O
CO2+H2O途径b:CH4
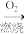 CO2+H2O
CO2+H2O(2)已知白磷(P4)和P4O6的分子结构和部分化学键的键能分别如下图、表所示:

| 化学键 | P-P | O=O | P-O |
| 键能(kJ·mol-1) | a | b | c |
②已知P4(白磷,s)=4P(红磷,s)ΔH=-16.7kJ·mol-1。白磷和红磷互为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。
(1)把煤作为燃料可通过下列两种途径:
途径I:C(s)+O2(g)=CO2(g) ΔH1<0 ①
途径II:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) ΔH2>0 ②
则途径I放出的热量___________ (填“大于”“等于”或“小于”)途径II放出的热量;ΔH1、ΔH2、ΔH3、ΔH4的数学关系式是___________ 。
(2)在25℃、101kPa下,2g甲醇完全燃料放热45.36kJ,写出甲醇燃烧热的热化学方程式___________ 。
(3)已知①CO(g)+ O2(g)=CO2(g) ∆H1=-283.0kJ/mol
O2(g)=CO2(g) ∆H1=-283.0kJ/mol
试计算④2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)的ΔH=___________ 。
(4)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:

反应I:2H2SO4(l)=2SO2(g)+2H2O(g) ∆H1=+551kJ/mol
反应Ⅲ:S(s)+O2(g)=SO2(g) ∆H3=-297kJ/mol
反应Ⅱ的热化学方程式:___________
(1)把煤作为燃料可通过下列两种途径:
途径I:C(s)+O2(g)=CO2(g) ΔH1<0 ①
途径II:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) ΔH2>0 ②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g) ΔH3<0 ③
2H2(g)+O2(g)=2H2O(g) ΔH4<0 ④
则途径I放出的热量
(2)在25℃、101kPa下,2g甲醇完全燃料放热45.36kJ,写出甲醇燃烧热的热化学方程式
(3)已知①CO(g)+
 O2(g)=CO2(g) ∆H1=-283.0kJ/mol
O2(g)=CO2(g) ∆H1=-283.0kJ/mol②H2(g)+ O2(g)=H2O(l) ΔH2=-285.8kJ/mol
O2(g)=H2O(l) ΔH2=-285.8kJ/mol
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH3=-1370kJ/mol
试计算④2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)的ΔH=
(4)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:

反应I:2H2SO4(l)=2SO2(g)+2H2O(g) ∆H1=+551kJ/mol
反应Ⅲ:S(s)+O2(g)=SO2(g) ∆H3=-297kJ/mol
反应Ⅱ的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】碳及其化合物在能源和材料方面具有广泛的用途,回答下列问题:
(1)已知CH4(g)+ O2(g)=CO(g)+2H2O(l)
O2(g)=CO(g)+2H2O(l) 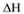 =-607.31kJ/mol
=-607.31kJ/mol
2CO(g)+ O2(g)=2CO2(g)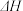 =-566.0kJ/mol
=-566.0kJ/mol
写出表示甲烷燃烧热的热化学方程式____________ 。
(2)天然气的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g) 2CO(g)+2H2(g) 。在密闭容器中通入物质的量浓度均为0.125mol/L的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示。则:
2CO(g)+2H2(g) 。在密闭容器中通入物质的量浓度均为0.125mol/L的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示。则:

①压强P1_____ P2(填 “>”或“<”);
②压强为P2时,在Y点:v(正)_______ v(逆)(填“>”、“<”或“=”)。
③求Y点对应温度下的该反应的平衡常数K=_________ 。(计算结果保留两位小数)
(3)CO可以合成二甲醚,2CO(g)+4H2(g) CH3OCH3(g)+H2O(g) △H<0,二甲醚可以作为燃料电池的原料。
CH3OCH3(g)+H2O(g) △H<0,二甲醚可以作为燃料电池的原料。
①写出二甲醚在KOH做电解质条件下的负极电极反应式_____________________ 。
②利用此燃料电池以石墨为电极电解1L,0.5mol/L的CuSO4溶液,导线通过1mol电子时,假设溶液体积不变,则所得溶液pH=_________ ,理论上消耗二甲醚________ g(保留小数点后两位)。
(1)已知CH4(g)+
 O2(g)=CO(g)+2H2O(l)
O2(g)=CO(g)+2H2O(l) 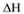 =-607.31kJ/mol
=-607.31kJ/mol2CO(g)+ O2(g)=2CO2(g)
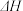 =-566.0kJ/mol
=-566.0kJ/mol写出表示甲烷燃烧热的热化学方程式
(2)天然气的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g)
 2CO(g)+2H2(g) 。在密闭容器中通入物质的量浓度均为0.125mol/L的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示。则:
2CO(g)+2H2(g) 。在密闭容器中通入物质的量浓度均为0.125mol/L的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示。则:
①压强P1
②压强为P2时,在Y点:v(正)
③求Y点对应温度下的该反应的平衡常数K=
(3)CO可以合成二甲醚,2CO(g)+4H2(g)
 CH3OCH3(g)+H2O(g) △H<0,二甲醚可以作为燃料电池的原料。
CH3OCH3(g)+H2O(g) △H<0,二甲醚可以作为燃料电池的原料。①写出二甲醚在KOH做电解质条件下的负极电极反应式
②利用此燃料电池以石墨为电极电解1L,0.5mol/L的CuSO4溶液,导线通过1mol电子时,假设溶液体积不变,则所得溶液pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据已知信息,按要求写出指定反应的热化学方程式
(1)LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g)=2LiH(s) ΔH=-182kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1
③4Li(s)+O2(g)=2Li2O(s) ΔH=-1196kJ·mol-1
试写出LiH在O2中燃烧的热化学方程式:____________ 。
(2)工业上制取硝酸铵的流程图如下所示:
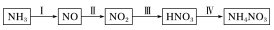
已知:4NO(g)+4NH3(g)+O2(g)⇌4N2(g)+6H2O(g) ΔH=-1745.2kJ·mol-1;
6NO(g)+4NH3(g)⇌5N2(g)+6H2O(g) ΔH=-1925.2kJ·mol-1。
则反应I的热化学方程式可表示为_______ 。
(3)饮用水中的 主要来自于
主要来自于 。已知在微生物的作用下,
。已知在微生物的作用下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
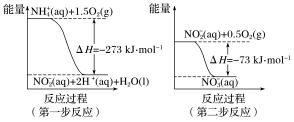
1mol 全部被氧化成
全部被氧化成 的热化学方程式为
的热化学方程式为_______ 。
(1)LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g)=2LiH(s) ΔH=-182kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1
③4Li(s)+O2(g)=2Li2O(s) ΔH=-1196kJ·mol-1
试写出LiH在O2中燃烧的热化学方程式:
(2)工业上制取硝酸铵的流程图如下所示:

已知:4NO(g)+4NH3(g)+O2(g)⇌4N2(g)+6H2O(g) ΔH=-1745.2kJ·mol-1;
6NO(g)+4NH3(g)⇌5N2(g)+6H2O(g) ΔH=-1925.2kJ·mol-1。
则反应I的热化学方程式可表示为
(3)饮用水中的
 主要来自于
主要来自于 。已知在微生物的作用下,
。已知在微生物的作用下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
1mol
 全部被氧化成
全部被氧化成 的热化学方程式为
的热化学方程式为
您最近一年使用:0次



