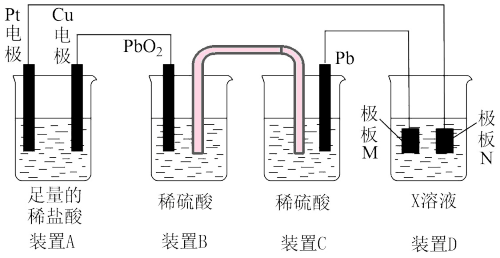
(1)催化硝化法和电化学降解法可用于治理水中硝酸盐的污染。
①催化硝化法中,用H2将NO3—还原为N2,一段时间后,溶液的碱性明显增强。则该反应离子方程式为____ 。
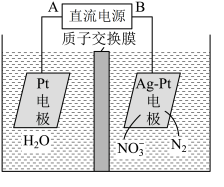
②电化学降解NO3—的原理如图所示,电源正极为________ (填“A”或 B”),若总反应4NO3-+4H+=5O2+2N2+2H2O,则阴极反应式为_______ 。
③能否把质子交换膜改为阴离子交换膜____________ (填“能“或”不能”)。
(2)研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
①CO与O2设计成燃料电池(以KOH溶液为电解液)。该电池的负极反应式为______ 。
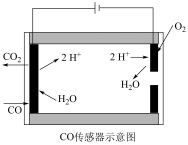
②测量汽车尾气中的CO浓度常用电化学气敏传感器,可用图简单表示,则阳极发生的电极反应为_____________________ 。
①催化硝化法中,用H2将NO3—还原为N2,一段时间后,溶液的碱性明显增强。则该反应离子方程式为
②电化学降解NO3—的原理如图所示,电源正极为
③能否把质子交换膜改为阴离子交换膜

(2)研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
①CO与O2设计成燃料电池(以KOH溶液为电解液)。该电池的负极反应式为
②测量汽车尾气中的CO浓度常用电化学气敏传感器,可用图简单表示,则阳极发生的电极反应为

更新时间:2019-11-21 15:11:16
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】含氮化合物在工农业生产中都有重要应用。
(1)氮和肼(N2H4)是两种最常见的氮氢化物。
已知:4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH1=-541.8 kJ·mol-1,化学平衡常数为K1。N2H4(g)+O2(g)
2N2(g)+6H2O(g) ΔH1=-541.8 kJ·mol-1,化学平衡常数为K1。N2H4(g)+O2(g) N2(g)+2H2O(g) ΔH2=-534 kJ·mol-1,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为
N2(g)+2H2O(g) ΔH2=-534 kJ·mol-1,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为__________________ ,该反应的化学平衡常数K=________ (用K1、K2表示)。
(2)对于2NO(g)+2CO(g) N2(g)+2CO2(g),在一定温度下,于1 L的恒容密闭容器中充入0.1 mol NO和0.3 mol CO,反应开始进行。
N2(g)+2CO2(g),在一定温度下,于1 L的恒容密闭容器中充入0.1 mol NO和0.3 mol CO,反应开始进行。
①下列能说明该反应已经达到平衡状态的是______ (填字母代号)。
A.c(CO)=c(CO2)
B.容器中混合气体的密度不变
C.v(N2)正=2v(NO)逆
D.容器中混合气体的平均摩尔质量不变
②图1为容器内的压强(p)与起始压强(p0)的比值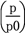 随时间(t)的变化曲线。0~5min内,该反应的平均反应速率v(N2)=
随时间(t)的变化曲线。0~5min内,该反应的平均反应速率v(N2)=________ ,平衡时NO的转化率为________ 。
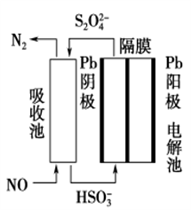
(3)使用间接电化学法可处理燃烧烟气中的NO,装置如图所示。已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:____________________ 。用离子方程式表示吸收池中除去NO的原理____________________________________________ 。
(1)氮和肼(N2H4)是两种最常见的氮氢化物。
已知:4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) ΔH1=-541.8 kJ·mol-1,化学平衡常数为K1。N2H4(g)+O2(g)
2N2(g)+6H2O(g) ΔH1=-541.8 kJ·mol-1,化学平衡常数为K1。N2H4(g)+O2(g) N2(g)+2H2O(g) ΔH2=-534 kJ·mol-1,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为
N2(g)+2H2O(g) ΔH2=-534 kJ·mol-1,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为(2)对于2NO(g)+2CO(g)
 N2(g)+2CO2(g),在一定温度下,于1 L的恒容密闭容器中充入0.1 mol NO和0.3 mol CO,反应开始进行。
N2(g)+2CO2(g),在一定温度下,于1 L的恒容密闭容器中充入0.1 mol NO和0.3 mol CO,反应开始进行。①下列能说明该反应已经达到平衡状态的是
A.c(CO)=c(CO2)
B.容器中混合气体的密度不变
C.v(N2)正=2v(NO)逆
D.容器中混合气体的平均摩尔质量不变
②图1为容器内的压强(p)与起始压强(p0)的比值
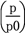 随时间(t)的变化曲线。0~5min内,该反应的平均反应速率v(N2)=
随时间(t)的变化曲线。0~5min内,该反应的平均反应速率v(N2)=
(3)使用间接电化学法可处理燃烧烟气中的NO,装置如图所示。已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入 和
和 ,电解质溶液为KOH溶液。某研究小组以甲烷燃料电池(装置甲)为电源,模拟氯碱工业生产原理,装置如图所示。
,电解质溶液为KOH溶液。某研究小组以甲烷燃料电池(装置甲)为电源,模拟氯碱工业生产原理,装置如图所示。
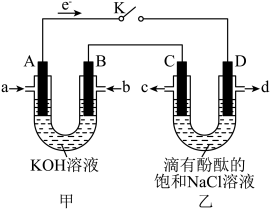
请回答以下问题:
(1)B、D的电极名称分别是___________ 、___________ 。
(2)C极可以选用的材料是___________(填标号)。
(3)该装置工作一段时间后,观察到C极和D极的不同现象是___________ 。
(4)气体b应为___________ (填“ ”或“
”或“ ”),A极发生的电极反应为
”),A极发生的电极反应为___________ 。
(5)装置甲、乙中的电解质溶液足量,当电路中通过0.4mol电子时,气体a、b的总物质的量与气体c、d的总物质的量之比为___________ 。
(6)若以装置甲为电源,要在铁器上镀铜,则铁器应连接___________ (填“A”或“B”)极。
 和
和 ,电解质溶液为KOH溶液。某研究小组以甲烷燃料电池(装置甲)为电源,模拟氯碱工业生产原理,装置如图所示。
,电解质溶液为KOH溶液。某研究小组以甲烷燃料电池(装置甲)为电源,模拟氯碱工业生产原理,装置如图所示。
请回答以下问题:
(1)B、D的电极名称分别是
(2)C极可以选用的材料是___________(填标号)。
| A.铁棒 | B.银棒 | C.石墨棒 | D.铜棒 |
(4)气体b应为
 ”或“
”或“ ”),A极发生的电极反应为
”),A极发生的电极反应为(5)装置甲、乙中的电解质溶液足量,当电路中通过0.4mol电子时,气体a、b的总物质的量与气体c、d的总物质的量之比为
(6)若以装置甲为电源,要在铁器上镀铜,则铁器应连接
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:
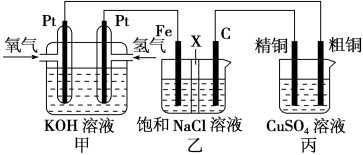
(1)石墨电极为______ (填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入”酚酞溶液,________ (填“铁极”或“石墨极”)区的溶液先变红。乙池中电解总反应化学方程式为_________ 。
(2)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,溶液中硫酸铜浓度将________ (填“增大”“减小”或“不变”)。精铜电极上的电极反应式为_________ 。
(3)若在标准状况下,有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下体积为________ mL;丙装置中阴极析出铜的质量为__________ g。
(4)若将甲改用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得燃料电池,则该电池负极反应式为______ ,正极反应式为_______ 。

(1)石墨电极为
(2)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,溶液中硫酸铜浓度将
(3)若在标准状况下,有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下体积为
(4)若将甲改用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得燃料电池,则该电池负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式:____________ 。
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为___________ ,NaH2PO2___________ (填“能”或“不能”)与NaOH反应。
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为________ (填化学式)。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式:____________________ 。
(4)H3PO2也可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
①写出阳极的电极反应式______________________________________________ 。
②分析产品室可得到H3PO2的原因______________________________________________ 。
(1)H3PO2是一元中强酸,写出其电离方程式:
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式:
(4)H3PO2也可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
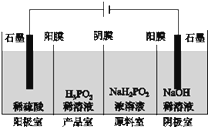
①写出阳极的电极反应式
②分析产品室可得到H3PO2的原因
您最近一年使用:0次