次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式:____________ 。
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为___________ ,NaH2PO2___________ (填“能”或“不能”)与NaOH反应。
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为________ (填化学式)。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式:____________________ 。
(4)H3PO2也可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
①写出阳极的电极反应式______________________________________________ 。
②分析产品室可得到H3PO2的原因______________________________________________ 。
(1)H3PO2是一元中强酸,写出其电离方程式:
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式:
(4)H3PO2也可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
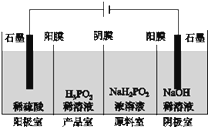
①写出阳极的电极反应式
②分析产品室可得到H3PO2的原因
更新时间:2018-10-23 19:57:21
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)化学与生产生活密切相关,请写出下列反应
①实验室制氯气_________________ (离子方程式)
②“腐蚀法”制作印刷电路板____________ (化学方程式)并用双线桥表示该反应的电子转移数目和方向
(2)K2FeO4可用作水处理剂,它可由以下反应制得:
____ Cl2 + ____ Fe(OH)3 + _____ OH- === ______ FeO4 2-+ _____ Cl- +____ H2O
配平此反应方程式。当1mol K2FeO4生成时,转移的电子数目为_____
①实验室制氯气
②“腐蚀法”制作印刷电路板
(2)K2FeO4可用作水处理剂,它可由以下反应制得:
配平此反应方程式。当1mol K2FeO4生成时,转移的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】二氧化氯(ClO2)气体也是一种常用的自来水消毒剂。
(1)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原氯酸钠,可较安全地生成ClO2,反应的离子方程式为___ 。
(2)自来水用ClO2处理后,有少量ClO2残留在水中,可用碘量法作如下检测(已知ClO2存在于pH为4~6的溶液中,ClO 存在于中性溶液中):
存在于中性溶液中):
①取0.50L水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,溶液变蓝。写出ClO2与碘化钾反应的化学方程式:___ 。
②已知:2Na2S2O3+I2=Na2S4O6+2NaI,向①所得溶液中滴加5.00×10-4mol·L-1的Na2S2O3溶液至恰好反应,消耗Na2S2O3溶液20.00mL,该水样中ClO2的浓度是___ mg·L-1。
(1)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原氯酸钠,可较安全地生成ClO2,反应的离子方程式为
(2)自来水用ClO2处理后,有少量ClO2残留在水中,可用碘量法作如下检测(已知ClO2存在于pH为4~6的溶液中,ClO
 存在于中性溶液中):
存在于中性溶液中):①取0.50L水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,溶液变蓝。写出ClO2与碘化钾反应的化学方程式:
②已知:2Na2S2O3+I2=Na2S4O6+2NaI,向①所得溶液中滴加5.00×10-4mol·L-1的Na2S2O3溶液至恰好反应,消耗Na2S2O3溶液20.00mL,该水样中ClO2的浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)根据元素周期律,碳的非金属性强于硅,请用一个化学反应方程式表示___________________ 。
(2)若FeSO4和O2的系数比为2∶1,试配平下列方程式:
 FeSO4+
FeSO4+ K2O2→
K2O2→ K2FeO4+
K2FeO4+ K2O+
K2O+ K2SO4+
K2SO4+ O2↑
O2↑ __________________
(3)各种氮氧化物(NO、NO2)是主要的大气污染物之一,治理氮氧化物(NOx)废气的方法之一是用NaOH溶液进行吸收,现有NO与NO2的混合气体,将其通入50 mL 2 mol/L的NaOH溶液中,恰好完全吸收,测得溶液中含有NO3- 0.02 mol。
①所得溶液中NaNO2的物质的量为________ mol;
②混合气体中V(NO)∶V(NO2)=________ 。
(4)As2O3俗称砒霜,As2O3是两性偏酸性氧化物,是亚砷酸(H3AsO3)的酸酐,易溶于碱生成亚砷酸盐,写出As2O3与足量氢氧化钠溶液反应的离子方程式___________ 。
(2)若FeSO4和O2的系数比为2∶1,试配平下列方程式:
 FeSO4+
FeSO4+ K2O2→
K2O2→ K2FeO4+
K2FeO4+ K2O+
K2O+ K2SO4+
K2SO4+ O2↑
O2↑ (3)各种氮氧化物(NO、NO2)是主要的大气污染物之一,治理氮氧化物(NOx)废气的方法之一是用NaOH溶液进行吸收,现有NO与NO2的混合气体,将其通入50 mL 2 mol/L的NaOH溶液中,恰好完全吸收,测得溶液中含有NO3- 0.02 mol。
①所得溶液中NaNO2的物质的量为
②混合气体中V(NO)∶V(NO2)=
(4)As2O3俗称砒霜,As2O3是两性偏酸性氧化物,是亚砷酸(H3AsO3)的酸酐,易溶于碱生成亚砷酸盐,写出As2O3与足量氢氧化钠溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】NaOH溶液可用于多种气体的处理。
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3。
①Na2CO3俗称纯碱,因CO 水解而使其水溶液呈碱性,写出CO
水解而使其水溶液呈碱性,写出CO 第一步水解的离子方程式
第一步水解的离子方程式______ 。已知25℃时,CO 第一步水解的平衡常数Kh=2×10﹣4mol/L,当溶液中c(HCO
第一步水解的平衡常数Kh=2×10﹣4mol/L,当溶液中c(HCO ):c(CO
):c(CO )=20:1 时,溶液的pH=
)=20:1 时,溶液的pH=______ 。
②泡沫灭火器中通常装有NaHCO溶液和Al2(SO4)3溶液,请写出这两种溶液混合时的离子反应方程式______ 。
(2)金属与浓硝酸反应产生的NO2可用NaOH溶液吸收,反应方程式为:2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.lmol•L﹣1CH3COONa溶液,则两份溶液中c(NO )、c(NO
)、c(NO )和c(CH3COO﹣)由大到小的顺序为
)和c(CH3COO﹣)由大到小的顺序为______ (已知HNO2的电离常数Ka=7.1×10﹣4mol•L﹣1,CH3COOH的电离常数Ka=1.7×10﹣5mol•L﹣1)。可使溶液A和溶液 B的 pH相等的方法是______ 。
A.向溶液A中加适量NaOH B.向溶液A中加适量水
C.向溶液B中加适量NaOH D.向溶液B中加适量水
(3)烟气中的SO2会引起酸雨,可利用氢氧化钠溶液吸收吸收SO2的过裎中,溶液中H2SO3、HSO 、SO
、SO 三者所占物质的量分数(a)随pH变化的关系如图所示:
三者所占物质的量分数(a)随pH变化的关系如图所示:
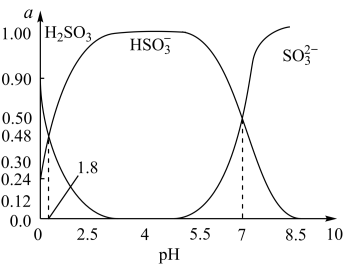
图中pH=7时,溶液中离子浓度关系正确的是______ 。
A.c(Na+)>2c(SO )>c(HSO
)>c(HSO )
)
B.c(Na+)=c(SO )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)
C.c(OH﹣)=c(H+)+c(H2SO3)+c(HSO )
)
D.c(Na+)>c(HSO )>c(SO
)>c(SO )>c(H+)=c(OH﹣)
)>c(H+)=c(OH﹣)
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3。
①Na2CO3俗称纯碱,因CO
 水解而使其水溶液呈碱性,写出CO
水解而使其水溶液呈碱性,写出CO 第一步水解的离子方程式
第一步水解的离子方程式 第一步水解的平衡常数Kh=2×10﹣4mol/L,当溶液中c(HCO
第一步水解的平衡常数Kh=2×10﹣4mol/L,当溶液中c(HCO ):c(CO
):c(CO )=20:1 时,溶液的pH=
)=20:1 时,溶液的pH=②泡沫灭火器中通常装有NaHCO溶液和Al2(SO4)3溶液,请写出这两种溶液混合时的离子反应方程式
(2)金属与浓硝酸反应产生的NO2可用NaOH溶液吸收,反应方程式为:2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.lmol•L﹣1CH3COONa溶液,则两份溶液中c(NO
 )、c(NO
)、c(NO )和c(CH3COO﹣)由大到小的顺序为
)和c(CH3COO﹣)由大到小的顺序为A.向溶液A中加适量NaOH B.向溶液A中加适量水
C.向溶液B中加适量NaOH D.向溶液B中加适量水
(3)烟气中的SO2会引起酸雨,可利用氢氧化钠溶液吸收吸收SO2的过裎中,溶液中H2SO3、HSO
 、SO
、SO 三者所占物质的量分数(a)随pH变化的关系如图所示:
三者所占物质的量分数(a)随pH变化的关系如图所示:
图中pH=7时,溶液中离子浓度关系正确的是
A.c(Na+)>2c(SO
 )>c(HSO
)>c(HSO )
)B.c(Na+)=c(SO
 )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)C.c(OH﹣)=c(H+)+c(H2SO3)+c(HSO
 )
)D.c(Na+)>c(HSO
 )>c(SO
)>c(SO )>c(H+)=c(OH﹣)
)>c(H+)=c(OH﹣)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.布朗斯特(Brönsted)和劳莱(Lowry)的质子理论认为,凡是给出质子(H+)的任何物质(分子或离子)都是酸;凡是接受质子(H+)的任何物质都是碱。简单地说,酸是质子的给予体,而碱是质子的接受体。酸和碱之间的关系表示如:酸 质子(H+)+ 碱
质子(H+)+ 碱
(1)根据酸碱质子理论,既能看成酸又能看成碱的是_____________ 。(均填序号)
① ②HS- ③
②HS- ③ ④H2O ⑤H3O+ ⑥Na+
④H2O ⑤H3O+ ⑥Na+
(2)已知反应C6H5OH + =C6H5O - +
=C6H5O - + ,则C6H5O – 和
,则C6H5O – 和 -碱性较强的是
-碱性较强的是__________ 。
Ⅱ.(3)水的离子积常数为Kw ,弱酸HA的电离平衡常数为Ka,NaA的溶液中A-的水解平衡常数为Kh ,根据它们的平衡常数表达式判断,Ka与Kh的关系为__________________ 。
(4)已知常温下弱酸HA的电离平衡常数为K=1.75× 10-5,常温下向0.2mol/L的HA的溶液中加入等体积0.1mol/L的NaOH溶液,该溶液pH值___ 7(填“>”或 “=”或 “<”),该溶液粒子浓度关系正确的是____ 。
A.2c(Na+)> c(HA)+c(A-)
B.c(A-)—c(HA)=2[c(H+)—c(OH-)]
C.c(A-)> c(Na+)> c(HA)> c(H+)>c(OH-)
D.c(Na+)>c(A-)> c(HA)>c(H+)> c(OH-)
 质子(H+)+ 碱
质子(H+)+ 碱(1)根据酸碱质子理论,既能看成酸又能看成碱的是
①
 ②HS- ③
②HS- ③ ④H2O ⑤H3O+ ⑥Na+
④H2O ⑤H3O+ ⑥Na+(2)已知反应C6H5OH +
 =C6H5O - +
=C6H5O - + ,则C6H5O – 和
,则C6H5O – 和 -碱性较强的是
-碱性较强的是Ⅱ.(3)水的离子积常数为Kw ,弱酸HA的电离平衡常数为Ka,NaA的溶液中A-的水解平衡常数为Kh ,根据它们的平衡常数表达式判断,Ka与Kh的关系为
(4)已知常温下弱酸HA的电离平衡常数为K=1.75× 10-5,常温下向0.2mol/L的HA的溶液中加入等体积0.1mol/L的NaOH溶液,该溶液pH值
A.2c(Na+)> c(HA)+c(A-)
B.c(A-)—c(HA)=2[c(H+)—c(OH-)]
C.c(A-)> c(Na+)> c(HA)> c(H+)>c(OH-)
D.c(Na+)>c(A-)> c(HA)>c(H+)> c(OH-)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)0.020 mol·L−1的HCN(aq)与0.020 mol·L−1 NaCN(aq)等体积混合,已知该混合溶液中c(Na+)>c(CN−),用“>”“<”“=”符号填空。
①溶液中c(OH−)________ c(H+)。
②溶液中c(HCN)________ c(CN−)。
(2)已知某溶液中存在OH−、H+、NH4+、Cl−四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
A.c(Cl−)>c(NH4+)>c(H+)>c(OH−)
B.c(Cl−)>c(NH4+)>c(OH−)>c(H+)
C.c(NH4+)>c(Cl−)>c(OH−)>c(H+)
D.c(Cl−)>c(H+)>c(NH4+)>c(OH−)
填写下列空白:
①若溶液中只溶解了一种溶质,则该溶质是__________________________ ,上述四种离子浓度的大小顺序为________ (填序号)。
②若上述关系中C是正确的,则溶液中的溶质为__________________ ;若上述关系中D是正确的,则溶液中的溶质为____________________ 。
③若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)________ c(NH3·H2O)(填“大于”“小于”或“等于”,下同),混合前酸中c(H+)和碱中c(OH−)的关系为c(H+)________ c(OH−)。
①溶液中c(OH−)
②溶液中c(HCN)
(2)已知某溶液中存在OH−、H+、NH4+、Cl−四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
A.c(Cl−)>c(NH4+)>c(H+)>c(OH−)
B.c(Cl−)>c(NH4+)>c(OH−)>c(H+)
C.c(NH4+)>c(Cl−)>c(OH−)>c(H+)
D.c(Cl−)>c(H+)>c(NH4+)>c(OH−)
填写下列空白:
①若溶液中只溶解了一种溶质,则该溶质是
②若上述关系中C是正确的,则溶液中的溶质为
③若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某学习小组为研究电化学原理,设计如图装置。请回答下列问题:
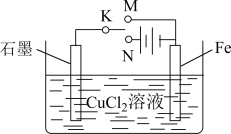
(1)若K与M、N均断开,发生的离子反应为____________________ 。
(2)若K与M相连、与N断开,石墨为_________ (填电极名称)。
(3)若K与N相连、与M断开,石墨电极处的现象为____________________ 。
(4)若将CuCl2溶液换成精制饱和食盐水,仍保持K与N相连、与M断开,此时装置中发生的离子反应方程式为_______________________________ 。若此反应过程中转移1mol电子,理论上共产生标准状况下气体__________________ L。

(1)若K与M、N均断开,发生的离子反应为
(2)若K与M相连、与N断开,石墨为
(3)若K与N相连、与M断开,石墨电极处的现象为
(4)若将CuCl2溶液换成精制饱和食盐水,仍保持K与N相连、与M断开,此时装置中发生的离子反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】碳及其化合物在生活、化工领域发挥着重要的作用。试回答下列问题:
(1)有科学家提出由CO2制取C的太阳能工艺如图所示。若重整系统发生的反应中 ,则重整系统中发生反应的化学方程式为
,则重整系统中发生反应的化学方程式为______________ 。

(2)以CO2为原料利用电解法可制取乙烯,其装置如图所示。电极a为电源的_____ (填正极”或“负极” ),溶液中的H+由_______ (填“阴”或“阳”,下同)极区流向____ 极区。

(3)草酸锌可应用于有机合成、电子工业等。工业上制取ZnC2O4的原理如图所示(电解液不参加反应),Zn电极是________ (填“正” “负”“阴”或“阳”)极。已知在Pb电极区得到ZnC2O4,则Pb电极上的电极反应式为_________________ 。
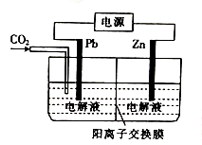
(1)有科学家提出由CO2制取C的太阳能工艺如图所示。若重整系统发生的反应中
 ,则重整系统中发生反应的化学方程式为
,则重整系统中发生反应的化学方程式为
(2)以CO2为原料利用电解法可制取乙烯,其装置如图所示。电极a为电源的

(3)草酸锌可应用于有机合成、电子工业等。工业上制取ZnC2O4的原理如图所示(电解液不参加反应),Zn电极是

您最近一年使用:0次
【推荐3】回答下列问题:
(1)有一种燃料电池,所用燃料为 和空气,电解质为熔融的
和空气,电解质为熔融的 。回答下列问题
。回答下列问题
① 移向
移向_______ 极。
②正极反应式为_______ 。
③电池中 的物质的量将逐渐
的物质的量将逐渐_______ (填增大、减少、不变)。
(2)用上面的电池对下物质进行电解,其中a、b、c、d、e、f电极均为惰性电极,通电后,a极产生的气体明显多于b极,2分钟后,测得乙池的pH为12,则
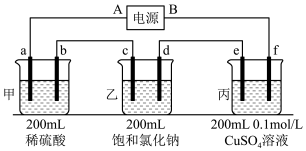
①电源A极是_______ 极。
②c极上的电极反应式:_______ 。
③甲、乙两池共可收集到_______ mol气体。
(1)有一种燃料电池,所用燃料为
 和空气,电解质为熔融的
和空气,电解质为熔融的 。回答下列问题
。回答下列问题①
 移向
移向②正极反应式为
③电池中
 的物质的量将逐渐
的物质的量将逐渐(2)用上面的电池对下物质进行电解,其中a、b、c、d、e、f电极均为惰性电极,通电后,a极产生的气体明显多于b极,2分钟后,测得乙池的pH为12,则

①电源A极是
②c极上的电极反应式:
③甲、乙两池共可收集到
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请用学过的化学知识对下面实验进行分析。

(1)图甲所示实验过程中,铜电极发生反应的电极反应式为______ 。银电极上发生______ (填“氧化”、“还原”)反应。
(2)图乙所示实验过程中b试管的现象是_____________________________ 。
(3)图丙所示实验过程中c 为电源的_____ 极。溶液中滴加酚酞溶液,则____ 极区(填“石墨”、“铁棒”)溶液变红。

(1)图甲所示实验过程中,铜电极发生反应的电极反应式为
(2)图乙所示实验过程中b试管的现象是
(3)图丙所示实验过程中c 为电源的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】H3PO2也可用电渗析法制备。“四室电渗析法”工作原理如下图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
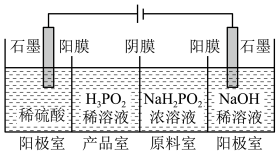
(1)写出阳极的电极反应式____________________________ 。
(2)分析产品室可得到H3PO2的原因________________________________________________________ 。
(3)早期采用“三室电渗析法”制备H3PO2:将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替。并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室。其缺点是产品中混有________ 杂质。该杂质产生的原因是___________________________________________ 。

(1)写出阳极的电极反应式
(2)分析产品室可得到H3PO2的原因
(3)早期采用“三室电渗析法”制备H3PO2:将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替。并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室。其缺点是产品中混有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)以甲烷、空气、氢氧化钾溶液为原料,石墨为电极可以构成燃料电池。该电池的负极反应式为___________________________________________ 。
(2)用如图所示装置进行电解①若A、B均为石墨电极,C为足量CuSO4溶液,则电解的总反应方程式为___________________________________________ 。
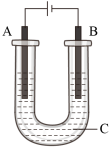
电解一段时间后,取出电极,向电解液中加入适量的___ (填化学式)可使C溶液恢复到电解前的成分和浓度。
②若A、B均为铂电极,C为Na2SO4溶液(含酚酞),电解一段时间后,___ (填“A”或“B”)极附近显红色;将电极取出,搅拌使溶液混合均匀,测得溶液的pH ____ 7(填“<”、“=”或“>”)。
③若A、B为同一材料的电极,C为CuCl2溶液,电解过程中CuCl2溶液的浓度始终 保持不变,则A、B为___ (填化学式)电极;当电路中有0.04 mol电子通过时,阴极增重___ g。
(2)用如图所示装置进行电解①若A、B均为石墨电极,C为足量CuSO4溶液,则电解的总反应方程式为

电解一段时间后,取出电极,向电解液中加入适量的
②若A、B均为铂电极,C为Na2SO4溶液(含酚酞),电解一段时间后,
③若A、B为同一材料的电极,C为CuCl2溶液,电解过程中CuCl2溶液的浓度始终 保持不变,则A、B为
您最近一年使用:0次



