已知① 银白色固体A,放在空气中可氧化成白色固体B;
②将A点燃,火焰呈黄色,生成淡黄色固体C;
③A、B、C三种物质都能跟无色液体D反应,生成碱性物质E,其中A跟D反应时还可生成可燃性气体F,C跟D反应时则生成另一种气体G;
④F和G混合后遇火可剧烈反应而发生爆炸,并生成D。
⑤H是黄绿色气体。
完成下列问题:
(1)B的名称______ ,B与D的反应类型属于______________________ 。
(2)写出下列 反应的化学方式:
A→C:__________________________________ 。
A→E:_________________________________ 。
C→E:__________________________________ 。
(3)H气体通入E溶液的离子方程式:______________________________ 。
②将A点燃,火焰呈黄色,生成淡黄色固体C;
③A、B、C三种物质都能跟无色液体D反应,生成碱性物质E,其中A跟D反应时还可生成可燃性气体F,C跟D反应时则生成另一种气体G;
④F和G混合后遇火可剧烈反应而发生爆炸,并生成D。
⑤H是黄绿色气体。
完成下列问题:
(1)B的名称
(2)写出下列 反应的化学方式:
A→C:
A→E:
C→E:
(3)H气体通入E溶液的离子方程式:
更新时间:2019-11-29 13:22:05
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E各物质的关系如下图所示:

已知:X能使湿润的红色石蕊试纸变蓝。
(1)无色液体A是_____ ,A与B反应的化学方程式是____________ 。
(2)由X转化为N2的化学方程式为______________ 。
(3)白色固体C的化学式为_____ 。由D转化为E的离子方程式为___ 。

已知:X能使湿润的红色石蕊试纸变蓝。
(1)无色液体A是
(2)由X转化为N2的化学方程式为
(3)白色固体C的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】i.下列几种物质:①NaHCO3晶体;②Na2O2;③NaHSO4溶液;④CO2;⑤NaOH溶液;⑥CH3CH2OH (酒精)。
(1)上述各物质属于电解质的是___________ (填物质编号,下同);属于非电解质的是___________ 。
(2)③中盐的电离方程式为___________ 。
(3)写出过量④通入⑤中反应的离子方程式:___________ 。
ii.有一包固体粉末,其中可能含有NaCl、Ba(NO3)2、K2SO4、Na2CO3、NaNO3中的一种或几种,现做以下实验:
①取部分固体粉末加入水中,振荡,有白色沉淀生成;
②向①的沉淀物中加入足量稀盐酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入硝酸银溶液,有白色沉淀产生。
(4)试根据上述实验事实可知:原固体粉末中一定含有的物质是___________ (写化学式,下同),可能含有的物质是___________ 。
(5)写出上述步骤②中发生反应的离子方程式:___________ 。
(1)上述各物质属于电解质的是
(2)③中盐的电离方程式为
(3)写出过量④通入⑤中反应的离子方程式:
ii.有一包固体粉末,其中可能含有NaCl、Ba(NO3)2、K2SO4、Na2CO3、NaNO3中的一种或几种,现做以下实验:
①取部分固体粉末加入水中,振荡,有白色沉淀生成;
②向①的沉淀物中加入足量稀盐酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入硝酸银溶液,有白色沉淀产生。
(4)试根据上述实验事实可知:原固体粉末中一定含有的物质是
(5)写出上述步骤②中发生反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。请回答下列问题:

(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B。则B的化学式为__ 。
(2)若D是氯碱工业的主要产品之一,B有两性,则反应②的离子方程式是__ 。
(3)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为___ 。
(4)若A的焰色反应呈黄色,D为二氧化碳,则反应②的离子方程式是___ 。

(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B。则B的化学式为
(2)若D是氯碱工业的主要产品之一,B有两性,则反应②的离子方程式是
(3)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为
(4)若A的焰色反应呈黄色,D为二氧化碳,则反应②的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】图中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色试验均为黄色。

(1)写出下列物质的化学式:B_______ ;D_______ ;E_______ 。
(2)写出B→D反应的化学方程式:_______ ;
(3)写出A→C的离子方程式:_______ 。
(4)加热6.00 g D和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31 g,则原混合物中D的质量为_______ 。

(1)写出下列物质的化学式:B
(2)写出B→D反应的化学方程式:
(3)写出A→C的离子方程式:
(4)加热6.00 g D和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31 g,则原混合物中D的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】由短周期元素组成的中学常见的含钠元素的物质A、B、C、D,存在如图转化关系(部分生成物和反应条件已略去)。
(1)若A为金属钠,则E为_______ ,A与水反应的离子方程式为_______ 。
(2)若A为过氧化钠,则E为_______ ,A与水反应的化学方程式为_______ 。
(3)A不论是Na还是Na2O2,依据转化关系判断物质D是_______ 。
(4)写出侯氏制碱法中两个重要的化学方程式_______ ;_______ ;
(5)下列鉴别C和D的方案中,合理的是_______ ;
①取等量的溶液于两支试管中,逐滴加入稀盐酸,开始就有气体放出的是Na2CO3
②取等量的溶液于两支试管中,加热,有气泡产生的是NaHCO3
③取等量的溶液于两支试管中,滴加BaCl2溶液,生成白色沉淀的是Na2CO3
④取等量的溶液于两支试管中,滴加Ba(OH)2溶液,生成白色沉淀的是Na2CO3

(1)若A为金属钠,则E为
(2)若A为过氧化钠,则E为
(3)A不论是Na还是Na2O2,依据转化关系判断物质D是
(4)写出侯氏制碱法中两个重要的化学方程式
(5)下列鉴别C和D的方案中,合理的是
①取等量的溶液于两支试管中,逐滴加入稀盐酸,开始就有气体放出的是Na2CO3
②取等量的溶液于两支试管中,加热,有气泡产生的是NaHCO3
③取等量的溶液于两支试管中,滴加BaCl2溶液,生成白色沉淀的是Na2CO3
④取等量的溶液于两支试管中,滴加Ba(OH)2溶液,生成白色沉淀的是Na2CO3
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,M为红褐色。

(1)写出A的电子式____ ,写出肼(N2H4)的电子式____ ,写出HClO的结构式____ 。
(2)请写出A与水反应的离子方程式:____ 。
(3)检验E溶液中含有Fe2+而不含有Fe3+的方法:____ 。
(4)写出H转化为M的化学方程式_____ 。
(5)写出D和足量稀硝酸反应(稀硝酸具有强氧化性,可将+2价铁氧化为+3价铁,自身被还原为NO)的离子方程式_____ 。
(6)往NaRO2溶液中通入少量CO2气体,写出发生反应的离子方程式____ 。

(1)写出A的电子式
(2)请写出A与水反应的离子方程式:
(3)检验E溶液中含有Fe2+而不含有Fe3+的方法:
(4)写出H转化为M的化学方程式
(5)写出D和足量稀硝酸反应(稀硝酸具有强氧化性,可将+2价铁氧化为+3价铁,自身被还原为NO)的离子方程式
(6)往NaRO2溶液中通入少量CO2气体,写出发生反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
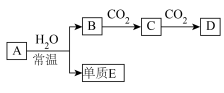
【推荐1】已知B是常见金属单质,E为常见非金属单质,H常温下为无色液体,C的浓溶液在加热时才与D反应。根据下列框图所示,试回答: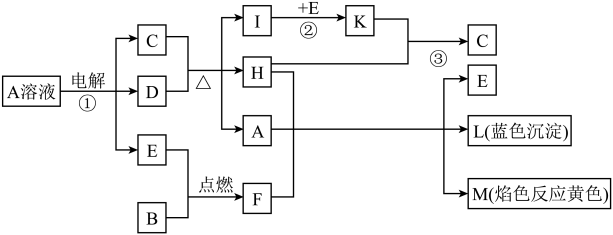
(1)写出化学式:A_______ ; E_______ ; L_______
(2)反应①的离子方程式:_______
(3)反应②,工业上采取的反应条件是_______
(4)反应③,工业上采取的操作不是K直接与H反应,原因是_______

(1)写出化学式:A
(2)反应①的离子方程式:
(3)反应②,工业上采取的反应条件是
(4)反应③,工业上采取的操作不是K直接与H反应,原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间能发生如图反应。(图中有些反应的产物和反应条件没有标出)
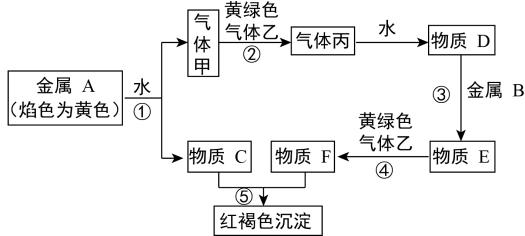
请回答下列问题:
(1)丙的化学式为________
(2)A的一种氧化物为淡黄色固体,该物质的化学式为________
(3)写出气体乙与C溶液反应的化学方程式:________________
(4)写出A与水反应的化学方程式:________________

请回答下列问题:
(1)丙的化学式为
(2)A的一种氧化物为淡黄色固体,该物质的化学式为
(3)写出气体乙与C溶液反应的化学方程式:
(4)写出A与水反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】草酸铁晶体Fe2(C2O4)3·xH2O通过相关处理后可溶于水,且能做净水剂,在110℃可完全失去结晶水。为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:
步骤1:称量4.66g草酸铁晶体进行处理后,配制成250 mL一定物质的量浓度的溶液。
步骤2:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根
恰好全部氧化成二氧化碳,同时 被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至溶液黄色刚好消失,过滤、洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至溶液黄色刚好消失,过滤、洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
步骤3:用0.0200 mol·L-1KMnO4溶液滴定步骤2所得溶液至终点,消耗KMnO4溶液V1 mL,滴定中 被还原成Mn2+。
被还原成Mn2+。
重复步骤2、步骤3的操作2次,分别滴定消耗0.0200 mol·L-1 KMnO4溶液为V2、V3 mL。
记录数据如下表:
请回答下列问题:
(1)草酸铁溶液能做净水剂的原因_________________ (用离子方程式表示)
(2)该实验步骤1和步骤3中使用的仪器除托盘天平、铁架台、滴定管夹、烧杯、玻璃棒外,一定需用下列仪器中的______________ (填序号)
A.酸式滴定管 B.碱式滴定管 C.量筒(10 mL) D.锥形瓶
E.胶头滴管 F.漏斗 G.250 mL容量瓶
(3)加入锌粉的目的是______________________
(4)步骤3滴定时是否选择指示剂_________ (是或否);说明理由_________________________ 写出步骤3中发生反应的离子方程式____________________________
(5)在步骤2中,若加入的KMnO4溶液的量不够,则测得的铁含量________ (填“偏低”、“偏高”或“不变”);实验测得该晶体中结晶水的个数x为________ 。
步骤1:称量4.66g草酸铁晶体进行处理后,配制成250 mL一定物质的量浓度的溶液。
步骤2:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根
恰好全部氧化成二氧化碳,同时
 被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至溶液黄色刚好消失,过滤、洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至溶液黄色刚好消失,过滤、洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。步骤3:用0.0200 mol·L-1KMnO4溶液滴定步骤2所得溶液至终点,消耗KMnO4溶液V1 mL,滴定中
 被还原成Mn2+。
被还原成Mn2+。重复步骤2、步骤3的操作2次,分别滴定消耗0.0200 mol·L-1 KMnO4溶液为V2、V3 mL。
记录数据如下表:
实验编号 | KMnO4溶液的浓度(mol·L-1) | KMnO4溶液滴入的体积(mL) |
1 | 0.0200 | V1 = 20.02 |
2 | 0.0200 | V2 = 20.12 |
3 | 0.0200 | V3 = 19.98 |
(1)草酸铁溶液能做净水剂的原因
(2)该实验步骤1和步骤3中使用的仪器除托盘天平、铁架台、滴定管夹、烧杯、玻璃棒外,一定需用下列仪器中的
A.酸式滴定管 B.碱式滴定管 C.量筒(10 mL) D.锥形瓶
E.胶头滴管 F.漏斗 G.250 mL容量瓶
(3)加入锌粉的目的是
(4)步骤3滴定时是否选择指示剂
(5)在步骤2中,若加入的KMnO4溶液的量不够,则测得的铁含量
您最近一年使用:0次



