某废液中含有 大量 的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO42-。某研究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴,(Br2常温下是深红棕色液体),设计了如下的流程图:
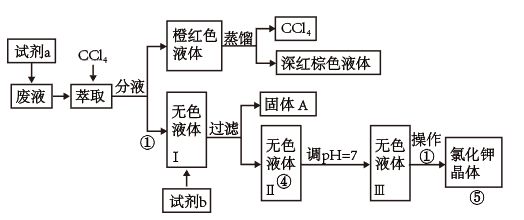
可供选择的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2溶液(H+)、KMnO4溶液(H+)、盐酸。请根据流程图回答相关问题 :
(1)若试剂a为H2O2溶液(H+),已知H2O2+2KBr+2HCl=Br2+2H2O+2KCl,
①发生反应的离子方程式为:___________ 。
②每消耗0.2mol H2O2,反应转移的电子数为_______ mol。
③还原剂和还原产物的物质的量之比是_____________ 。
(2)操作①②③④⑤对应的名称分别是:萃取、_________ 、蒸馏、过滤、__________ 。蒸馏过程用到下图装置的名称是A____________ B____________ 。

(3)为了除去无色液体中的Ca2+、Mg2+、SO42-,从可供选则试剂中选择试剂b所代表的物质,按照滴加的顺序依次是_______ 、_________ 、_________ (填化学式)。
(4)调节pH=7是为了除去杂质离子_______ 和________ ,以提高氯化钾晶体的纯度。

可供选择的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2溶液(H+)、KMnO4溶液(H+)、盐酸。请根据流程图回答相关问题 :
(1)若试剂a为H2O2溶液(H+),已知H2O2+2KBr+2HCl=Br2+2H2O+2KCl,
①发生反应的离子方程式为:
②每消耗0.2mol H2O2,反应转移的电子数为
③还原剂和还原产物的物质的量之比是
(2)操作①②③④⑤对应的名称分别是:萃取、

(3)为了除去无色液体中的Ca2+、Mg2+、SO42-,从可供选则试剂中选择试剂b所代表的物质,按照滴加的顺序依次是
(4)调节pH=7是为了除去杂质离子
更新时间:2019-12-04 15:46:08
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有含NaCl、Na2SO4和NaNO3的混合溶液,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液。相应过程用如图表示:
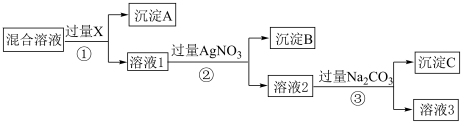
(1)写出下列物质的化学式X___________ ,B的化学式是___________ 。
(2)判断步骤②中AgNO3已过量的方法是___________ 。
(3)沉淀C的主要成分是___________ (填化学式)。
(4)按此实验方案得到的溶液3中肯定含有杂质,为了解决这个问题,可以向溶液3中加入适量的___________ (填试剂名称)。

(1)写出下列物质的化学式X
(2)判断步骤②中AgNO3已过量的方法是
(3)沉淀C的主要成分是
(4)按此实验方案得到的溶液3中肯定含有杂质,为了解决这个问题,可以向溶液3中加入适量的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。

请回答下列问题:
(1)请列举海水淡化的一种方法__________________________ 。
(2)步骤I中,粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是______ (填字母)。
A.①②③④ B.②③④① C.②④③① D.③④②①
(3)在实验室中可以用萃取的方法提取溴,可选用的试剂是________________ ,所用主要仪器的名称是____________________ 。
(4)步骤I已经获得Br2,步骤II又将Br2还原为Br—,其目的是_____________________
(5)写出步骤III反应的离子方程式__________________________________________ 。

请回答下列问题:
(1)请列举海水淡化的一种方法
(2)步骤I中,粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是
A.①②③④ B.②③④① C.②④③① D.③④②①
(3)在实验室中可以用萃取的方法提取溴,可选用的试剂是
(4)步骤I已经获得Br2,步骤II又将Br2还原为Br—,其目的是
(5)写出步骤III反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为了将混有K2SO4、MgSO4的KNO3固体提纯,并制得纯净的KNO3溶液,某同学设计如下实验方案:
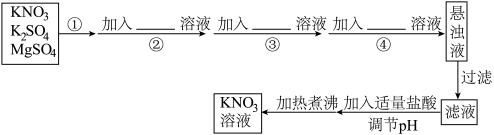
(1)操作①为________ 。
(2)操作②~④加入的试剂可以为________ 。
(3)如何判断 已除尽,简述实验操作
已除尽,简述实验操作________________________ 。
(4)实验过程中产生的多次沉淀________ (填“需要”或“不需要”)多次过滤,理由是_____________ 。
(5)该同学设计的实验方案________ (填“合理”或“不合理”),理由是____________________________ 。

(1)操作①为
(2)操作②~④加入的试剂可以为
(3)如何判断
 已除尽,简述实验操作
已除尽,简述实验操作(4)实验过程中产生的多次沉淀
(5)该同学设计的实验方案
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】草酸亚铁晶体(FeC2O4·2H2O)是实验室常用的分析试剂,可通过硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O,易氧化]与草酸反应制得。制备并测定其组成设计实验如下。
Ⅰ.硫酸铵和硫酸亚铁混合结晶制备硫酸亚铁铵。
(1)操作(ⅰ)为______ 。
(2)操作(ⅳ)产生H2,赶出装置内的空气的目的为______ a、b止水夹“操作2”为______
(3)仪器甲的名称为______ 。该装置中存在一处缺陷为______
(4)写出装置C中发生反应的化学方程式____________ 。
Ⅱ.制备草酸亚铁晶体并测定其组成。
将制得的硫酸亚铁铵与草酸一定条件下混合加热,经沉淀,抽滤、洗涤获得草酸亚铁晶体
粗品。该草酸亚铁晶体(FeC2O4·2H2O)粗品中可能含有的杂质为Fe2(C2O4)3、H2C2O4·2H2O,采用KMnO4溶液滴定法测定该粗品的组成,实验过程如图。已知草酸为弱酸,可被KMnO4溶液氧化为CO2,回答下列问题。____________ 。
(6)样品中所含H2C2O4·2H2O(摩尔质量为M g/mol)的质量分数表达式为____________ 。
Ⅰ.硫酸铵和硫酸亚铁混合结晶制备硫酸亚铁铵。
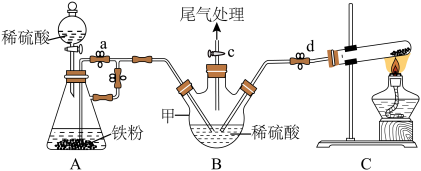
(1)操作(ⅰ)为
(2)操作(ⅳ)产生H2,赶出装置内的空气的目的为
(3)仪器甲的名称为
(4)写出装置C中发生反应的化学方程式
Ⅱ.制备草酸亚铁晶体并测定其组成。
将制得的硫酸亚铁铵与草酸一定条件下混合加热,经沉淀,抽滤、洗涤获得草酸亚铁晶体
粗品。该草酸亚铁晶体(FeC2O4·2H2O)粗品中可能含有的杂质为Fe2(C2O4)3、H2C2O4·2H2O,采用KMnO4溶液滴定法测定该粗品的组成,实验过程如图。已知草酸为弱酸,可被KMnO4溶液氧化为CO2,回答下列问题。

(6)样品中所含H2C2O4·2H2O(摩尔质量为M g/mol)的质量分数表达式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】下面是某学习小组对乙二酸的某些性质进行研究性学习的过程:
【研究课题】探究乙二酸的某些性质
【查阅资料】乙二酸(HOOC-COOH)俗称草酸,其主要物理常数如下:
又知草酸在100℃时开始升华,157℃时大量升华,并开始分解。草酸钙不溶于水。根据上述材料提供的信息,回答下列问题:
【提出猜想】
[猜想一]根据草酸晶体的组成对其分解产物进行猜想,设计方案:
(1)该小组同学猜想其产物为CO、CO2和H2O,并设计了探究实验,实验装置如下(草酸晶体分解装置略)。

A中水槽装冰水混合物、B中装氧化铜、C中装无水硫酸铜,D中装澄清石灰水、E中装碱石灰(已知草酸蒸气也可使澄清石灰水变浑浊,草酸蒸气在低温下可冷凝为固体)。请回答下列问题:
①装置的连接顺序为:A→__________ ;
②检验产物中CO的实验现象是__________ ;
③整套装置是否存在不合理之处,__________ (填是或否),若有该如何解决__________ ;
(猜想二)乙二酸具有弱酸性,设计方案:
(2)该小组同学为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是__________ (填字母)
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定相同浓度的草酸和硫酸溶液的pH
C.测定草酸钠(Na2C2O4)溶液的pH
D.将草酸溶液加入Na2CO3溶液中,有CO2放出
(猜想三)乙二酸具有还原性,设计方案:
(3)该小组同学向用硫酸酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色,从而判断草酸具有较强的还原性,写出该反应的离子方程式:__________ ;
(4)利用上述原理可定量测定某草酸晶体样品(含有H2C2O4•2H2O及其它一些杂质)中H2C2O4•2H2O的含量。方法是:称取该样品0.12g,加适量水完全溶解,然后用0.020mol•L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示(单位:mL),则该草酸晶体样品中H2C2O4•2H2O的质量分数为__________ ;(已知相对原子质量:Mr(H2C2O4•2H2O)=126)。

【研究课题】探究乙二酸的某些性质
【查阅资料】乙二酸(HOOC-COOH)俗称草酸,其主要物理常数如下:
| 名称 | 乙二酸 | 乙二酸晶体 |
| 分子式 | H2C2O4 | H2C2O4·2H2O |
| 颜色状态 | 无色固体 | 无色晶体 |
| 溶解度(g) | 8.6(20℃) | — |
| 熔点(℃) | 189.5 | 101.5 |
| 密度(g·cm-3) | 1.900 | 1.650 |
【提出猜想】
[猜想一]根据草酸晶体的组成对其分解产物进行猜想,设计方案:
(1)该小组同学猜想其产物为CO、CO2和H2O,并设计了探究实验,实验装置如下(草酸晶体分解装置略)。

A中水槽装冰水混合物、B中装氧化铜、C中装无水硫酸铜,D中装澄清石灰水、E中装碱石灰(已知草酸蒸气也可使澄清石灰水变浑浊,草酸蒸气在低温下可冷凝为固体)。请回答下列问题:
①装置的连接顺序为:A→
②检验产物中CO的实验现象是
③整套装置是否存在不合理之处,
(猜想二)乙二酸具有弱酸性,设计方案:
(2)该小组同学为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定相同浓度的草酸和硫酸溶液的pH
C.测定草酸钠(Na2C2O4)溶液的pH
D.将草酸溶液加入Na2CO3溶液中,有CO2放出
(猜想三)乙二酸具有还原性,设计方案:
(3)该小组同学向用硫酸酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色,从而判断草酸具有较强的还原性,写出该反应的离子方程式:
(4)利用上述原理可定量测定某草酸晶体样品(含有H2C2O4•2H2O及其它一些杂质)中H2C2O4•2H2O的含量。方法是:称取该样品0.12g,加适量水完全溶解,然后用0.020mol•L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示(单位:mL),则该草酸晶体样品中H2C2O4•2H2O的质量分数为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】如图是一套制取并验证氯气部分化学性质的实验装置。已知:I2遇淀粉变蓝色。

(1)装置A中,仪器a的名称_______ ,该仪器中盛放的试剂为_______ ,写出A装置发生反应的离子方程式:_______ 实验室用固体KClO3与浓HCl反应也可以制Cl2,反应的化学方程式为:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,若该反应生成6.72L(标准状况)Cl2,转移的电子数为_______ mol。
(2)B装置中饱和食盐水的作用是_______ ;当有少量Cl2通过后,观察到装置C中溶液变成蓝色,反应的离子方程式为:_______ 说明非金属性Cl_______ I(填“>”或“<”)。_______ 由此比较HCl和HI的酸性强弱,(填“能”或“不能”)理由:_______ 。
(3)当Cl2持续通过时,装置D中干燥的有色布条能否褪色?_______ 。
(4)若要证明Cl2无漂白性,则必须在装置_______ (用装置字母序号填写)之前增加一个_______ 的装置。
(5)装置E的作用是尾气处理,该反应的离子方程式为_______ 。
(6)家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式:_______ 。
(7)Cl2可用于自来水消毒,但Cl2会与水中的有机物发生反应,生成对人体有害的有机氯化物,因此,从2000年开始,国家开始逐渐用ClO2取代Cl2对自来水消毒。ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室可利用KClO3与H2C2O4(已知H2C2O4为弱酸)在酸性条件下反应,制取ClO2。请写出该反应的离子方程式:_______ 。该反应中还原产物的化学式是_______ ,被氧化的元素是_______ (填元素符号)。

(1)装置A中,仪器a的名称
(2)B装置中饱和食盐水的作用是
(3)当Cl2持续通过时,装置D中干燥的有色布条能否褪色?
(4)若要证明Cl2无漂白性,则必须在装置
(5)装置E的作用是尾气处理,该反应的离子方程式为
(6)家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
| 注意事项: 1.本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用 2.密封保存,请勿与洁厕灵同时使用 3.保质期为一年 |
(7)Cl2可用于自来水消毒,但Cl2会与水中的有机物发生反应,生成对人体有害的有机氯化物,因此,从2000年开始,国家开始逐渐用ClO2取代Cl2对自来水消毒。ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室可利用KClO3与H2C2O4(已知H2C2O4为弱酸)在酸性条件下反应,制取ClO2。请写出该反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
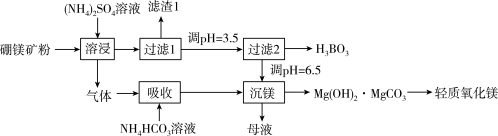
(1)能缩短“溶浸”时间的方法有_______________ 。
(2)“滤渣1”的主要成分有_________ 。如何检验“滤渣1”中是否有Fe2O3_________ 。
(3)已知:硼酸(H3BO3)是一元弱酸,其钠盐化学式为Na[B(OH)4],则硼酸在水中的电离方程式是_______________________ 。
(4)在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式为__________ ,母液经加热后可返回___________ 工序循环使用。

(1)能缩短“溶浸”时间的方法有
(2)“滤渣1”的主要成分有
(3)已知:硼酸(H3BO3)是一元弱酸,其钠盐化学式为Na[B(OH)4],则硼酸在水中的电离方程式是
(4)在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】试剂级 可用海盐(含泥沙、海藻、
可用海盐(含泥沙、海藻、 、
、 、
、 、
、 、
、 等杂质)为原料制备。制备流程简图如下:
等杂质)为原料制备。制备流程简图如下:

(1)根据除杂原理,除杂时依次添加的试剂为___________ 、 、
、___________ (填化学式)。操作 为
为___________ 。
(2)用如图所示装置,以焙炒后的海盐为原料制备 气体,并通入
气体,并通入 饱和溶液中使
饱和溶液中使 结晶析出。
结晶析出。

①用浓硫酸和海盐混合加热制取氯化氢利用了浓硫酸的性质是___________ (填编号),相比分液漏斗,选用仪器 的优点是
的优点是___________ 。
A. 高沸点 B. 强酸性 C. 强氧化性
②对比实验发现,将烧瓶中的海盐磨细可加快 晶体的析出,其原因是
晶体的析出,其原因是___________ 。
(3)设计如下实验测定 产品中
产品中 的含量,填写下列表格。
的含量,填写下列表格。
 可用海盐(含泥沙、海藻、
可用海盐(含泥沙、海藻、 、
、 、
、 、
、 、
、 等杂质)为原料制备。制备流程简图如下:
等杂质)为原料制备。制备流程简图如下:
(1)根据除杂原理,除杂时依次添加的试剂为
 、
、 为
为(2)用如图所示装置,以焙炒后的海盐为原料制备
 气体,并通入
气体,并通入 饱和溶液中使
饱和溶液中使 结晶析出。
结晶析出。
①用浓硫酸和海盐混合加热制取氯化氢利用了浓硫酸的性质是
 的优点是
的优点是A. 高沸点 B. 强酸性 C. 强氧化性
②对比实验发现,将烧瓶中的海盐磨细可加快
 晶体的析出,其原因是
晶体的析出,其原因是(3)设计如下实验测定
 产品中
产品中 的含量,填写下列表格。
的含量,填写下列表格。| 操作 | 目的/结论 | |
| ① | 称取样品 ,加水溶解,加盐酸调至弱酸性,滴加过量 ,加水溶解,加盐酸调至弱酸性,滴加过量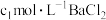 溶液 溶液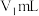 | 目的: |
| ② | 过滤、洗涤,干燥后称得沉淀为 | 结论:样品中 的质量分数为 的质量分数为 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:

请回答下列问题:
(1)固体a的化学式为________ 。
(2)写出Ⅱ中加过量的烧碱涉及到的反应离子方程式______________ 、_____________ ;Ⅲ中通入足量CO2气体发生反应的离子方程式为_______________ 。
(3)由Ⅲ中得到滤液c的实验操作为__________ ,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)________ 、冷却结晶、过滤洗涤。
(4)将NH4Al(SO4)2溶液和Ba(OH)2溶液,按物质的量比1:2混合,写出离子方程式为_______________ 。
(5)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为________ 。

请回答下列问题:
(1)固体a的化学式为
(2)写出Ⅱ中加过量的烧碱涉及到的反应离子方程式
(3)由Ⅲ中得到滤液c的实验操作为
(4)将NH4Al(SO4)2溶液和Ba(OH)2溶液,按物质的量比1:2混合,写出离子方程式为
(5)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室用如下方法测定 与
与 的混合物中
的混合物中 的质量分数。
的质量分数。
(1)称取该混合物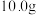 ,溶于水配成
,溶于水配成 溶液,下列操作会使所配溶液浓度偏小的有
溶液,下列操作会使所配溶液浓度偏小的有____ (填标号)。
A.未将洗涤液转移至容量瓶中
B.定容时俯视刻度线
C.定容振荡摇匀后液面低于刻度线,未做处理
(2)量取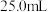 上述溶液于烧杯中,滴加足量
上述溶液于烧杯中,滴加足量 溶液,将
溶液,将 、
、 完全转化为沉淀,其中
完全转化为沉淀,其中 参与反应的离子方程式为
参与反应的离子方程式为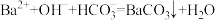 ,
, 属于
属于_______ (填“酸碱”或“盐”)。
(3)简述证明溶液中 、
、 已完全转化为沉淀的操作及现象:
已完全转化为沉淀的操作及现象:________ 。
 与
与 的混合物中
的混合物中 的质量分数。
的质量分数。(1)称取该混合物
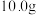 ,溶于水配成
,溶于水配成 溶液,下列操作会使所配溶液浓度偏小的有
溶液,下列操作会使所配溶液浓度偏小的有A.未将洗涤液转移至容量瓶中
B.定容时俯视刻度线
C.定容振荡摇匀后液面低于刻度线,未做处理
(2)量取
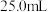 上述溶液于烧杯中,滴加足量
上述溶液于烧杯中,滴加足量 溶液,将
溶液,将 、
、 完全转化为沉淀,其中
完全转化为沉淀,其中 参与反应的离子方程式为
参与反应的离子方程式为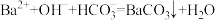 ,
, 属于
属于(3)简述证明溶液中
 、
、 已完全转化为沉淀的操作及现象:
已完全转化为沉淀的操作及现象:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】Ⅰ.写出下列反应的离子方程式:
(1)将鸡蛋壳在醋酸中溶解有气泡产生:_____________________________________________ ;
(2)CuSO4溶液与Ba(OH)2溶液混合:________________________________________ 。
Ⅱ.对一份稀溶液作初步分析后发现,溶液无色、澄清,其可能含有SO42—、Na+、CO32—、H+、NO3—、HCO3—、Cl−等离子中的若干种。然后又作了如下分析,以确定这些离子是否存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(1)原溶液中一定存在的离子是__________ ,一定不存在的离子是____________ 。
(2)在上述实验操作中,有错误的步骤是(填代号)______ 。对该错误改正的方法是(要作较详细的说明)_________________________________________________________ 。
(3)到目前为止,不能肯定在原溶液中是否存在的离子是____________ 。
(1)将鸡蛋壳在醋酸中溶解有气泡产生:
(2)CuSO4溶液与Ba(OH)2溶液混合:
Ⅱ.对一份稀溶液作初步分析后发现,溶液无色、澄清,其可能含有SO42—、Na+、CO32—、H+、NO3—、HCO3—、Cl−等离子中的若干种。然后又作了如下分析,以确定这些离子是否存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(1)原溶液中一定存在的离子是
(2)在上述实验操作中,有错误的步骤是(填代号)
(3)到目前为止,不能肯定在原溶液中是否存在的离子是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钾溶液中得到氯化钾固体,选择装置________ (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置________ 。
(2)从碘水中分离出I2,选择装置______ ,该分离方法的名称为________ 、_______ 。
(3)装置B在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是_________________________________________________________ 。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:

粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④用适量盐酸调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发
正确的操作顺序是________ (填选项字母)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
(5)粗盐的提纯实验中每步所加试剂均需过量,如何判断除杂过程中所加BaCl2溶液是否过量?_______________________________________________________ 。

(1)从氯化钾溶液中得到氯化钾固体,选择装置
(2)从碘水中分离出I2,选择装置
(3)装置B在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:

粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④用适量盐酸调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发
正确的操作顺序是
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
(5)粗盐的提纯实验中每步所加试剂均需过量,如何判断除杂过程中所加BaCl2溶液是否过量?
您最近一年使用:0次



