为探究X(仅含三种元素)的组成和热稳定性,设计并完成如下实验:
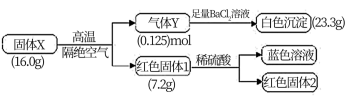
气体Y不能使品红溶液褪色,红色固体1是一种纯净物,请回答:
(1)X除了含有Cu元素之外,还有___ 元素(填元素符号)。
(2)该流程中X高温分解的化学方程式为____ 。
(3)写出气体Y通入BaCl2溶液发生反应的离子方程式___ 。

气体Y不能使品红溶液褪色,红色固体1是一种纯净物,请回答:
(1)X除了含有Cu元素之外,还有
(2)该流程中X高温分解的化学方程式为
(3)写出气体Y通入BaCl2溶液发生反应的离子方程式
18-19高一·浙江·期中 查看更多[2]
更新时间:2019-11-13 09:37:14
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E、X均为短周期元素形成的无机物,存在下图所示转化关系(部分生成物和反应条件略去);已知A 由短周期非金属元素组成,B具有漂白性且光照易分解。请回答以下问题:

(1)若A为单质,且C为一元强酸。
①写出一种工业制备单质A的离子方程式:____________________ 。
②X可能为________ (填字母代号)。
a.NaOH b.AlCl3 c.Na2CO3 d.NaAlO2
(2)若A为两种元素形成的化合物,且E与水反应生成的G的浓溶液遇C有白烟产生。
①A与H2O反应的化学方程式为_____________________________ 。
②室温下,NH2OH(羟氨)会发生分解生成C、D,试写出其分解反应的化学方程式_______ 。

(1)若A为单质,且C为一元强酸。
①写出一种工业制备单质A的离子方程式:
②X可能为
a.NaOH b.AlCl3 c.Na2CO3 d.NaAlO2
(2)若A为两种元素形成的化合物,且E与水反应生成的G的浓溶液遇C有白烟产生。
①A与H2O反应的化学方程式为
②室温下,NH2OH(羟氨)会发生分解生成C、D,试写出其分解反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W四种常见化合物,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去):

请回答:
(1)画出X、Y、Z中焰色试验呈黄色的元素原子结构示意图_______ ,W的名称是_______ 。
(2)X与Y在溶液中反应的离子方程式是_______ 。
(3)①将132克W通入到含160克Y的的水溶液中,该反应的总离子方程式为_______ 。
②自然界中存在X、Z和H2O按一定比例结晶而成的固体。取m克该固体测得所含金属阳离子的质量为1.15克, 若取相同质量的固体加热至恒重,剩余固体的质量为_______ g。
(4)Ⅰ和Ⅱ中为X所含有的四种元素中的两种或三种组成的化合物,并利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色助燃性气体。

①装置Ⅱ中物质的化学式是_______ 。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集干燥的装置Ⅴ中气体,该化合物的化学式是_______ ,所需仪器装置是_______ (从上图选择必要装置,填写装置下方的编号)。

请回答:
(1)画出X、Y、Z中焰色试验呈黄色的元素原子结构示意图
(2)X与Y在溶液中反应的离子方程式是
(3)①将132克W通入到含160克Y的的水溶液中,该反应的总离子方程式为
②自然界中存在X、Z和H2O按一定比例结晶而成的固体。取m克该固体测得所含金属阳离子的质量为1.15克, 若取相同质量的固体加热至恒重,剩余固体的质量为
(4)Ⅰ和Ⅱ中为X所含有的四种元素中的两种或三种组成的化合物,并利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色助燃性气体。

①装置Ⅱ中物质的化学式是
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集干燥的装置Ⅴ中气体,该化合物的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知A、E为金属单质,B是淡黄色粉末且常用于防毒面具中,回答下题。
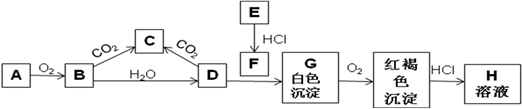
(1)实验室中A常常保存在盛放__________ 的广口瓶中,A焰色反应为__________ 色。
(2)写出B转变成C的化学方程式_______________________ 。该反应中氧化剂是_________ ,还原剂是___________ ,0.1molB参与该反应,转移电子的个数为_________ 。
(3)写出D与F反应生成G的离子方程式:____________________________________________ 。
(4)描述H溶液中金属阳离子的实验室检验方法______________________________________ ;其涉及到的离子反应方程式为:_________________________________ 。

(1)实验室中A常常保存在盛放
(2)写出B转变成C的化学方程式
(3)写出D与F反应生成G的离子方程式:
(4)描述H溶液中金属阳离子的实验室检验方法
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】生活中我们都会发现,煮鸡蛋时间太久或放置时间过长,蛋黄上会产生一层“黑膜”,该黑膜的成分是硫化亚铁。这是由于鸡蛋里的蛋白质受热分解成小分子的氨基酸,有的氨基酸含硫元素,会形成硫化氢,而蛋黄中富含铁元素,当硫化氢遇到铁元素就形成了硫化亚铁,也就是蛋黄上覆盖的那层“黑膜”。

某同学由此联想到铁与硫单质的反应,为了验证铁与硫单质反应产物中铁元素的化合价,该同学设计了以下实验:

已知:①FeS固体难溶于水,可与稀盐酸、稀硫酸发生反应:FeS+2H+=Fe2++H2S↑。
②3S+6NaOH 2Na2S+Na2SO3+3H2O。
2Na2S+Na2SO3+3H2O。
请回答以下问题:
(1)混合粉末A中硫粉必须过量的原因是_______ 。
(2)反应在“惰性环境”中进行的原因是_______ 。
(3)操作②的作用是_______ ,也可改用_______ 。
(4)操作③稀硫酸煮沸的目的是_______ 。
(5)为检验产物中铁元素的价态,对D溶液的实验操作最好是_______ 。

某同学由此联想到铁与硫单质的反应,为了验证铁与硫单质反应产物中铁元素的化合价,该同学设计了以下实验:

已知:①FeS固体难溶于水,可与稀盐酸、稀硫酸发生反应:FeS+2H+=Fe2++H2S↑。
②3S+6NaOH
 2Na2S+Na2SO3+3H2O。
2Na2S+Na2SO3+3H2O。请回答以下问题:
(1)混合粉末A中硫粉必须过量的原因是
(2)反应在“惰性环境”中进行的原因是
(3)操作②的作用是
(4)操作③稀硫酸煮沸的目的是
(5)为检验产物中铁元素的价态,对D溶液的实验操作最好是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】物质的类别和核心元素的化合价是研究物质性质的两个重要维度。下图为硫及其部分化合物的“价类二维图”, 根据图示回答下列问题:

(1)图中A、B、C、D四种物质中,属于非电解质的是__________ (用化学式表示)。
(2)足量B通入紫色石蕊试液的现象是______________________________________ ;
FeCl3溶液(酸性)中通入B的离子方程式为___________________________ 。
(3)C在反应中既可作氧化剂,又可作还原剂。当它作氧化剂时,理论上其可被还原为____ (填标号)。
A.Na2S B.S C.H2SO3 D.Na2SO4 E.H2SO4
(4)从硫元素化合价分析,硫单质具有氧化性和还原性。请举一例说明其具有氧化性(用化学方程式表示)_______________________________ 。
(5)将A与SO2混合,可生成淡黄色固体。该反应的氧化产物与还原产物的质量之比为__________________________ 。

(1)图中A、B、C、D四种物质中,属于非电解质的是
(2)足量B通入紫色石蕊试液的现象是
FeCl3溶液(酸性)中通入B的离子方程式为
(3)C在反应中既可作氧化剂,又可作还原剂。当它作氧化剂时,理论上其可被还原为
A.Na2S B.S C.H2SO3 D.Na2SO4 E.H2SO4
(4)从硫元素化合价分析,硫单质具有氧化性和还原性。请举一例说明其具有氧化性(用化学方程式表示)
(5)将A与SO2混合,可生成淡黄色固体。该反应的氧化产物与还原产物的质量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下列为A、B、C、D四种物质的转化关系,a、b为反应条件。
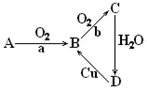
(1)若A为单质,a为点燃,b为催化剂、加热,则A为_________ (填写化学式),
写出B→C的方程式___________________ 。
(2)若A为气态化合物,B→C转化不需要条件,则A为______ (填写化学式),写出A→B化学方程式_________________ 。
写出Cu+D溶液→B的离子方程式___________________ 。
(3)把某黑色固体Y加热至红热,投入到上述某种无色溶液D中产生两种气体组成的混合气体X,将X做如下所示实验:

写出M、G所代表物质的化学式 M___________ 、G_____________

(1)若A为单质,a为点燃,b为催化剂、加热,则A为
写出B→C的方程式
(2)若A为气态化合物,B→C转化不需要条件,则A为
写出Cu+D溶液→B的离子方程式
(3)把某黑色固体Y加热至红热,投入到上述某种无色溶液D中产生两种气体组成的混合气体X,将X做如下所示实验:

写出M、G所代表物质的化学式 M
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】工业上冶炼冰铜(mCu2O·nFeS)可得到粗铜,在空气中煅烧冰铜时,产生一种有刺激性气味的气体A,该气体排放到空气中,会对空气形成严重污染。

完成下列填空:
(1)为了降低污染气体A的排放,可选用下列试剂中的__ (填序号)吸收。
a.浓硫酸 b.浓硝酸 c.氢氧化钠溶液 d.石灰乳
(2)已知Al能将某些金属从其氧化物中置换出来,将铝与泡铜高温反应可制得粗铜,制取该粗铜的化学方程式是________________________________ 。当转移电子数为6NA时,理论上消耗Al的质量为_______ g。
(3)SO2气体和H2S气体反应可生成单质硫,现有SO2和H2S混合气体2.0 mol,当所得到的氧化产物比还原产物多16克时,则混合气体中H2S的物质的量可能为:__________________ 。
(4)纳米氧化铝在陶瓷材料、电子工业、生物医药等方面有广阔的应用前景,它可通过硫酸铝铵晶体热分解得到。取4.53g硫酸铝铵晶体【Al2(NH4)2(SO4)n·24H2O,相对分子质量为906】加热分解,最终剩余0.51 g Al2O3固体。加热过程中,固体质量随时间的变化如图2所示。
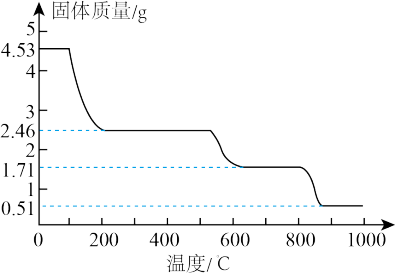
试通过计算确定400℃剩余固体成分的化学式________________ 。(写出计算过程)

完成下列填空:
(1)为了降低污染气体A的排放,可选用下列试剂中的
a.浓硫酸 b.浓硝酸 c.氢氧化钠溶液 d.石灰乳
(2)已知Al能将某些金属从其氧化物中置换出来,将铝与泡铜高温反应可制得粗铜,制取该粗铜的化学方程式是
(3)SO2气体和H2S气体反应可生成单质硫,现有SO2和H2S混合气体2.0 mol,当所得到的氧化产物比还原产物多16克时,则混合气体中H2S的物质的量可能为:
(4)纳米氧化铝在陶瓷材料、电子工业、生物医药等方面有广阔的应用前景,它可通过硫酸铝铵晶体热分解得到。取4.53g硫酸铝铵晶体【Al2(NH4)2(SO4)n·24H2O,相对分子质量为906】加热分解,最终剩余0.51 g Al2O3固体。加热过程中,固体质量随时间的变化如图2所示。

试通过计算确定400℃剩余固体成分的化学式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
【推荐2】现拟用图所示装置(尾气处理部分略)来制取一氧化碳,并用以测定某铜粉样品(混有CuO粉末)中金属铜的含量

(1)制备一氧化碳的化学方程式是______ ;
(2)试验中,观察到反应管中发生的现象是______ ;尾气的主要成分是______ ;
(3)反应完成后,正确的操作顺序为______ (填字母)
a.关闭漏斗开关 b.熄灭酒精1 c.熄灭酒精灯2
(4)若试验中称取铜粉样品5.0g,充分反应后,反应管中剩余固体的质量为4.8g,则原样品中单质铜的质量分数为______ ;
(5)从浓硫酸、浓硝酸、蒸馏水、双氧水中选用合适的试剂,设计一个测定样品中金属铜质量分数的方案;
①设计方案的主要步骤是(不必描述操作过程的细节)______ ;
②写出有关反应的化学方程式______ 。

(1)制备一氧化碳的化学方程式是
(2)试验中,观察到反应管中发生的现象是
(3)反应完成后,正确的操作顺序为
a.关闭漏斗开关 b.熄灭酒精1 c.熄灭酒精灯2
(4)若试验中称取铜粉样品5.0g,充分反应后,反应管中剩余固体的质量为4.8g,则原样品中单质铜的质量分数为
(5)从浓硫酸、浓硝酸、蒸馏水、双氧水中选用合适的试剂,设计一个测定样品中金属铜质量分数的方案;
①设计方案的主要步骤是(不必描述操作过程的细节)
②写出有关反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】在工业上用辉铜矿(主要成分为(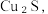 含少量Fe₂O₃、SiO₂等杂质)来制备碱式碳酸铜的工艺流程如下图:
含少量Fe₂O₃、SiO₂等杂质)来制备碱式碳酸铜的工艺流程如下图:_____ 。(填字母)
A.适当增大硫酸浓度 B.将辉铜矿粉碎 C.延长浸取时间
(2)“浸取”过程中,会加入软锰矿(主要成分为 氧化
氧化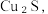 并生成一种黄色沉淀,该沉淀为:
并生成一种黄色沉淀,该沉淀为:_____ 。
(3)“除铁”时将溶液从强酸性调至pH约为3,A物质宜选用_____ 。
(4)为了保证产品纯度,请设计实验确认 是否除尽
是否除尽_____ 。
(5)“沉锰”(除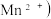 过程中有关反应的离子方程式为
过程中有关反应的离子方程式为_____ 。
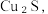 含少量Fe₂O₃、SiO₂等杂质)来制备碱式碳酸铜的工艺流程如下图:
含少量Fe₂O₃、SiO₂等杂质)来制备碱式碳酸铜的工艺流程如下图: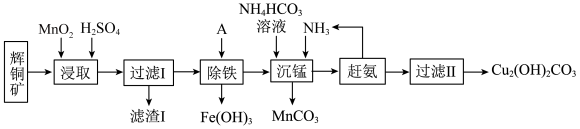
A.适当增大硫酸浓度 B.将辉铜矿粉碎 C.延长浸取时间
(2)“浸取”过程中,会加入软锰矿(主要成分为
 氧化
氧化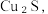 并生成一种黄色沉淀,该沉淀为:
并生成一种黄色沉淀,该沉淀为:(3)“除铁”时将溶液从强酸性调至pH约为3,A物质宜选用
(4)为了保证产品纯度,请设计实验确认
 是否除尽
是否除尽(5)“沉锰”(除
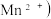 过程中有关反应的离子方程式为
过程中有关反应的离子方程式为
您最近一年使用:0次



