为除去粗盐中的CaCl2、MgCl2、硫酸钠以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:
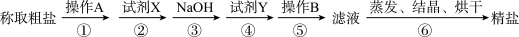
(1)第⑤步中,操作B是___ (填操作名称),第④步中,试剂Y是___ 。
(2)判断试剂X过量的方法是___ 。
(3)写出第②步中涉及反应的化学方程式___ 。
(4)第⑤步操作中得到的固体成分有:泥沙、CaCO3、Mg(OH)2、___ (填化学式)。
(5)此实验方案尚需完善,具体步骤是___ 。
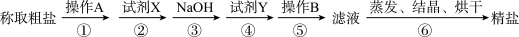
(1)第⑤步中,操作B是
(2)判断试剂X过量的方法是
(3)写出第②步中涉及反应的化学方程式
(4)第⑤步操作中得到的固体成分有:泥沙、CaCO3、Mg(OH)2、
(5)此实验方案尚需完善,具体步骤是
更新时间:2019-12-11 14:44:01
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】软锰矿是一种常见的锰矿物,主要成分是MnO2,常含有铁、铝元素形成的杂质。工业上,用软锰矿制取高锰酸钾的流程如下(部分条件和产物省略):
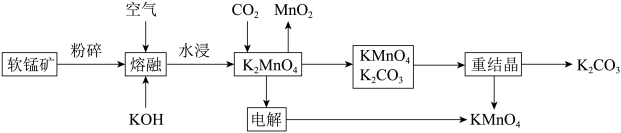
请回答下列问题:
(1)Mn的价层电子排布式为_______ ;杂质中的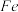 元素在元素周期表中的位置为
元素在元素周期表中的位置为_______ 。
(2)CO2与K2MnO4反应的离子方程式为_______ 。
(3)KMnO4与K2CO3能用重结晶(冷却结晶)的方法分离的原理是_______ 。
(4)“电解”过程中使用的是惰性电极,则:
①阴极附近溶液的pH将_______ (填“增大”“减小”或“不变”)。
②工业上可用石墨为电极电解硫酸锰和硫酸的混合溶液制备MnO2,其阳极的电极反应式为_______ 。
(5)可用过氧化氢溶液滴定的方法测定高锰酸钾样品纯度。当达到滴定终点时,溶液中产生的现象为_______ 。
(6)常温下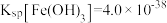 ,
, 。常温下,若某溶液中,
。常温下,若某溶液中, ,
, ,向其中逐滴加入稀氨水,若Mn2+开始沉淀时,c(Fe3+)=
,向其中逐滴加入稀氨水,若Mn2+开始沉淀时,c(Fe3+)=_______ mol/L。

请回答下列问题:
(1)Mn的价层电子排布式为
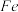 元素在元素周期表中的位置为
元素在元素周期表中的位置为(2)CO2与K2MnO4反应的离子方程式为
(3)KMnO4与K2CO3能用重结晶(冷却结晶)的方法分离的原理是
(4)“电解”过程中使用的是惰性电极,则:
①阴极附近溶液的pH将
②工业上可用石墨为电极电解硫酸锰和硫酸的混合溶液制备MnO2,其阳极的电极反应式为
(5)可用过氧化氢溶液滴定的方法测定高锰酸钾样品纯度。当达到滴定终点时,溶液中产生的现象为
(6)常温下
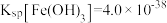 ,
, 。常温下,若某溶液中,
。常温下,若某溶液中, ,
, ,向其中逐滴加入稀氨水,若Mn2+开始沉淀时,c(Fe3+)=
,向其中逐滴加入稀氨水,若Mn2+开始沉淀时,c(Fe3+)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某校学生用如图所示装置进行实验,以探究苯与溴发生反应的原理并分离提纯反应的产物。回答下列问题:
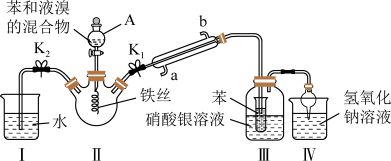
(1)仪器A的名称是___________ ,冷凝管所起的作用为冷凝回流蒸气,冷凝水从___________ (填“a”或“b”口)进入。
(2)实验开始时,关闭 、开启
、开启 和分液漏斗活塞,滴加苯和液溴的混合液,反应开始,III中小试管内苯的作用是
和分液漏斗活塞,滴加苯和液溴的混合液,反应开始,III中小试管内苯的作用是___________ 。
(3)能说明苯与液溴发生了取代反应的现象是___________ ;若把III中洗气瓶内的硝酸银溶液换为___________ (填试剂名称),当出现___________ 现象也能说明发生了取代反应。
(4)四个实验装置中能起防倒吸作用的装置有___________ (填装置编号)。
(5)将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。用蒸馏水洗涤,振荡,分液;用5%的NaOH溶液洗涤,振荡,分液;用蒸馏水洗涤,振荡,分液;加入无水氯化钙干燥;___________ (填操作名称。)
(6)将有机物A置于氧气流中充分燃烧,A和氧气恰好完全反应且消耗6.72L(标准状况)氧气,生成5.4g 和8.8g
和8.8g  ,则A的最简式为
,则A的最简式为___________ 。
(7)要确定该有机物A的分子式,还需要测定___________ ,目前最精确、最快捷的测定方法是___________ 。
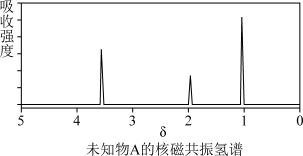
(8)若核磁共振氢谱如下图,则该分子可能为___________ (填名称)。

(1)仪器A的名称是
(2)实验开始时,关闭
 、开启
、开启 和分液漏斗活塞,滴加苯和液溴的混合液,反应开始,III中小试管内苯的作用是
和分液漏斗活塞,滴加苯和液溴的混合液,反应开始,III中小试管内苯的作用是(3)能说明苯与液溴发生了取代反应的现象是
(4)四个实验装置中能起防倒吸作用的装置有
(5)将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。用蒸馏水洗涤,振荡,分液;用5%的NaOH溶液洗涤,振荡,分液;用蒸馏水洗涤,振荡,分液;加入无水氯化钙干燥;
(6)将有机物A置于氧气流中充分燃烧,A和氧气恰好完全反应且消耗6.72L(标准状况)氧气,生成5.4g
 和8.8g
和8.8g  ,则A的最简式为
,则A的最简式为(7)要确定该有机物A的分子式,还需要测定
(8)若核磁共振氢谱如下图,则该分子可能为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】市场销售的某种食用精制盐包装袋上有如下说明:
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,
KIO +5KI+3H2SO4 = 3K2SO4+ 3
+5KI+3H2SO4 = 3K2SO4+ 3 + 3H2O
+ 3H2O
上述反应生成的 可用四氯化碳检验:确认有
可用四氯化碳检验:确认有 生成的现象是
生成的现象是___________________
利用 稀溶液,将
稀溶液,将 还原,可从碘的四氯化碳溶液中回收四氯化碳。
还原,可从碘的四氯化碳溶液中回收四氯化碳。 稀溶液与
稀溶液与 反应的离子方程式为
反应的离子方程式为________________________ 。
(2)已知:I2+2S2O32-═2I-+S4O62-,某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解:
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂。逐滴加入物质的量浓度为2.0×10 mol/L的Na2S2O3溶液10.0mL,恰好反应完全。
mol/L的Na2S2O3溶液10.0mL,恰好反应完全。
①判断c中恰好完全反应依据的现象是_____________________________________ 。
②b中反应所产生的 的物质的量是
的物质的量是____________ ?(写出计算过程)
③根据以上实验和包装袋说明测得精制盐的碘(I)含量(以含w的代数式表示,单位为mg/kg)_______________ 。(写出计算过程)
产品标准 | GB5461 |
产品等级 | 一级 |
配料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50mg/kg |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,
KIO
 +5KI+3H2SO4 = 3K2SO4+ 3
+5KI+3H2SO4 = 3K2SO4+ 3 + 3H2O
+ 3H2O上述反应生成的
 可用四氯化碳检验:确认有
可用四氯化碳检验:确认有 生成的现象是
生成的现象是利用
 稀溶液,将
稀溶液,将 还原,可从碘的四氯化碳溶液中回收四氯化碳。
还原,可从碘的四氯化碳溶液中回收四氯化碳。 稀溶液与
稀溶液与 反应的离子方程式为
反应的离子方程式为(2)已知:I2+2S2O32-═2I-+S4O62-,某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解:
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂。逐滴加入物质的量浓度为2.0×10
 mol/L的Na2S2O3溶液10.0mL,恰好反应完全。
mol/L的Na2S2O3溶液10.0mL,恰好反应完全。①判断c中恰好完全反应依据的现象是
②b中反应所产生的
 的物质的量是
的物质的量是③根据以上实验和包装袋说明测得精制盐的碘(I)含量(以含w的代数式表示,单位为mg/kg)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】某工厂的工业废水中含有大量的FeSO4、较多的CuSO4和少量Na2SO4,为了减少污染并变废为宝,某化学兴趣小组计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。

(1)操作a所需要的玻璃仪器除烧杯外还需要_________________ 。
(2)试剂a为____________ (化学式),发生反应的化学方程式:____________________________ ;试剂b为____________ ,该试剂对应的危险品标志为_____________ (填名称)。
(3)固体A的成分为:_____ ;洗涤固体B,判断固体B已洗净的操作:_________________ 。
(4)要得到FeSO4·7H2O晶体,操作c涉及的实验操作有:_______________________ 。

(1)操作a所需要的玻璃仪器除烧杯外还需要
(2)试剂a为
(3)固体A的成分为:
(4)要得到FeSO4·7H2O晶体,操作c涉及的实验操作有:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】从海水中可以获得淡水、食盐并可提取镁、溴等物质。
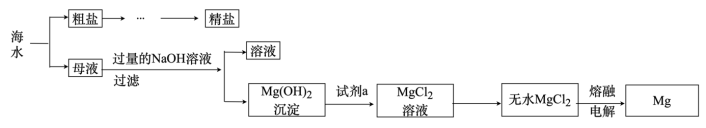
(1)试剂a是_______ 。
(2)从母液中提取镁的过程中,镁元素经历了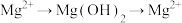 的过程,目的是
的过程,目的是_______ 。
(3)若要验证所得 溶液中是否含有
溶液中是否含有 ,可采用的方法是
,可采用的方法是_______ 。(不要求描述操作步骤和现象)
(4)用 溶液制成无水
溶液制成无水 ,加热溶液过程中,会生成
,加热溶液过程中,会生成 溶液和一种酸性气体。写出该反应的化学方程式
溶液和一种酸性气体。写出该反应的化学方程式_______ 。
(5)为了除去粗盐中 、
、 、
、 及泥沙可将粗盐溶于水,然后进行下列操作,正确的操作顺序是_______。
及泥沙可将粗盐溶于水,然后进行下列操作,正确的操作顺序是_______。
①过滤 ②加过量 溶液 ③加适量盐酸 ④加过量
溶液 ③加适量盐酸 ④加过量 溶液 ⑤加过量
溶液 ⑤加过量 溶液
溶液

(1)试剂a是
(2)从母液中提取镁的过程中,镁元素经历了
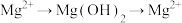 的过程,目的是
的过程,目的是(3)若要验证所得
 溶液中是否含有
溶液中是否含有 ,可采用的方法是
,可采用的方法是(4)用
 溶液制成无水
溶液制成无水 ,加热溶液过程中,会生成
,加热溶液过程中,会生成 溶液和一种酸性气体。写出该反应的化学方程式
溶液和一种酸性气体。写出该反应的化学方程式(5)为了除去粗盐中
 、
、 、
、 及泥沙可将粗盐溶于水,然后进行下列操作,正确的操作顺序是_______。
及泥沙可将粗盐溶于水,然后进行下列操作,正确的操作顺序是_______。①过滤 ②加过量
 溶液 ③加适量盐酸 ④加过量
溶液 ③加适量盐酸 ④加过量 溶液 ⑤加过量
溶液 ⑤加过量 溶液
溶液| A.②⑤④①③ | B.①④②⑤③ | C.④②⑤③① | D.⑤②④①③ |
您最近一年使用:0次
【推荐3】铝土矿(主要成分是Al2O3,含SiO2、Fe2O3等杂质)是提取铝的原料,提取铝的工艺流程如图:

请回答下列问题:
(1)过滤操作需用到的玻璃仪器除烧杯、玻璃棒外,还需要___________ 。
(2)流程图中试剂X为___________ 。
(3)为验证滤液A含Fe3+,可取少量滤液A滴加___________ 溶液,溶液显红色。
(4)写出由滤液A得到NaAlO2的离子方程式:___________ 。
(5)现有153t含氧化铝50%的铝土矿,理论上可炼出___________ t金属铝。

请回答下列问题:
(1)过滤操作需用到的玻璃仪器除烧杯、玻璃棒外,还需要
(2)流程图中试剂X为
(3)为验证滤液A含Fe3+,可取少量滤液A滴加
(4)写出由滤液A得到NaAlO2的离子方程式:
(5)现有153t含氧化铝50%的铝土矿,理论上可炼出
您最近一年使用:0次



