印刷电路板的主要反应是:Cu+2FeCl3===CuCl2+2FeCl2,其中氧化剂是______ ,氧化产物是________ ;若反应中消耗了32g铜,转移电子的物质的量为_____ 。
更新时间:2019/12/16 13:57:29
|
相似题推荐
【推荐1】(1)在热的稀硫酸中溶解了11.4g FeSO4固体,加入足量 KNO3溶液,使Fe2+全部转化成Fe3+,并放出NO气体。
①反应中氧化产物是(填化学式)______ ,FeSO4恰好完全反应时,转移电子的物质的量是_____ 。
②配平该反应的方程式:
____ FeSO4+____ KNO3+____ H2SO4=_____ K2SO4+____ Fe2(SO4)3+____ NO↑+____ H2O
③用单线桥法表示下面反应中的电子转移方向和数目:_________________
2Mg+CO2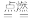 2MgO+C。
2MgO+C。
(2)硫代硫酸钠可用作脱氯剂,已知25.0mL0.10mol/L Na2S2O3溶液恰好把标准状况下112mLCl2完全转化为Cl-,则S2O32-将转化成______________
①反应中氧化产物是(填化学式)
②配平该反应的方程式:
③用单线桥法表示下面反应中的电子转移方向和数目:
2Mg+CO2
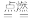 2MgO+C。
2MgO+C。(2)硫代硫酸钠可用作脱氯剂,已知25.0mL0.10mol/L Na2S2O3溶液恰好把标准状况下112mLCl2完全转化为Cl-,则S2O32-将转化成
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化亚铜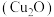 是一种鲜红色粉末状固体,主要用于制造安全杀虫剂、分析试剂、红色玻璃等,几乎不溶于水,可在酸性溶液中发生反应,与硫酸、盐酸、硝酸反应如下:
是一种鲜红色粉末状固体,主要用于制造安全杀虫剂、分析试剂、红色玻璃等,几乎不溶于水,可在酸性溶液中发生反应,与硫酸、盐酸、硝酸反应如下:
①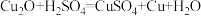
②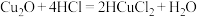
③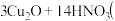 稀
稀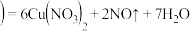
(1) 中
中 的化合价为
的化合价为_______ 。
(2)反应①中还原剂为_______ ,还原产物为_______ 。
(3)反应②_______ (填“是”或“不是”)氧化还原反应 若不是请说明判断依据:
若不是请说明判断依据:_______ 。
(4)请写出反应③的离子方程式:_______ 。
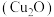 是一种鲜红色粉末状固体,主要用于制造安全杀虫剂、分析试剂、红色玻璃等,几乎不溶于水,可在酸性溶液中发生反应,与硫酸、盐酸、硝酸反应如下:
是一种鲜红色粉末状固体,主要用于制造安全杀虫剂、分析试剂、红色玻璃等,几乎不溶于水,可在酸性溶液中发生反应,与硫酸、盐酸、硝酸反应如下:①
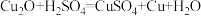
②
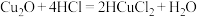
③
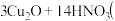 稀
稀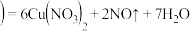
(1)
 中
中 的化合价为
的化合价为(2)反应①中还原剂为
(3)反应②
 若不是请说明判断依据:
若不是请说明判断依据:(4)请写出反应③的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】地球上的金属矿物资源是有限的,应合理开发利用。
(1)金属冶炼的实质是金属离子被_______ (填“氧化”或“还原”)生成金属单质。
(2)铜在自然界存在于多种矿石中,如:
请回答下列问题:
①上表所列铜化合物中,推断铜的质量百分含量最高的是_______ 。
②CuFeS2其中 Cu 为+1 价、Fe 为+3 价,高温焙烧时发生的反应是CuFeS2 + O2 SO2 +FeS +Cu,焙烧过程中被还原的元素有
SO2 +FeS +Cu,焙烧过程中被还原的元素有_______ 。
③工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:Cu2S+O2 2Cu+SO2,该反应中氧化剂是
2Cu+SO2,该反应中氧化剂是_______ 。
④Cu2(OH)2 CO3与稀硫酸反应的化学方程式为_______ 。
(1)金属冶炼的实质是金属离子被
(2)铜在自然界存在于多种矿石中,如:
| 矿石名称 | 黄铜矿 | 辉铜矿 | 孔雀石 |
| 主要成分 | CuFeS2 | Cu2S | Cu2(OH)2CO3 |
①上表所列铜化合物中,推断铜的质量百分含量最高的是
②CuFeS2其中 Cu 为+1 价、Fe 为+3 价,高温焙烧时发生的反应是CuFeS2 + O2
 SO2 +FeS +Cu,焙烧过程中被还原的元素有
SO2 +FeS +Cu,焙烧过程中被还原的元素有③工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:Cu2S+O2
 2Cu+SO2,该反应中氧化剂是
2Cu+SO2,该反应中氧化剂是④Cu2(OH)2 CO3与稀硫酸反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)在下列各反应均涉及HCl:
①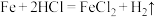 ②
②
③ ④
④
其中HCl做还原剂的是_______ (填序号),HCl做氧化剂的是_______ (填序号);试比较Cl2、Br2、KClO3的氧化性,其由强到弱的顺序为_______ ;试用“单线桥法”标明④中电子转移的方向和数目_______ 。
(2)黑火药着火时主要发生化学反应: 。该反应中被还原的元素为
。该反应中被还原的元素为_______ ,氧化产物为_______ ,若生成14gN2,则转移电子数目为_______ 。
(3)CuCl常用作催化剂,可以在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热生成CuCl沉淀,请写出该反应的离子方程式_______ 。
(1)在下列各反应均涉及HCl:
①
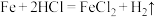 ②
②
③
 ④
④
其中HCl做还原剂的是
(2)黑火药着火时主要发生化学反应:
 。该反应中被还原的元素为
。该反应中被还原的元素为(3)CuCl常用作催化剂,可以在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热生成CuCl沉淀,请写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】将高碘酸H5IO6加入MnSO4溶液中可使溶液呈紫红色,已知H5IO6在反应中发生如下过程:H5IO6→HIO3。完成下列填空:
(1)将该反应的氧化剂、还原剂及配平后的系数填入正确位置。
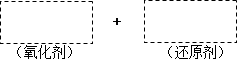
(2)在上图中标明电子转移的方向和数目:
______________________________
(3)若向H5IO6溶液中加入足量的下列物质,能将碘元素还原成碘离子的是____ (选填序号)。
a. 盐酸 b. 硫化氢 c. 溴化钠 d. 硫酸亚铁
(4)若向含1mol H5IO6的溶液中加入过量的过氧化氢溶液,再加入淀粉溶液,溶液变蓝,同时有大量气体产生。请写出此反应的化学方程式:________________________________ ,此过程中至少可得到气体_________ L(标准状态下)。
(1)将该反应的氧化剂、还原剂及配平后的系数填入正确位置。
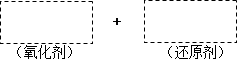
(2)在上图中标明电子转移的方向和数目:
(3)若向H5IO6溶液中加入足量的下列物质,能将碘元素还原成碘离子的是
a. 盐酸 b. 硫化氢 c. 溴化钠 d. 硫酸亚铁
(4)若向含1mol H5IO6的溶液中加入过量的过氧化氢溶液,再加入淀粉溶液,溶液变蓝,同时有大量气体产生。请写出此反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】地球上的氮元素对动植物有重要作用,其中氨的合成与应用是当前的研究热点。
(1) 的电子式为
的电子式为_______ ,实验室通过加热 和
和 的混合物制取氨,该反应的化学方程式为
的混合物制取氨,该反应的化学方程式为_______ 。
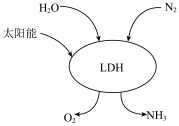
(2)我国科研团队借助一种固体催化剂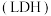 ,在常温、常压和可见光条件下合成氨,其过程如图所示。该反应的化学方程式为
,在常温、常压和可见光条件下合成氨,其过程如图所示。该反应的化学方程式为_______ ,该反应中每转移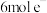 ,生成
,生成 的体积为
的体积为_______ L(标准状况下)。
(3)实验室为模拟工业生产制备少量硝酸,设计的流程如图。
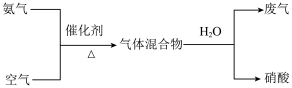
①实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可超过700℃,由此可知该反应是_______ (填“吸热”或“放热”)反应,反应的化学方程式为_______ 。
②控制氨气和空气( 体积分数为20%)的比例是制备硝酸的关键。当比例不合适时,废气中含有氮氧化物。欲使氨气尽可能完全转化为硝酸,理论上
体积分数为20%)的比例是制备硝酸的关键。当比例不合适时,废气中含有氮氧化物。欲使氨气尽可能完全转化为硝酸,理论上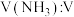 (空气)的最佳比例为
(空气)的最佳比例为_______ (同温同压条件下)。
(4)农业生产过程中使用的铵态氮肥,是水体中铵态氮元素的来源之一、检验某氮肥样品中是否存在 的实验方法是
的实验方法是_______ 。
(1)
 的电子式为
的电子式为 和
和 的混合物制取氨,该反应的化学方程式为
的混合物制取氨,该反应的化学方程式为(2)我国科研团队借助一种固体催化剂
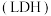 ,在常温、常压和可见光条件下合成氨,其过程如图所示。该反应的化学方程式为
,在常温、常压和可见光条件下合成氨,其过程如图所示。该反应的化学方程式为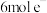 ,生成
,生成 的体积为
的体积为
(3)实验室为模拟工业生产制备少量硝酸,设计的流程如图。

①实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可超过700℃,由此可知该反应是
②控制氨气和空气(
 体积分数为20%)的比例是制备硝酸的关键。当比例不合适时,废气中含有氮氧化物。欲使氨气尽可能完全转化为硝酸,理论上
体积分数为20%)的比例是制备硝酸的关键。当比例不合适时,废气中含有氮氧化物。欲使氨气尽可能完全转化为硝酸,理论上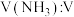 (空气)的最佳比例为
(空气)的最佳比例为(4)农业生产过程中使用的铵态氮肥,是水体中铵态氮元素的来源之一、检验某氮肥样品中是否存在
 的实验方法是
的实验方法是
您最近一年使用:0次
【推荐1】 是目前国际上公认的新一代高效、广谱、安全的杀菌。我国最近成功研制出制取
是目前国际上公认的新一代高效、广谱、安全的杀菌。我国最近成功研制出制取 的新方法,其反应的微观过程如图所示:
的新方法,其反应的微观过程如图所示:
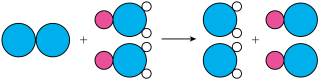
其中 表示Cl原子
表示Cl原子  表示Na原子
表示Na原子  表示O原子
表示O原子
(1)试写出该反应的化学方程式_______ ,氧化剂是_______ 。
(2)将 通入酸性淀性粉KI溶液,溶液变成蓝色,
通入酸性淀性粉KI溶液,溶液变成蓝色, 转化为氯离子,该反应是氧化还原反应,其中氧化产物是
转化为氯离子,该反应是氧化还原反应,其中氧化产物是_______ ,试写出该反应的离子方程式(无需配平)。_______ 。
(3)通过以上信息,推测 、NaClO2、
、NaClO2、 三种物质氧化性强弱的顺序为
三种物质氧化性强弱的顺序为_______ 。
 是目前国际上公认的新一代高效、广谱、安全的杀菌。我国最近成功研制出制取
是目前国际上公认的新一代高效、广谱、安全的杀菌。我国最近成功研制出制取 的新方法,其反应的微观过程如图所示:
的新方法,其反应的微观过程如图所示:
其中
 表示Cl原子
表示Cl原子  表示Na原子
表示Na原子  表示O原子
表示O原子(1)试写出该反应的化学方程式
(2)将
 通入酸性淀性粉KI溶液,溶液变成蓝色,
通入酸性淀性粉KI溶液,溶液变成蓝色, 转化为氯离子,该反应是氧化还原反应,其中氧化产物是
转化为氯离子,该反应是氧化还原反应,其中氧化产物是(3)通过以上信息,推测
 、NaClO2、
、NaClO2、 三种物质氧化性强弱的顺序为
三种物质氧化性强弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铝在地壳中的含量仅次于氧和硅,是地壳中含量最多的金属。
(1)写出铝的原子结构示意图________ 。
(2)地壳中含量前三位的元素中,和铝处于同一周期的元素是______ 。
(3)铝既能与酸又能与碱发生反应,写出其分别与盐酸、氢氧化钠溶液反应得到的铝盐______ 、_______ 。
(4)铝能和氧化铁发生铝热反应:2Al+Fe2O3 2Fe+Al2O3,工业上利用该原理来冶炼某些难熔的金属。在该反应中铝的作用是
2Fe+Al2O3,工业上利用该原理来冶炼某些难熔的金属。在该反应中铝的作用是_______ ,标出该反应的电子转移方向和数目_______ 。
(5)明矾[KAl(SO4)2·12H2O]是一种常用的净水剂,写出水解的离子方程式并分析其净水原理______ 、_______ 。
(1)写出铝的原子结构示意图
(2)地壳中含量前三位的元素中,和铝处于同一周期的元素是
(3)铝既能与酸又能与碱发生反应,写出其分别与盐酸、氢氧化钠溶液反应得到的铝盐
(4)铝能和氧化铁发生铝热反应:2Al+Fe2O3
 2Fe+Al2O3,工业上利用该原理来冶炼某些难熔的金属。在该反应中铝的作用是
2Fe+Al2O3,工业上利用该原理来冶炼某些难熔的金属。在该反应中铝的作用是(5)明矾[KAl(SO4)2·12H2O]是一种常用的净水剂,写出水解的离子方程式并分析其净水原理
您最近一年使用:0次
【推荐3】建筑工地常用的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒.已知NaNO2能发生如下反应:NaNO2+HI→NO+I2+NaI+H2O。
(1)配平上述反应方程式_________ ;
(2)上述反应的氧化剂是________ ;
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①水 ②碘化钾淀粉试纸 ③淀粉 ④白酒 ⑤食醋,进行实验,下列几组合适的是________ (填序号)。
A.③⑤
B.①②④
C.①②⑤
D.①②③⑤
(4)某厂废切削液中,含有2%~5%的NaNO2,直接排放会造成污染,采用NH4Cl,能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为________ ;该反应中被氧化的元素是________ 。
(1)配平上述反应方程式
(2)上述反应的氧化剂是
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①水 ②碘化钾淀粉试纸 ③淀粉 ④白酒 ⑤食醋,进行实验,下列几组合适的是
A.③⑤
B.①②④
C.①②⑤
D.①②③⑤
(4)某厂废切削液中,含有2%~5%的NaNO2,直接排放会造成污染,采用NH4Cl,能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为
您最近一年使用:0次



