某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合K时,观察到电流表的指针发生了偏移。
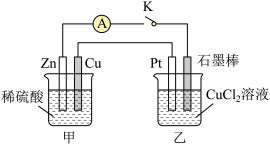
请回答下列问题:
(1)甲装置的名称是________ ;乙装置的名称是________ ;Zn极为________ 极;Pt极为______ 极。
(2)写出电极反应式:Cu极_____________ ;石墨棒极____________ 。
(3)当甲中产生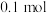 气体时,乙中析出铜的质量应为
气体时,乙中析出铜的质量应为________ ;乙中产生的气体在标准状况下的体积应为________ 。
(4)若乙中溶液不变,将其电极都换成铜电极,闭合K一段时间后,乙中溶液的颜色________ (填“变深”、“变浅”或“无变化”)。
(5)若乙中电极不变,将其溶液换成 溶液,闭合K一段时间后,甲中溶液的pH将
溶液,闭合K一段时间后,甲中溶液的pH将________ (填“增大”、“减小”或“不变”,下同);乙中溶液的pH将_______ 。
(6)若乙中电极不变,将其溶液换成饱和 溶液,闭合K一段时间,当阴极上有
溶液,闭合K一段时间,当阴极上有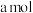 气体生成时,同时有
气体生成时,同时有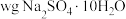 析出,假设温度不变,剩余溶液中溶质的质量分数应为
析出,假设温度不变,剩余溶液中溶质的质量分数应为_____ (用含w、a的代数式表示,不必化简)。

请回答下列问题:
(1)甲装置的名称是
(2)写出电极反应式:Cu极
(3)当甲中产生
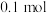 气体时,乙中析出铜的质量应为
气体时,乙中析出铜的质量应为(4)若乙中溶液不变,将其电极都换成铜电极,闭合K一段时间后,乙中溶液的颜色
(5)若乙中电极不变,将其溶液换成
 溶液,闭合K一段时间后,甲中溶液的pH将
溶液,闭合K一段时间后,甲中溶液的pH将(6)若乙中电极不变,将其溶液换成饱和
 溶液,闭合K一段时间,当阴极上有
溶液,闭合K一段时间,当阴极上有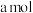 气体生成时,同时有
气体生成时,同时有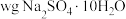 析出,假设温度不变,剩余溶液中溶质的质量分数应为
析出,假设温度不变,剩余溶液中溶质的质量分数应为
更新时间:2019/12/16 12:02:35
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。
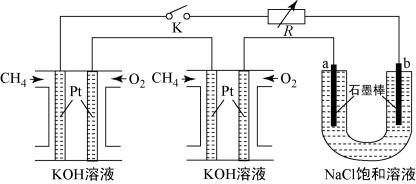
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为_______________ 、_______________ 。
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是_____ ,电解氯化钠溶液的总反应方程式为____________________________ ;
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为
_____ (法拉第常数F=9.65×l04C.mol-1,列式计算),最多能产生的氯气体积为___ L(标准状况)。

回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图是一个电化学过程的示意图,请按要求回答下列问题
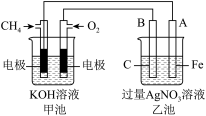
(1)甲池是_______ 装置(填“原电池”或“电解池”)
(2)写出电极反应式:通入CH4的电极_______ 。
(3)反应一段时间后,甲池中消耗1.6g甲烷,则乙池中某电极的质量增_______ g。
(4)反应一段时间后,乙池中溶液成分发生了变化,想要完全恢复到电解前可加入的物质是____
(5)某工厂烟气中主要含SO2,可用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。
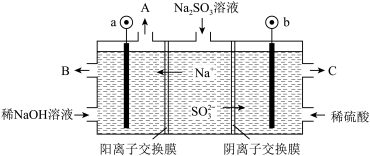
①图中a极要连接电源的_______ (填“正”或“负”)极,C口流出的物质是_______ 。
② 放电的电极反应式为
放电的电极反应式为_______ 。

(1)甲池是
(2)写出电极反应式:通入CH4的电极
(3)反应一段时间后,甲池中消耗1.6g甲烷,则乙池中某电极的质量增
(4)反应一段时间后,乙池中溶液成分发生了变化,想要完全恢复到电解前可加入的物质是
(5)某工厂烟气中主要含SO2,可用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。

①图中a极要连接电源的
②
 放电的电极反应式为
放电的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】为探究原电池和电解池的工作原理,某研究性小组分别用如图所示装置进行实验。
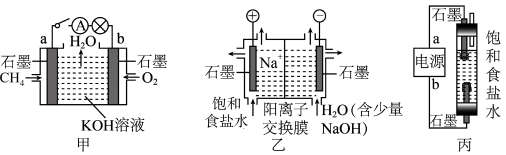
(1)甲装置中,a电极的反应式为_____ 。
(2)乙装置中,阴极区产物为_____ 。
(3)丙装置是一种家用84消毒液(NaClO)发生器。外接电源a为_____ (填“正”或“负”)极,该装置内发生反应的化学方程式为_____ 、_____ 。
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为_____ (不考虑气体的溶解)。
(5)某工厂采用电解法处理含 的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水,
的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水, 被还原成为Cr3+,Cr3+在阴极区生成Cr(OH)3沉淀除去,工作原理如图。
被还原成为Cr3+,Cr3+在阴极区生成Cr(OH)3沉淀除去,工作原理如图。
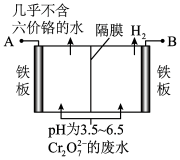
①写出电解时阴极的电极反应式____ 。
②写出 被还原为Cr3+的离子方程式
被还原为Cr3+的离子方程式____ 。

(1)甲装置中,a电极的反应式为
(2)乙装置中,阴极区产物为
(3)丙装置是一种家用84消毒液(NaClO)发生器。外接电源a为
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为
(5)某工厂采用电解法处理含
 的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水,
的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水, 被还原成为Cr3+,Cr3+在阴极区生成Cr(OH)3沉淀除去,工作原理如图。
被还原成为Cr3+,Cr3+在阴极区生成Cr(OH)3沉淀除去,工作原理如图。
①写出电解时阴极的电极反应式
②写出
 被还原为Cr3+的离子方程式
被还原为Cr3+的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】依据电化学知识,解决下列问题:
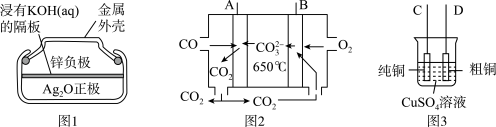
(1)图1为锌银电池,负极是Zn,正极是Ag2O,电解质是KOH。写出该电池负极电极反应式:___ ,电池工作时,正极区周围溶液的pH___ (填“增大”、“减小”、“不变”)。
(2)图2是一种新型燃料电池,以CO为燃料,一定比例的Li2CO3和Na2CO3的熔融混合物为电解质,图3是粗铜精炼的装置图,现用该燃料电池为电源进行粗铜的精炼实验。
①写出A极的电极反应式:___ 。
②要用燃料电池为电源进行粗铜的精炼实验,则B极应该与__ 极(填“C”或“D”)相连。
③当消耗标准状况下2.24LO2时,C电极的质量变化为___ 。

(1)图1为锌银电池,负极是Zn,正极是Ag2O,电解质是KOH。写出该电池负极电极反应式:
(2)图2是一种新型燃料电池,以CO为燃料,一定比例的Li2CO3和Na2CO3的熔融混合物为电解质,图3是粗铜精炼的装置图,现用该燃料电池为电源进行粗铜的精炼实验。
①写出A极的电极反应式:
②要用燃料电池为电源进行粗铜的精炼实验,则B极应该与
③当消耗标准状况下2.24LO2时,C电极的质量变化为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】1929年,吴蕴初先生在上海创建了天原化工厂,它是中国最早的氯碱工业。下图给出了部分生产流程:
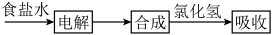
(1)写出电解饱和食盐水的化学方程式___________ ,阳极产生的气体如何检验?___________ 。工业上常用电解生成的产物氯气和氢气燃烧的方法制取氯化氢气体,写出 溶于水后电离方程式
溶于水后电离方程式___________ 。
(2)实验测得产生的氢气体积(已折算成标准状况)为5.60mL,电解后溶液的体积恰好为50.0mL,则溶液中 的浓度为
的浓度为___________ 。
(3)实际生产中使用的盐往往含有一些杂质,在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的 、
、 、
、 及泥沙,可将粗盐溶于水,然后进行下列五项操作,①过滤②加过量的
及泥沙,可将粗盐溶于水,然后进行下列五项操作,①过滤②加过量的 溶液 ③加适量的盐酸④加过量的
溶液 ③加适量的盐酸④加过量的 溶液⑤加过量的
溶液⑤加过量的 溶液,操作正确的顺序是___________(选填字母)。
溶液,操作正确的顺序是___________(选填字母)。
(4)新制的氯水中存在多种微粒。
①将氯气溶于水后制得氯水,新制的氯水显浅黄绿色,说明氯水中有___________ (填微粒符号)存在。
②向氯水中滴加硝酸银溶液,有白色沉淀生成,证明氯水中含___________ (填微粒符号)。
③用pH计测出,氯水的 ,说明了氯水中含
,说明了氯水中含___________ (填微粒符号)。
(5)工业上通常把氯气通入石灰乳中可以制得漂粉精,其中有效成份为___________ (写名称),漂粉精可用于游泳池中水的消毒,原因是(用化学方程式表示):___________ 。

(1)写出电解饱和食盐水的化学方程式
 溶于水后电离方程式
溶于水后电离方程式(2)实验测得产生的氢气体积(已折算成标准状况)为5.60mL,电解后溶液的体积恰好为50.0mL,则溶液中
 的浓度为
的浓度为(3)实际生产中使用的盐往往含有一些杂质,在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的
 、
、 、
、 及泥沙,可将粗盐溶于水,然后进行下列五项操作,①过滤②加过量的
及泥沙,可将粗盐溶于水,然后进行下列五项操作,①过滤②加过量的 溶液 ③加适量的盐酸④加过量的
溶液 ③加适量的盐酸④加过量的 溶液⑤加过量的
溶液⑤加过量的 溶液,操作正确的顺序是___________(选填字母)。
溶液,操作正确的顺序是___________(选填字母)。| A.①④②⑤③ | B.④⑤②①③ | C.②⑤④①③ | D.⑤②④③① |
(4)新制的氯水中存在多种微粒。
①将氯气溶于水后制得氯水,新制的氯水显浅黄绿色,说明氯水中有
②向氯水中滴加硝酸银溶液,有白色沉淀生成,证明氯水中含
③用pH计测出,氯水的
 ,说明了氯水中含
,说明了氯水中含(5)工业上通常把氯气通入石灰乳中可以制得漂粉精,其中有效成份为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图中,甲是电解氯化钠溶液,乙是铜的电解精炼,丙是电镀,回答:
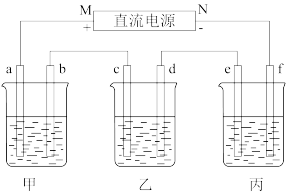
(1)a极上的电极反应式为_______ 。
(2)在粗铜的电解过程中,图中c电极的材料是_______  填“粗铜板”或“纯铜板”
填“粗铜板”或“纯铜板” ;在 d电极上发生的电极反应为
;在 d电极上发生的电极反应为 _______ 。
(3)如果要在铁制品上镀镍 二价金属
二价金属 ,则 e电极的材料是
,则 e电极的材料是 _______  填“铁制品”或“镍块”)。
填“铁制品”或“镍块”)。
(4)用人工光合作用得到的甲醇 、氧气和稀硫酸制作燃料电池,则甲醇应通入该燃料电池的
、氧气和稀硫酸制作燃料电池,则甲醇应通入该燃料电池的_______ 极 填“正”或“负”
填“正”或“负” ,通入氧气一极的电极反应式:
,通入氧气一极的电极反应式:_______

(1)a极上的电极反应式为
(2)在粗铜的电解过程中,图中c电极的材料是
 填“粗铜板”或“纯铜板”
填“粗铜板”或“纯铜板” ;在 d电极上发生的电极反应为
;在 d电极上发生的电极反应为 (3)如果要在铁制品上镀镍
 二价金属
二价金属 ,则 e电极的材料是
,则 e电极的材料是  填“铁制品”或“镍块”)。
填“铁制品”或“镍块”)。(4)用人工光合作用得到的甲醇
 、氧气和稀硫酸制作燃料电池,则甲醇应通入该燃料电池的
、氧气和稀硫酸制作燃料电池,则甲醇应通入该燃料电池的 填“正”或“负”
填“正”或“负” ,通入氧气一极的电极反应式:
,通入氧气一极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)双极膜(BP)是一种能将水分子解离为 和
和 的特殊离子交换膜。应用双极膜制取聚合硫酸铁净水剂
的特殊离子交换膜。应用双极膜制取聚合硫酸铁净水剂 (简称PFS)的电化学装置如图所示。回答下列问题:
(简称PFS)的电化学装置如图所示。回答下列问题:_________ 。
②M为_________ (填“阴离子”或“阳离子”)交换膜,图中甲是_________ (填“ ”或“
”或“ ”)。
”)。
③电流过大,会使PFS产品的纯度降低,原因可能是_________ 。
(2)工业上常用连二亚硫酸钠 消除烟气中的
消除烟气中的 ,通过电解可使
,通过电解可使 再生,装置如图所示。吸收塔内发生的离子反应方程式为
再生,装置如图所示。吸收塔内发生的离子反应方程式为_________ 。吸收塔内每吸收11.2L的 ,理论上
,理论上 电极上会放出
电极上会放出_________ L气体(体积均为标准状况)。
(1)双极膜(BP)是一种能将水分子解离为
 和
和 的特殊离子交换膜。应用双极膜制取聚合硫酸铁净水剂
的特殊离子交换膜。应用双极膜制取聚合硫酸铁净水剂 (简称PFS)的电化学装置如图所示。回答下列问题:
(简称PFS)的电化学装置如图所示。回答下列问题: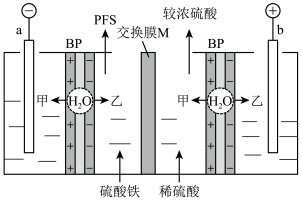
②M为
 ”或“
”或“ ”)。
”)。③电流过大,会使PFS产品的纯度降低,原因可能是
(2)工业上常用连二亚硫酸钠
 消除烟气中的
消除烟气中的 ,通过电解可使
,通过电解可使 再生,装置如图所示。吸收塔内发生的离子反应方程式为
再生,装置如图所示。吸收塔内发生的离子反应方程式为 ,理论上
,理论上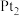 电极上会放出
电极上会放出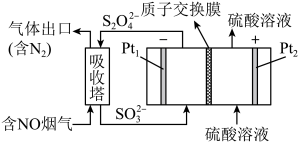
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】利用所学电化学反应原理,解决以下问题:
Ⅰ.如图所示,A为电源,B为浸透饱和食盐水和酚酞溶液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液如图所示。
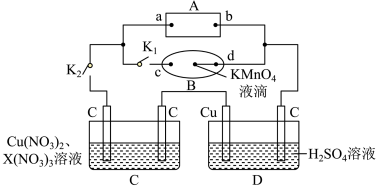
(1)闭合K1,断开K2,通电后,d端显红色,则电源b端为___________ 极,若c、d为惰性电极,检验c端产物的方法为___________ 。滤纸中央KMnO4溶液处发生的现象为___________ 。
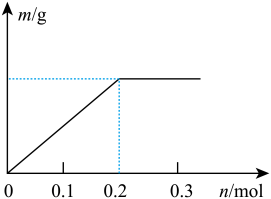
(2)已知C装置中溶液的溶质为Cu(NO3)2和X(NO3)3,且均为0.1mol,打开K1,关闭K2, 通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是___________ 。
(3)D装置中溶液是H2SO4溶液,则电极C端从开始至一段时间后的实验现象是___________ 。
Ⅱ.电化学技术是有效解决 CO、SO2、NOx 等大气污染的重要方法,某兴趣小组以SO2为原料,采用电化学方法制取硫酸,装置如下 :
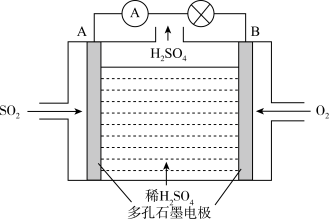
(4)电解质溶液中 离子向
离子向___________ (填“A极”或“B极” )移动。
(5)请写出负极电极反应式___________ 。
(6)用该原电池做电源,石墨做电极电解2L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24 L(标准状况)气体,假设电解前后溶液体积不变,则电解后溶液中H+的浓度为___________ 。
Ⅰ.如图所示,A为电源,B为浸透饱和食盐水和酚酞溶液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液如图所示。

(1)闭合K1,断开K2,通电后,d端显红色,则电源b端为
(2)已知C装置中溶液的溶质为Cu(NO3)2和X(NO3)3,且均为0.1mol,打开K1,关闭K2, 通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是

(3)D装置中溶液是H2SO4溶液,则电极C端从开始至一段时间后的实验现象是
Ⅱ.电化学技术是有效解决 CO、SO2、NOx 等大气污染的重要方法,某兴趣小组以SO2为原料,采用电化学方法制取硫酸,装置如下 :

(4)电解质溶液中
 离子向
离子向(5)请写出负极电极反应式
(6)用该原电池做电源,石墨做电极电解2L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24 L(标准状况)气体,假设电解前后溶液体积不变,则电解后溶液中H+的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表中阿拉伯数字(1、2……)是元素周期表中行或列的序号。请参照元素A~I在周期表中的位置,回答下列问题。
(1)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1∶1和1∶2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素以原子个数之比为1∶1和1∶2形成两种离子化合物Z和M。写出Z与Y反应的化学方程式:_______ 。
(2)I元素在周期表中的位置是第_______ 周期、第_______ 族。
(3)实验室中采用下图所示装置模拟工业上同时制取元素A和I的单质的过程。
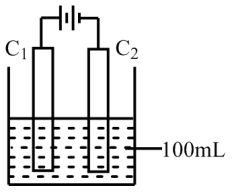
①写出电极C1上发生反应的电极反应式_______ 。
②当电极上产生112 mL(标准状况)元素I的单质气体时(假设气体完全逸出,溶液体积不变),烧杯中溶液的pH=_______ 。(Kw=1.0×10-14)
纵行 横行 | 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18 |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I |
(1)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1∶1和1∶2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素以原子个数之比为1∶1和1∶2形成两种离子化合物Z和M。写出Z与Y反应的化学方程式:
(2)I元素在周期表中的位置是第
(3)实验室中采用下图所示装置模拟工业上同时制取元素A和I的单质的过程。

①写出电极C1上发生反应的电极反应式
②当电极上产生112 mL(标准状况)元素I的单质气体时(假设气体完全逸出,溶液体积不变),烧杯中溶液的pH=
您最近一年使用:0次



