(1)绿色植物是空气天然的“净化器”,在家里科学选种一些绿色植物,可以达到净化空气、吸收有害物质的作用。科学研究发现,1公顷柳杉每月可以吸收160 kg SO2,则1公顷柳杉每月吸收的SO2的物质的量为________ 。
(2)铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混合、压制,就可以制成不同型号的铅笔芯。如果某铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为1 mg。那么一个铅笔字含有的碳原子数约为________ 。
(3)吸食“摇头丸”会严重破坏人体的中枢神经,“摇头丸”的化学式为C9H13N,请计算:
①“摇头丸”的摩尔质量为________ ;
②某毒枭被查获带有270 g“摇头丸”,该毒枭所带的“摇头丸”的物质的量为________ 。
(4)将14.3 g Na2CO3·10H2O固体溶于水配成250 mL溶液,则所得溶液物质的量浓度是________ 。
(2)铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混合、压制,就可以制成不同型号的铅笔芯。如果某铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为1 mg。那么一个铅笔字含有的碳原子数约为
(3)吸食“摇头丸”会严重破坏人体的中枢神经,“摇头丸”的化学式为C9H13N,请计算:
①“摇头丸”的摩尔质量为
②某毒枭被查获带有270 g“摇头丸”,该毒枭所带的“摇头丸”的物质的量为
(4)将14.3 g Na2CO3·10H2O固体溶于水配成250 mL溶液,则所得溶液物质的量浓度是
更新时间:2019-12-23 16:15:10
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】(1)12.4 g Na2X含有0.4 mol Na+,Na2X的摩尔质量为_____ ,其相对分子质量为______ ,X的相对原子质量为________ ,该物质的化学式为________ 。
(2)相同状况下,一定体积的气态氢化物HmX的质量是等体积NH3的2倍。则X的相对原子质量为________ 。
(3)a个X原子的总质量为bg,则X的相对原子质量可表示为________ 。
(4)20 g A物质和14 g B物质完全反应,生成8.8 g C物质、3.6 g D物质和0.2 mol E物质,则E物质的摩尔质量为________ 。
(2)相同状况下,一定体积的气态氢化物HmX的质量是等体积NH3的2倍。则X的相对原子质量为
(3)a个X原子的总质量为bg,则X的相对原子质量可表示为
(4)20 g A物质和14 g B物质完全反应,生成8.8 g C物质、3.6 g D物质和0.2 mol E物质,则E物质的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为________ ,R的相对原子质量为________ 。含R的质量为1.6 g的Na2R,其物质的量为________ 。
(2)86.4gA单质与4.80molCl2完全反应,生成3.20molAClx,则x=___________ ,A的摩尔质量为__________________ g·mol-1
(2)86.4gA单质与4.80molCl2完全反应,生成3.20molAClx,则x=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)分子数为0.5NA的CO2的质量是______ g。
(2)在标准状况下,由CO和CO2组成的混合气体4.48L,质量是8g,此混合气体的平均摩尔质量是______ 。
(2)在标准状况下,由CO和CO2组成的混合气体4.48L,质量是8g,此混合气体的平均摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】标准状态下质量比为14 :15的N2和NO气体,N2和NO的物质的量之比为____________ ,密度之比为______________ 如将其混合氮原子和氧原子的个数比为_________________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】设NA表示阿伏伽德罗常数的值。回答下列问题:
(1)0.3mol NH3分子中所含原子数与__________ 个H2O分子中所含原子数相等。
(2)含0.4mol Al3+的Al2(SO4)3中所含的 的物质的量是
的物质的量是__________
(3)—定条件下,16g A和20g B恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为__________
(4)某混合盐溶液中含有离子:Na+、Mg2+、Cl-、 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为: 0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(
,测得Na+、Mg2+和Cl-的物质的量浓度依次为: 0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c( ) =
) =__________ 。
(1)0.3mol NH3分子中所含原子数与
(2)含0.4mol Al3+的Al2(SO4)3中所含的
 的物质的量是
的物质的量是(3)—定条件下,16g A和20g B恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为
(4)某混合盐溶液中含有离子:Na+、Mg2+、Cl-、
 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为: 0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(
,测得Na+、Mg2+和Cl-的物质的量浓度依次为: 0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c( ) =
) =
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】物质的量是高中化学计算的核心:
(1)相同物质的量的NH3和H2S的质量比___ ,分子个数比为____ ,同温同压下的体积比___ ,所含氢原子的个数比为_____ 。
(2)现有mg某气体,它的一个分子由四原子构成,它的摩尔质量为Mg·mol-1。设阿伏伽德罗常数为NA,则:①该气体的物质的量为____ mol。②该气体中所含的原子总数为_____ 个。
(1)相同物质的量的NH3和H2S的质量比
(2)现有mg某气体,它的一个分子由四原子构成,它的摩尔质量为Mg·mol-1。设阿伏伽德罗常数为NA,则:①该气体的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)标准状况下的甲烷和一氧化碳的混合气体8.96 L,其质量是7.60 g,则混合气体中甲烷的体积为________ ,一氧化碳的质量为_______ 。
(2)现有CO、CO2的混合气体,根据下列条件回答问题
①若该混合气体在标准状况下的密度为1.79 g/L,则混合气体中CO的体积分数为__________ 。
②若标准状况下,2.24 L该混合气体的质量为4 g,则混合气体中CO和CO2的物质的量之比为_________ 。
(3)一定量的甲烷在O2不足的情况下燃烧,得到CO、CO2和H2O的总质量是7.2 g,若其中水的质量为3.6 g,则CO的质量是_________ 。
(4)在一定条件下,某固体化合物X受热分解方程式为: 2X = A↑+2B↑+3C↑,测得反应后生成的混合气体对H2的相对密度为11。在相同条件下,X的相对分子质量是_____________ 。
(2)现有CO、CO2的混合气体,根据下列条件回答问题
①若该混合气体在标准状况下的密度为1.79 g/L,则混合气体中CO的体积分数为
②若标准状况下,2.24 L该混合气体的质量为4 g,则混合气体中CO和CO2的物质的量之比为
(3)一定量的甲烷在O2不足的情况下燃烧,得到CO、CO2和H2O的总质量是7.2 g,若其中水的质量为3.6 g,则CO的质量是
(4)在一定条件下,某固体化合物X受热分解方程式为: 2X = A↑+2B↑+3C↑,测得反应后生成的混合气体对H2的相对密度为11。在相同条件下,X的相对分子质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)100 mL0.3 mol·L-1 Na2SO4溶液和50 mL0.2 mol·L-1Al2(SO4)3溶液混合后,溶液中 的物质的量浓度约为
的物质的量浓度约为___ (忽略溶液体积变化)。
(2)某结晶水合物的化学式为A·nH2O,其相对分子质量为M,在25℃时,a g晶体溶于b g水中即达饱和,形成密度为ρ g·mL-1的溶液,饱和溶液的物质的量浓度为___ 。
 的物质的量浓度约为
的物质的量浓度约为(2)某结晶水合物的化学式为A·nH2O,其相对分子质量为M,在25℃时,a g晶体溶于b g水中即达饱和,形成密度为ρ g·mL-1的溶液,饱和溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】请按要求,回答下列问题:
(1)相同物质的量的SO2和SO3,所含O的质量之比为________ 。
(2)标准状况下,4.48 L 的NH3中,所含H的数目约为________ 。
(3)标准状况下,1 mol H2O、11.2 L CH 4、8 g O2中,体积最小的是________ 。
(4)某气体的质量为3.4 g,含有6.02×1022个分子,则该气体的摩尔质量为________ 。
(5)10 mL 0.5 mol·L-1 Al (NO3)3 溶液中NO3-的物质的量浓度为________ 。
(6)标准状况下,89.6 L HCl 气体溶于1 L水(ρ = 1 g·mL-1)中,所得盐酸的密度为1.146 g·mL-1,则此盐酸的物质的量浓度为________ 。
(1)相同物质的量的SO2和SO3,所含O的质量之比为
(2)标准状况下,4.48 L 的NH3中,所含H的数目约为
(3)标准状况下,1 mol H2O、11.2 L CH 4、8 g O2中,体积最小的是
(4)某气体的质量为3.4 g,含有6.02×1022个分子,则该气体的摩尔质量为
(5)10 mL 0.5 mol·L-1 Al (NO3)3 溶液中NO3-的物质的量浓度为
(6)标准状况下,89.6 L HCl 气体溶于1 L水(ρ = 1 g·mL-1)中,所得盐酸的密度为1.146 g·mL-1,则此盐酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】物质的量是宏观量与微观量相互联系的桥梁,回答下列问题。
(1)等质量的 和
和 所含分子个数比为
所含分子个数比为___________ ;常温常压下,等体积的 和
和 两种气体所含原子个数比为
两种气体所含原子个数比为___________ ,质量比为___________ 。
(2)将6L标准状况下的氯化氢气体溶于100mL水中(水的密度近似为 ),得到密度为
),得到密度为 的盐酸,则该盐酸的物质的量浓度是
的盐酸,则该盐酸的物质的量浓度是___________  (列出计算式)。
(列出计算式)。
(3)铜有两种常见的氧化物CuO和 。某学习小组用电子天平称取
。某学习小组用电子天平称取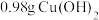 固体,加热至
固体,加热至 完全分解成铜的氧化物,其质量随温度的变化如图所示,计算N点各成分的质量:CuO
完全分解成铜的氧化物,其质量随温度的变化如图所示,计算N点各成分的质量:CuO___________ g,
___________ g。

(1)等质量的
 和
和 所含分子个数比为
所含分子个数比为 和
和 两种气体所含原子个数比为
两种气体所含原子个数比为(2)将6L标准状况下的氯化氢气体溶于100mL水中(水的密度近似为
 ),得到密度为
),得到密度为 的盐酸,则该盐酸的物质的量浓度是
的盐酸,则该盐酸的物质的量浓度是 (列出计算式)。
(列出计算式)。(3)铜有两种常见的氧化物CuO和
 。某学习小组用电子天平称取
。某学习小组用电子天平称取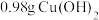 固体,加热至
固体,加热至 完全分解成铜的氧化物,其质量随温度的变化如图所示,计算N点各成分的质量:CuO
完全分解成铜的氧化物,其质量随温度的变化如图所示,计算N点各成分的质量:CuO

您最近一年使用:0次

 的物质的量是
的物质的量是

