(1)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为________ ,R的相对原子质量为________ 。含R的质量为1.6 g的Na2R,其物质的量为________ 。
(2)86.4gA单质与4.80molCl2完全反应,生成3.20molAClx,则x=___________ ,A的摩尔质量为__________________ g·mol-1
(2)86.4gA单质与4.80molCl2完全反应,生成3.20molAClx,则x=
更新时间:2020-01-11 20:31:34
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】相同物质的量的SO2与SO3,其质量之比为___________ ,氧元素的质量之比为___________ ,原子总数之比为___________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】乙酸是实验室常用的一种化学试剂,某乙酸试剂瓶上标签的部分内容如图所示。利用标签提供的信息,回答下列问题:
乙酸 |
(1)乙酸的摩尔质量为
(2)若该乙酸溶液的密度为1.02g/cm3,求此乙酸溶液的物质的量浓度是多少
(3)某实验中要用3mol·L-1的乙酸溶液204mL,需要取用上述乙酸溶液多少毫升
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】同温同压下,相同质量的一氧化碳和二氧化碳气体:
①它们的密度比是_______ ;②它们的体积比是_______ ;③它们所含氧元素的质量比是_______ ;④它们的原子个数比是_______ 。
若改为同温同压同体积下的一氧化碳和二氧化碳气体:
①它们的质量比是_______ ;②它们的密度比是_______ ;③它们的分子数比是_______ ;④它们的压强比是_______ 。
①它们的密度比是
若改为同温同压同体积下的一氧化碳和二氧化碳气体:
①它们的质量比是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)某气体氧化物的化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为___________ ,R的相对原子质量为___________ 。
(2)标准状况下有① ,②
,② 个
个 分子,③
分子,③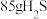 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是___________ (填序号)。
(3)某混合盐溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
___________  。
。
(4)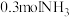 中含有质子数与
中含有质子数与___________ 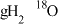 分子中所含质子数相等。
分子中所含质子数相等。
(5) 溶液中
溶液中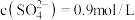 ,则
,则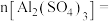
___________ 。
(1)某气体氧化物的化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为(2)标准状况下有①
 ,②
,② 个
个 分子,③
分子,③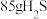 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是(3)某混合盐溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
 。
。(4)
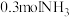 中含有质子数与
中含有质子数与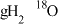 分子中所含质子数相等。
分子中所含质子数相等。(5)
 溶液中
溶液中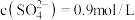 ,则
,则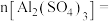
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】物质的量在计算中的应用
(1)有等质量的两气体O3和 O2 ,同温同压下的密度之比为______ 。
(2)有7.8gNa2R含Na+为0.2mol,则Na2R的摩尔质量为_____ ,R的相对原子质量为___ 。
(3)质量比为51:32:34的NH3、CH4、H2S,其物质的量之比为___ ,它们所含氢原子数之比为__ ,所含质子数之比为___ 。
(4)在150°C,m gNH4HCO3固体完全分解生成NH3、CO2、H2O,若所得混合气体对H2的相对密度为d,则用含m、d的代数式表示混合气体的物质的量为_________ 。
(5)某市售盐酸的质量分数为36.5%,密度为1.18g/cm3,该盐酸的物质的量浓度为_______ 。
(1)有等质量的两气体O3和 O2 ,同温同压下的密度之比为
(2)有7.8gNa2R含Na+为0.2mol,则Na2R的摩尔质量为
(3)质量比为51:32:34的NH3、CH4、H2S,其物质的量之比为
(4)在150°C,m gNH4HCO3固体完全分解生成NH3、CO2、H2O,若所得混合气体对H2的相对密度为d,则用含m、d的代数式表示混合气体的物质的量为
(5)某市售盐酸的质量分数为36.5%,密度为1.18g/cm3,该盐酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某液体化合物X2Y4,常用做火箭燃料。16g X2Y4在一定量的O2中恰好完全燃烧,反应方程式为X2Y4(l)+O2(g)=X2(g)+2Y2O(l)。冷却后标准状况下测得生成物的体积为11.2 L,其密度为1.25g/L,则:
(1)反应前O2的体积V(O2)为________ 。
(2)X2的摩尔质量为________ ;Y元素的名称是________ 。
(3)若反应生成0.1mol X2,则转移电子的物质的量为________ mol。
(1)反应前O2的体积V(O2)为
(2)X2的摩尔质量为
(3)若反应生成0.1mol X2,则转移电子的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】(1)6.02×1023个氢氧根离子的物质的量是________ mol,其摩尔质量为________ 。
(2)3.01×1023个H2O的物质的量为________ mol,其中,所有原子的物质的量为________ mol,所含电子的物质的量为________ mol。
(3)标准状况下,2 mol O2 的体积是________ ;标准状况下,11.2 L O2的质量是________ 含有的氧气分子数目是________ ;含有的氧原子数目是________ 。
(2)3.01×1023个H2O的物质的量为
(3)标准状况下,2 mol O2 的体积是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】化学计量在化学中占有重要地位,请回答下列问题。
(1)含0.4 mol Al3+的Al2(SO4)3中所含的 的物质的量是
的物质的量是__________ 。
(2)0.3 mol NH3分子中所含原子数与_______ mol H2O分子中所含原子数相等。
(3)现有质量比为22:14的CO2和CO的混合气体,则该混合气体中的CO2和CO物质的量之比为________ ,碳原子和氧原子的个数比为_________ 。
(4)现有12.0 g O2和CO2的混合气体,在标准状况下所占体积约为6.72 L。则混合气体中O2与CO2的体积比为:______ 。
(1)含0.4 mol Al3+的Al2(SO4)3中所含的
 的物质的量是
的物质的量是(2)0.3 mol NH3分子中所含原子数与
(3)现有质量比为22:14的CO2和CO的混合气体,则该混合气体中的CO2和CO物质的量之比为
(4)现有12.0 g O2和CO2的混合气体,在标准状况下所占体积约为6.72 L。则混合气体中O2与CO2的体积比为:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)5.4 g H2O的物质的量是_____ ,含有_________ 个水分子(用NA表示),含有____ mol H。
(2)11.2L NH3(标况)约含_____ mol氢原子,_____ g的氮原子。
(3)6.02×1022个OH− 的质量为____ ,含有质子的物质的量为_____ ,含有电子的物质的量为__ 。
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ 。含R的质量为1.6 g的Na2R,其物质的量为________ 。
(5)物质的量相同的CO2和O2,其所含原子数目之比为_____ ,所含氧原子数目之比为______ ;质量相同的CO2和O2,其物质的量之比为_________ 。
(2)11.2L NH3(标况)约含
(3)6.02×1022个OH− 的质量为
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(5)物质的量相同的CO2和O2,其所含原子数目之比为
您最近一年使用:0次




