下列说法正确的是
下列图示与对应的叙述符合的是

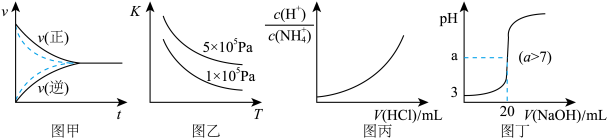
下列图示与对应的叙述符合的是
| A.图甲实线、虚线分别表示某可逆反应未使用催化剂和使用催化剂的正、逆反应速率随时间的变化 |
B.图乙表示反应2SO2(g)+O2(g)  2SO3(g)△H<0的平衡常数K与温度和压强的关系 2SO3(g)△H<0的平衡常数K与温度和压强的关系 |
C.图丙表示向0.1mol/L的NH4Cl溶液中滴加0.1mol/L的HCl溶液时,溶液中 随HCl溶液体积变化关系 随HCl溶液体积变化关系 |
| D.图丁表示常温下向20mL pH=3的醋酸中滴加pH=11的NaOH溶液,溶液的pH随NaOH溶液体积的变化关系 |
2017·江苏南通·三模 查看更多[9]
江西省鄱阳县第一中学2019-2020学年高二上学期第二次检测化学试题(已下线)【南昌新东方】江西省九江第一中学2017-2018学年高二上学期期末考试化学试题江西省上饶市2018-2019学年高二下学期期末教学质量测试化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——水的电离及溶液的酸碱性江西省吉安市吉水二中、新干二中、吉安县二中、永丰二中、泰和二中五校2019-2020学年高二期中联考化学试题河北安平中学2020届高三上学期第二次月考化学试题【校级联考】江西省吉安市几所重点中学2018-2019学年高二上学期联考化学试题江西省九江第一中学2017-2018学年高二上学期期末考试化学试题江苏省南通、扬州、泰州市2017届高三第三次模拟考试化学试题
更新时间:2019-12-23 15:50:45
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某化学科研小组研究在其他条件不变时,改变某一条件对3A2(g)+B2(g)⇌2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据右图可得出的判断结论正确的


| A.a、b、c三点平衡常数的大小关系为:Kb>Kc >Ka |
| B.达到平衡时B2的转化率大小为:b>a>c |
| C.增大压强有利于AB3的生成,因此在实际生产中压强越大越好 |
D.若起始量为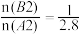 ,则在T2温度下,平衡时AB3的体积分数接近b点 ,则在T2温度下,平衡时AB3的体积分数接近b点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
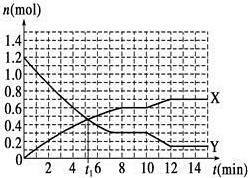
【推荐2】一定条件下,在体积为10 L的固定容器中发生反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,反应过程如图,下列说法正确的是
2NH3(g) ΔH<0,反应过程如图,下列说法正确的是
 2NH3(g) ΔH<0,反应过程如图,下列说法正确的是
2NH3(g) ΔH<0,反应过程如图,下列说法正确的是 
| A.t1 min时正、逆反应速率相等 |
| B.Y曲线表示N2的物质的量随时间变化的关系 |
| C.8 min时的平衡常数与12min时平衡常数相等 |
| D.10~12 min,升高温度使反应速率加快,平衡正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
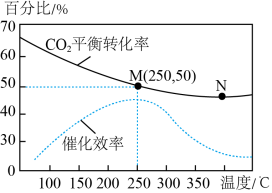
【推荐1】一定条件下合成乙烯: 6 H2(g) +2CO2(g) CH2=CH2(g) +4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是
CH2=CH2(g) +4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是
 CH2=CH2(g) +4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是
CH2=CH2(g) +4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是
| A.生成乙烯的速率:v(M)一定小于v(N) |
| B.化学平衡常数:KN>K M |
| C.当温度高于250℃时,升高温度,平衡向逆反应方向移动,从而使催化剂的催化效率降低 |
| D.若投料比n(H2):n(CO2)=3:1,则图中M点时,乙烯的体积分数为7.7% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在密闭容器中发生如下反应: 。反应达平衡后,保持温度不变,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡时的1.8倍。下列叙述正确的是
。反应达平衡后,保持温度不变,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡时的1.8倍。下列叙述正确的是
 。反应达平衡后,保持温度不变,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡时的1.8倍。下列叙述正确的是
。反应达平衡后,保持温度不变,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡时的1.8倍。下列叙述正确的是A. |
| B.W的体积分数增大 |
| C.平衡向逆反应方向移动 |
| D.该反应的化学平衡常数逐渐增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知:[FeCl4(H2O)2]-为黄色,下列实验所得结论不正确 的是( )

注:加热为微热,忽略体积变化。

注:加热为微热,忽略体积变化。
| A.实验①中,Fe2(SO4)3溶液显浅黄色原因是Fe3+水解产生了少量Fe(OH)3 |
| B.实验②中,酸化对Fe3+水解的影响程度大于温度的影响 |
C.实验③中,存在可逆反应: Fe3+ + 4Cl-+ 2H2O  [FeCl4(H2O)2]- [FeCl4(H2O)2]- |
| D.实验④,可证明升高温度,Fe3+水解平衡正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关说法正确的是
A.反应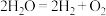 在任何条件下都不会自发进行 在任何条件下都不会自发进行 |
B.溶液 加水稀释后,溶液中 加水稀释后,溶液中 的值减小 的值减小 |
| C.温度升高,反应物的活化分子数增多,主要因素是分子的运动加快,反应速率加快 |
D. 液中加入少量 液中加入少量 固体, 固体, 水解程度减小,溶液的pH减小 水解程度减小,溶液的pH减小 |
您最近一年使用:0次

 氧化
氧化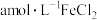 溶液过程中所测的实验数据如图所示。下列分析或推测合理的是。下列分析或推测
溶液过程中所测的实验数据如图所示。下列分析或推测合理的是。下列分析或推测
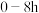 内,
内, 的氧化率随时间延长而逐渐增大
的氧化率随时间延长而逐渐增大 越大,
越大, 时,
时,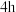 内
内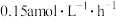
 ;
;
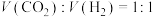 投料比进行反应,平衡时含碳物质体积分数随温度的变化如图所示。
投料比进行反应,平衡时含碳物质体积分数随温度的变化如图所示。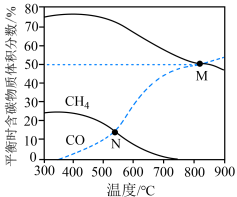
 ,反应II的
,反应II的

 的压强是
的压强是 的3倍
的3倍 投料,则曲线之间交点位置不变
投料,则曲线之间交点位置不变 2NH4++SO42-
2NH4++SO42-

