某种常见的白色晶体A,与盐酸反应产生无刺激性气味的气体B,将B通入澄清石灰水,石灰水变浑浊。若在A的水溶液中加氢氧化钡溶液微热,则析出白色沉淀C和无色气体D,D可以使湿润的红色石蕊试纸变蓝。加热固体A,可生成水、B和D,而且B和D的物质的量之比为1:1。
(1)根据以上事实,可以判断出A是________ ,B是________ ,C是________ 。
(2)加热固体A生成水、B和D的化学方程式是_________________________ ,A与盐酸反应的离子方程式是___________________________________ ,A与氢氧化钡溶液反应的离子方程式是___________________________________________ 。
(1)根据以上事实,可以判断出A是
(2)加热固体A生成水、B和D的化学方程式是
12-13高一上·甘肃白银·期末 查看更多[1]
(已下线)2011-2012学年甘肃省白银市平川中恒学校高一上学期期末考试化学试卷
更新时间:2016-12-09 02:42:16
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
(1)若A为黄绿色气体单质,D为造成“温室效应”的气体之一,则B的化学式为___________ ;
(2)若A为淡黄色粉末,若X为铁粉,铁粉在C中燃烧,其产物D为___________ 。(填化学式)。
(3)若A为金属单质,C俗称烧碱。A与 反应的离子方程式为
反应的离子方程式为___________ 。
(4)若A为 (其中氢元素为
(其中氢元素为 价,
价, 常用作还原剂、生氢剂),C到D为工业生产漂白粉的反应原理。写出漂白粉的有效成分
常用作还原剂、生氢剂),C到D为工业生产漂白粉的反应原理。写出漂白粉的有效成分______ (填化学式);A与 反应化学方程式
反应化学方程式________ 。

(1)若A为黄绿色气体单质,D为造成“温室效应”的气体之一,则B的化学式为
(2)若A为淡黄色粉末,若X为铁粉,铁粉在C中燃烧,其产物D为
(3)若A为金属单质,C俗称烧碱。A与
 反应的离子方程式为
反应的离子方程式为(4)若A为
 (其中氢元素为
(其中氢元素为 价,
价, 常用作还原剂、生氢剂),C到D为工业生产漂白粉的反应原理。写出漂白粉的有效成分
常用作还原剂、生氢剂),C到D为工业生产漂白粉的反应原理。写出漂白粉的有效成分 反应化学方程式
反应化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
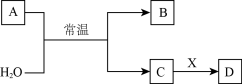
【推荐2】Na3N是科学家制备的新化合物,它可以和水反应生成两种碱性物质,其中一种A可以发生下列转化关系(A、B、C、D为中学常见物质且均含有同一种元素,反应条件及其他物质已经略去):
A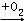 B
B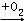 C
C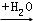 D
D
(1)Na3N中N的化合价为_______ ;
(2)写出Na3N和水反应的化学方程式_______ ;
(3)写出C→D的离子方程式_______ 。
A
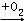 B
B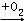 C
C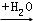 D
D(1)Na3N中N的化合价为
(2)写出Na3N和水反应的化学方程式
(3)写出C→D的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有关物质的转化关系如下图所示(部分物质和条件已略去)。B、C、E是常见气体;A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应;G的焰色反应显黄色;I的溶液呈黄色。
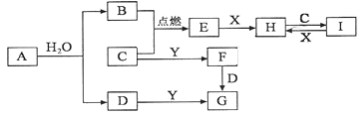
请回答下列问题:
(1)F的化学式为___________ 。
(2)E的电子式为_____________ 。
(3)写出Y和D溶液反应的离子方程式:______________________ 。
(4)写出C与H溶液反应的化学方程式,并用单线桥标出电子转移的方向和数目:______________ 。

请回答下列问题:
(1)F的化学式为
(2)E的电子式为
(3)写出Y和D溶液反应的离子方程式:
(4)写出C与H溶液反应的化学方程式,并用单线桥标出电子转移的方向和数目:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
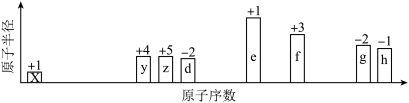
根据判断出的元素回答问题:
(1)f在元素周期表的位置是_____________ 。
(2)比较d、e常见离子的半径大小(用化学式表示,下同)_______ >_________ ;比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______ >__________ 。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式__________ 。
(4)已知1 mol e的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式:_____________________________ 。
(5)上述元素可组成盐R:zx4f(gd4)2,向盛有10 mL1 mol/LR溶液的烧杯中滴加1 mol/LNaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
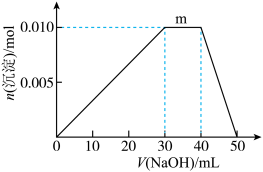
①写出m点反应的离子方程式____________________ 。
②若R溶液改加20 mL1.2 mol/LBa(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为_______ mol。

根据判断出的元素回答问题:
(1)f在元素周期表的位置是
(2)比较d、e常见离子的半径大小(用化学式表示,下同)
(3)任选上述元素组成一种四原子共价化合物,写出其电子式
(4)已知1 mol e的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式:
(5)上述元素可组成盐R:zx4f(gd4)2,向盛有10 mL1 mol/LR溶液的烧杯中滴加1 mol/LNaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:

①写出m点反应的离子方程式
②若R溶液改加20 mL1.2 mol/LBa(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】硫酸铁铵[化学式可表示为NH4Fe(SO4)2]可用作分析试剂等。某兴趣小组利用铁矿石(主要成分为FeO、Fe2O3)制硫酸铁铵的流程如下:
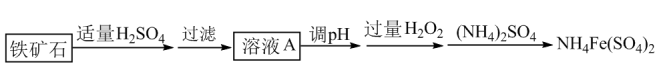
回答下列问题:
(1)溶液A中所含金属阳离子有___________ 。
(2)写出FeO与稀硫酸反应的离子方程式:___________ 。
(3)加入H2O2的作用是___________ 。
(4)若想探究NH4Fe(SO4)2与Ba(OH)2反应生成最大质量沉淀的条件,某同学向含amol NH4Fe(SO4)2的溶液中滴加含bmolBa(OH)2的溶液,与OH—反应的顺序:先是___________ (填离子符号,下同)后是___________ ,当a=b时,发生的离子反应为___________ ,当___________ 时,沉淀的质量达到最大。

回答下列问题:
(1)溶液A中所含金属阳离子有
(2)写出FeO与稀硫酸反应的离子方程式:
(3)加入H2O2的作用是
(4)若想探究NH4Fe(SO4)2与Ba(OH)2反应生成最大质量沉淀的条件,某同学向含amol NH4Fe(SO4)2的溶液中滴加含bmolBa(OH)2的溶液,与OH—反应的顺序:先是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】某固态结晶水合物 X 由 5 种元素组成。某学习小组进行了如下实验

已知气体B具有刺激性气味且能与 AgNO3溶液反应, D 中两种元素质量比为 4:1,请回答:
(1)写出X的组成元素原子序数最大的元素符号_______
(2)检验气体 B 的实验方法是_______
(3)写出 X在隔绝空气条件下加热,生成 A、D、E的化学方程式_______ 。
(4)已知气体 B 和固体D 加热时会发生反应,产物中有两种单质,写出该反应的化学方程式_______ ,当参加反应的 D 质量是 1.2g 时,所生成的两种单质的质量差为_______ g。

已知气体B具有刺激性气味且能与 AgNO3溶液反应, D 中两种元素质量比为 4:1,请回答:
(1)写出X的组成元素原子序数最大的元素符号
(2)检验气体 B 的实验方法是
(3)写出 X在隔绝空气条件下加热,生成 A、D、E的化学方程式
(4)已知气体 B 和固体D 加热时会发生反应,产物中有两种单质,写出该反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】I. 草木灰中含有可溶性钾盐(主要成分是K2SO4、K2CO3、KCl).某学生按下列操作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤,取滤液;③蒸发滤液;④冷却结晶.
(1)在操作①、②、③中均用到玻璃棒,该仪器的作用依次是______ 、______ 、______ .
(2)为检验草木灰中的阴离子,取少量晶体溶于水,并把溶液分成三等份:
①取一份溶液,加入适量盐酸,观察到_____________ ,证明含有碳酸根.
②取另一份溶液,为检验其中是否含有SO42﹣,方法是________ .产生的现象是_____ .
II.有M、N两种溶液,经测定这两种溶液中共含有下列10种离子:Al3+、Cl-、Na+、K+、NO3-、OH-、Fe2+、CO32-、SO42-、H+。
(3)完成下列表格中实验①的结论和实验②的实验内容以及现象:
(4)根据(1)中的实验回答:
NO3-存在于________ 溶液中,理由是_____________________________________ ;
Cl-存在于________ 溶液中,理由是________________________ 。
(5)根据(3)中的实验确定,M溶液中含有的离子___________________________ 。
(1)在操作①、②、③中均用到玻璃棒,该仪器的作用依次是
(2)为检验草木灰中的阴离子,取少量晶体溶于水,并把溶液分成三等份:
①取一份溶液,加入适量盐酸,观察到
②取另一份溶液,为检验其中是否含有SO42﹣,方法是
II.有M、N两种溶液,经测定这两种溶液中共含有下列10种离子:Al3+、Cl-、Na+、K+、NO3-、OH-、Fe2+、CO32-、SO42-、H+。
(3)完成下列表格中实验①的结论和实验②的实验内容以及现象:
| 实验内容以及现象 | 结论 |
| ①取少量N溶液滴加足量的硝酸钡溶液,无沉淀产生 | |
| ② | 确定M溶液中含有Na+,不含K+ |
| ③用pH试纸检测M溶液,pH试纸呈蓝色 |
(4)根据(1)中的实验回答:
NO3-存在于
Cl-存在于
(5)根据(3)中的实验确定,M溶液中含有的离子
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】某无色透明溶液中可能大量存在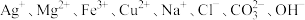 和
和 中的几种.请回答下列问题:
中的几种.请回答下列问题:
(1)不做任何实验就可以判断原溶液中不存在的离子为_______ .
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不溶解,说明原溶液中一定存在的离子是___________________________ ;有关反应的离子方程式为____________________________ .
(3)取(2)中的滤液,逐滴加入过量 溶液,出现白色沉淀,说明原溶液中一定含有
溶液,出现白色沉淀,说明原溶液中一定含有_____________________ ;该过程发生反应的离子方程式为:___________________________ .
(4)该溶液还可能存在的离子是_____________________ .
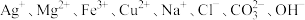 和
和 中的几种.请回答下列问题:
中的几种.请回答下列问题:(1)不做任何实验就可以判断原溶液中不存在的离子为
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不溶解,说明原溶液中一定存在的离子是
(3)取(2)中的滤液,逐滴加入过量
 溶液,出现白色沉淀,说明原溶液中一定含有
溶液,出现白色沉淀,说明原溶液中一定含有(4)该溶液还可能存在的离子是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有一瓶澄清的溶液,其中可能含有NH4+、K+、Ba2+、Al3+、Fe3+、I-、NO3-、CO32-、SO42-、AlO2-。取该溶液进行以下实验:
①用pH试纸检测,溶液呈强酸性;
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色;
③另取溶液适量,逐滴加入NaOH溶液;
a.溶液从酸性变为中性 b.溶液逐渐产生沉淀 c.沉淀完全溶解
d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝
④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)一定存在的离子______________
(2)一定不存在的离子___________________
(3)可能存在的离子___________ ,如何进一步检验该离子 ______________
①用pH试纸检测,溶液呈强酸性;
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色;
③另取溶液适量,逐滴加入NaOH溶液;
a.溶液从酸性变为中性 b.溶液逐渐产生沉淀 c.沉淀完全溶解
d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝
④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)一定存在的离子
(2)一定不存在的离子
(3)可能存在的离子
您最近一年使用:0次



