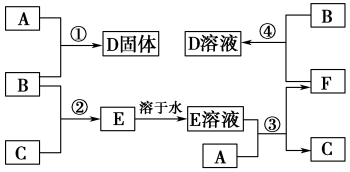
某固态结晶水合物 X 由 5 种元素组成。某学习小组进行了如下实验

已知气体B具有刺激性气味且能与 AgNO3溶液反应, D 中两种元素质量比为 4:1,请回答:
(1)写出X的组成元素原子序数最大的元素符号_______
(2)检验气体 B 的实验方法是_______
(3)写出 X在隔绝空气条件下加热,生成 A、D、E的化学方程式_______ 。
(4)已知气体 B 和固体D 加热时会发生反应,产物中有两种单质,写出该反应的化学方程式_______ ,当参加反应的 D 质量是 1.2g 时,所生成的两种单质的质量差为_______ g。

已知气体B具有刺激性气味且能与 AgNO3溶液反应, D 中两种元素质量比为 4:1,请回答:
(1)写出X的组成元素原子序数最大的元素符号
(2)检验气体 B 的实验方法是
(3)写出 X在隔绝空气条件下加热,生成 A、D、E的化学方程式
(4)已知气体 B 和固体D 加热时会发生反应,产物中有两种单质,写出该反应的化学方程式
更新时间:2023-01-24 14:59:46
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】以下是测定 中结晶水含量的实验流程:
中结晶水含量的实验流程:
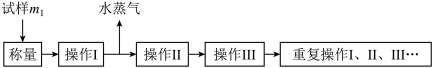
(1) 应放在
应放在___________ (填仪器名称)中加热。
(2)重复操作Ⅰ、Ⅱ、Ⅲ这叫___________ 操作,目的是___________ 。
(3)操作Ⅱ必须要在___________ (填仪器名称)中进行,原因是___________ 。
(4)完成下列表格中数据处理:(保留两位有效数字)
第一次实验: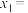
___________ ,第二次实验: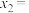
___________ 。两次所测x的平均值为___________ 。
 中结晶水含量的实验流程:
中结晶水含量的实验流程:
(1)
 应放在
应放在(2)重复操作Ⅰ、Ⅱ、Ⅲ这叫
(3)操作Ⅱ必须要在
(4)完成下列表格中数据处理:(保留两位有效数字)
| 第一次实验 | 第二次实验 | |
| 坩埚的质量(g) | 14.520 | 14.670 |
| 坩埚+试样的质量(g) | 17.020 | 18.350 |
| 恒重后,坩埚+硫酸铜的质量(g) | 16.070 | 17.004 |
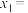
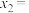
您最近一年使用:0次
【推荐2】化合物X在工业、农业生产中都有重要用途,X由4种常见元素组成,某兴趣小组展开如下实验(气体的体积均在标准状况下测得):

已知:①X的摩尔质量为454g·mol-1;②化合物B常温下是常见的液体;③混合气体C能使品红溶液褪色,气体E能使带火星的木条复燃。
请回答:
(1)白色沉淀F的化学式是___________ ,化合物X的化学式是___________ 。
(2)混合气体C与足量氯水反应的离子方程式为___________ 。
(3)化合物X高温分解的化学方程式为___________ 。
(4)蓝色溶液G 与NaOH溶液发生非氧化还原反应可制得X,化学方程式为___________ 。

已知:①X的摩尔质量为454g·mol-1;②化合物B常温下是常见的液体;③混合气体C能使品红溶液褪色,气体E能使带火星的木条复燃。
请回答:
(1)白色沉淀F的化学式是
(2)混合气体C与足量氯水反应的离子方程式为
(3)化合物X高温分解的化学方程式为
(4)蓝色溶液G 与NaOH溶液发生非氧化还原反应可制得X,化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】一水草酸钙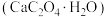 可用作分离稀有金属的载体。回答下列问题:
可用作分离稀有金属的载体。回答下列问题:
(1)制备一水草酸钙的方法如下:
先用精制氯化钙稀溶液与草酸钠溶液共热反应,过滤,将固体溶于热盐酸中;再加氨水反应得一水草酸钙沉淀,过滤,热水洗涤,在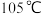 干燥得产品。
干燥得产品。
①已知 溶液的
溶液的 质量浓度为
质量浓度为 ,则该溶液中
,则该溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
②写出上述再加入氨水反应生成一水草酸钙沉淀的化学方程式:___________ 。
(2)为研究一水草酸钙的热分解性质,进行如下实验:准确称取 样品加热,样品的固体残留率
样品加热,样品的固体残留率
 )随温度的变化如下图所示。
)随温度的变化如下图所示。

① 时残留固体的成分为
时残留固体的成分为___________ , 时残留固体的成分为
时残留固体的成分为___________ 。
②已知 时固体的成分为
时固体的成分为 和
和 ,则
,则 的质量为
的质量为___________ g, 的质量为
的质量为___________ g。
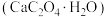 可用作分离稀有金属的载体。回答下列问题:
可用作分离稀有金属的载体。回答下列问题:(1)制备一水草酸钙的方法如下:
先用精制氯化钙稀溶液与草酸钠溶液共热反应,过滤,将固体溶于热盐酸中;再加氨水反应得一水草酸钙沉淀,过滤,热水洗涤,在
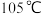 干燥得产品。
干燥得产品。①已知
 溶液的
溶液的 质量浓度为
质量浓度为 ,则该溶液中
,则该溶液中 的物质的量浓度为
的物质的量浓度为②写出上述再加入氨水反应生成一水草酸钙沉淀的化学方程式:
(2)为研究一水草酸钙的热分解性质,进行如下实验:准确称取
 样品加热,样品的固体残留率
样品加热,样品的固体残留率 )随温度的变化如下图所示。
)随温度的变化如下图所示。
①
 时残留固体的成分为
时残留固体的成分为 时残留固体的成分为
时残留固体的成分为②已知
 时固体的成分为
时固体的成分为 和
和 ,则
,则 的质量为
的质量为 的质量为
的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生大量的白烟,D是日常生活中常见的盐(部分反应物和生成物及溶剂水已略去)。

请回答下列问题:
(1)用电子式表示D的形成过程_________________ ;
(2)C的电子式为______________________ ;
(3)写出A溶液和丁反应生成D的离子方程式_________________________________ ;
(4)写出A和E反应的化学方程式_____________________________________ 。.

请回答下列问题:
(1)用电子式表示D的形成过程
(2)C的电子式为
(3)写出A溶液和丁反应生成D的离子方程式
(4)写出A和E反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。
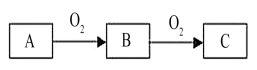
(1)若A是一种黄色单质固体,则B→C的化学方程式为____________________ 。
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为____________ ,试用化学方程式表示该物质与二氧化碳气体的反应___________________ 。将C长期露置于空气中,最后将变成物质D,D的化学式为____________ 。现有D和NaHCO3的固体混合物10 g,加热至质量不再改变,剩余固体质量为9.38 g,D的质量分数为_______ 。
(3)若C是红棕色气体,A可能是一种能使湿润的红色石蕊试纸变蓝的气体。下图是实验室制取A气体的装置,请结合所学知识,回答下列问题:
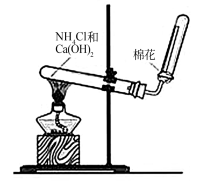
①收集A的方法是_______ ,验证A是否已经收集满的方法是________ (任写一种)。
②写出实验室制取A的化学方程式___________________________ 。
③若有5.35 g氯化铵参加反应,则产生的A气体在标准状况下的体积为______ L。
④试写出C与水反应的化学方程式_____________ ,反应可得到酸X,X是_______ 电解质(填“强”或“弱”)。如下图:足量X的浓溶液与Cu反应,写出烧瓶中发生反应的离子方程式_________ 。实验完毕后,试管中收集到的气体的主要成分为____ (写化学式)。


(1)若A是一种黄色单质固体,则B→C的化学方程式为
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为
(3)若C是红棕色气体,A可能是一种能使湿润的红色石蕊试纸变蓝的气体。下图是实验室制取A气体的装置,请结合所学知识,回答下列问题:

①收集A的方法是
②写出实验室制取A的化学方程式
③若有5.35 g氯化铵参加反应,则产生的A气体在标准状况下的体积为
④试写出C与水反应的化学方程式

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价——物质类别关系如图。回答下列问题:
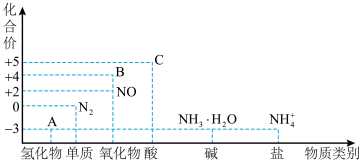
(1)在氮的单质和常见的含氮化合物中,常用作保护气的物质是___________ (填化学式),常用作制冷剂的物质是___________ (填名称)
(2)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是___________ 。
(3)A极易溶于水,水溶液显___________ 性,实验室以NH4Cl固体为主要原料制备A气体,其化学方程式为___________ ;
(4)欲吸收尾气中的A,下列装置中不可选用___________ (填字母)。(已知A难溶于CCl4)
a.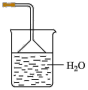 b.
b. c.
c. d.
d.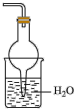
(5)氨气极易溶于水,可以利用如图装置进行喷泉实验。下列组合中也能产生“喷泉”现象的为___________ (填字母)。

a.NO和水 b.CO2和饱和NaHCO3溶液
c.Cl2和浓NaOH溶液 d.HCl和水
(6)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究的成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程___________ 。

(1)在氮的单质和常见的含氮化合物中,常用作保护气的物质是
(2)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是
(3)A极易溶于水,水溶液显
(4)欲吸收尾气中的A,下列装置中不可选用
a.
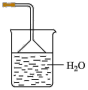 b.
b. c.
c. d.
d.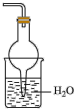
(5)氨气极易溶于水,可以利用如图装置进行喷泉实验。下列组合中也能产生“喷泉”现象的为

a.NO和水 b.CO2和饱和NaHCO3溶液
c.Cl2和浓NaOH溶液 d.HCl和水
(6)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究的成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A—H等8种物质存在如下转化关系下列A~H八种物质存在如下图所示的转化关系(反应条件、部分产物未标出)。已知A是正盐,B能使品红溶液褪色,G是红棕色气体。试回答下列问题:

(1)按要求写出下列反应的有关方程式:
①E→F反应的化学方程式_______ ;
②G→H反应的离子方程式_______ 。
(2)写出H的浓溶液与木炭反应的化学方程式_______ 。
(3)检验D中阴离子的方法是_______ 。
(4)将1.92 g铜粉投入含有0.11molH的溶液中,当铜粉和H恰好完全反应后,产生的气体在标准状况下的体积为_______ mL。

(1)按要求写出下列反应的有关方程式:
①E→F反应的化学方程式
②G→H反应的离子方程式
(2)写出H的浓溶液与木炭反应的化学方程式
(3)检验D中阴离子的方法是
(4)将1.92 g铜粉投入含有0.11molH的溶液中,当铜粉和H恰好完全反应后,产生的气体在标准状况下的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氨气能与金属氧化物(MxOy)反应生成M、N2和H2O,根据测定出H2O的量可推出金属M的相对原子质量,某研究小组同学用下列装置进行相关实验探究。请回答下列问题:
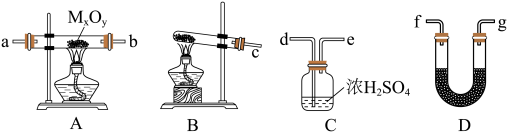
(1)按气流方向,正确的装置接口顺序为c→_________ (填序号,装置可重复使用)。
(2)装置D中盛放的药品名称为______ ,装置C的作用是_______ 。
(3)若实验中准确称取金属氧化物的质量为zg,完全反应后,测得D中生成水的质量为wg。则M的相对原子质量为_____ (用含x、y、z、w的式子表示)。
(4)某同学仔细分析上述装置后认为仍存在缺陷。你认为该如何改进:_________ .
(5)某同学用装置A、B、D以及装置E进行NH3的催化氧化实验研究,其中装置D盛放的药品为Na2O2。
①装置B中盛放的药品为________ .
②装置A中发生反应的化学方程式为_____________
③验证有NO生成的反应现象为_________ ,E中发生反应的化学方程式为____________


(1)按气流方向,正确的装置接口顺序为c→
(2)装置D中盛放的药品名称为
(3)若实验中准确称取金属氧化物的质量为zg,完全反应后,测得D中生成水的质量为wg。则M的相对原子质量为
(4)某同学仔细分析上述装置后认为仍存在缺陷。你认为该如何改进:
(5)某同学用装置A、B、D以及装置E进行NH3的催化氧化实验研究,其中装置D盛放的药品为Na2O2。
①装置B中盛放的药品为
②装置A中发生反应的化学方程式为
③验证有NO生成的反应现象为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】、下图中A~J分别代表相关反应中的一种物质,已知A分解得到等物质的量的B、C、D,已知B、D为常温下气态化合物,C为常温下液态化合物,图中有部分生成物未标出。
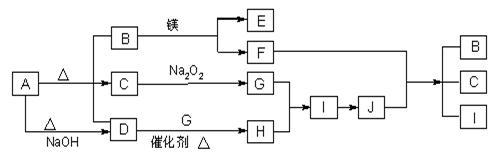
请填写以下空白:
(1)A的化学式_____________ B的电子式_______________ 。
(2)写出下列反应的化学方程式:
D+G→ H_____________________________ 。
F+J → B + C + I______________________________ 。
(3)写出A+NaOH→D的离子方程式______________________________ 。

请填写以下空白:
(1)A的化学式
(2)写出下列反应的化学方程式:
D+G→ H
F+J → B + C + I
(3)写出A+NaOH→D的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】宏观辨识与微观探析是化学学科重要的学科素养。回答下列问题:
Ⅰ.已知某无色水样中只含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种。某化学研究性学习小组对该水样的成分进行检验:
中的若干种。某化学研究性学习小组对该水样的成分进行检验:
①取部分水样;
②向水样中滴加足量硝酸钡溶液,产生白色沉淀;
③向步骤②所得沉淀中滴加足量稀盐酸,沉淀部分溶解;
④向步骤③所得溶液中滴加硝酸银溶液,又产生白色沉淀。
(1)该水样中一定存在的离子是__________ (填离子符号,下同),可能存在的离子是__________ ,一定不存在的离子是__________ 。
(2)若要确定可能存在的离子是否存在,还需进行的实验操作是__________ 。
Ⅱ.现有 、
、 、
、 、
、 四种溶液,该小组同学设计如下实验步骤进行鉴别:
四种溶液,该小组同学设计如下实验步骤进行鉴别:
①取等体积的上述四种溶液A、B、C、D分别置于四支试管中,对四支试管均进行下列操作:加入过量的 溶液、加热,将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。
溶液、加热,将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。
②向①中反应后的四支试管中,分别依次加入足量 溶液,观察到盛装B、C溶液的试管内产生白色沉淀。
溶液,观察到盛装B、C溶液的试管内产生白色沉淀。
(3)溶液A、B、C、D中的溶质依次为__________ 、__________ 、__________ 、__________ (填化学式)。
(4)有同学提出用一种试剂即可将四种溶液鉴别出来,该试剂为__________ (填化学式)。
Ⅰ.已知某无色水样中只含有
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种。某化学研究性学习小组对该水样的成分进行检验:
中的若干种。某化学研究性学习小组对该水样的成分进行检验:①取部分水样;
②向水样中滴加足量硝酸钡溶液,产生白色沉淀;
③向步骤②所得沉淀中滴加足量稀盐酸,沉淀部分溶解;
④向步骤③所得溶液中滴加硝酸银溶液,又产生白色沉淀。
(1)该水样中一定存在的离子是
(2)若要确定可能存在的离子是否存在,还需进行的实验操作是
Ⅱ.现有
 、
、 、
、 、
、 四种溶液,该小组同学设计如下实验步骤进行鉴别:
四种溶液,该小组同学设计如下实验步骤进行鉴别:①取等体积的上述四种溶液A、B、C、D分别置于四支试管中,对四支试管均进行下列操作:加入过量的
 溶液、加热,将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。
溶液、加热,将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。②向①中反应后的四支试管中,分别依次加入足量
 溶液,观察到盛装B、C溶液的试管内产生白色沉淀。
溶液,观察到盛装B、C溶液的试管内产生白色沉淀。(3)溶液A、B、C、D中的溶质依次为
(4)有同学提出用一种试剂即可将四种溶液鉴别出来,该试剂为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】氨氮废水中的氮元素多以 和
和 的形式存在。某工厂处理氨氮废水的流程如下:
的形式存在。某工厂处理氨氮废水的流程如下:

(1)过程①的目的是将 转化为
转化为 ,并通过鼓入大量空气将氨气吹出,写出
,并通过鼓入大量空气将氨气吹出,写出 转化为
转化为 的离子方程式:
的离子方程式:_______ 。
(2)过程②加入NaClO溶液可将氨氮物质转化为无毒物质,反应后含氮元素、氯元素的物质化学式分别为_______ 。
(3)过程③中含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到去除余氯的目的_______ (填字母)。
a.KOH b. c.
c. d.NaCl
d.NaCl
(4)过程②中向氨氮废水中加入NaClO溶液后生成HClO、HClO能够与水中的 反应达到去除氨氮的效果。测得不同pH的NaClO溶液对氨氮去除效果的影响如图所示。
反应达到去除氨氮的效果。测得不同pH的NaClO溶液对氨氮去除效果的影响如图所示。

① 时氨氮去除率随pH增大的而增大的原因是
时氨氮去除率随pH增大的而增大的原因是_______ ,
② 时氨氮去除率随pH增大的而减小的原因是
时氨氮去除率随pH增大的而减小的原因是_______ 。
 和
和 的形式存在。某工厂处理氨氮废水的流程如下:
的形式存在。某工厂处理氨氮废水的流程如下:
(1)过程①的目的是将
 转化为
转化为 ,并通过鼓入大量空气将氨气吹出,写出
,并通过鼓入大量空气将氨气吹出,写出 转化为
转化为 的离子方程式:
的离子方程式:(2)过程②加入NaClO溶液可将氨氮物质转化为无毒物质,反应后含氮元素、氯元素的物质化学式分别为
(3)过程③中含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到去除余氯的目的
a.KOH b.
 c.
c. d.NaCl
d.NaCl(4)过程②中向氨氮废水中加入NaClO溶液后生成HClO、HClO能够与水中的
 反应达到去除氨氮的效果。测得不同pH的NaClO溶液对氨氮去除效果的影响如图所示。
反应达到去除氨氮的效果。测得不同pH的NaClO溶液对氨氮去除效果的影响如图所示。
①
 时氨氮去除率随pH增大的而增大的原因是
时氨氮去除率随pH增大的而增大的原因是②
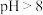 时氨氮去除率随pH增大的而减小的原因是
时氨氮去除率随pH增大的而减小的原因是
您最近一年使用:0次