一水草酸钙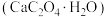 可用作分离稀有金属的载体。回答下列问题:
可用作分离稀有金属的载体。回答下列问题:
(1)制备一水草酸钙的方法如下:
先用精制氯化钙稀溶液与草酸钠溶液共热反应,过滤,将固体溶于热盐酸中;再加氨水反应得一水草酸钙沉淀,过滤,热水洗涤,在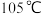 干燥得产品。
干燥得产品。
①已知 溶液的
溶液的 质量浓度为
质量浓度为 ,则该溶液中
,则该溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
②写出上述再加入氨水反应生成一水草酸钙沉淀的化学方程式:___________ 。
(2)为研究一水草酸钙的热分解性质,进行如下实验:准确称取 样品加热,样品的固体残留率
样品加热,样品的固体残留率
 )随温度的变化如下图所示。
)随温度的变化如下图所示。

① 时残留固体的成分为
时残留固体的成分为___________ , 时残留固体的成分为
时残留固体的成分为___________ 。
②已知 时固体的成分为
时固体的成分为 和
和 ,则
,则 的质量为
的质量为___________ g, 的质量为
的质量为___________ g。
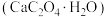 可用作分离稀有金属的载体。回答下列问题:
可用作分离稀有金属的载体。回答下列问题:(1)制备一水草酸钙的方法如下:
先用精制氯化钙稀溶液与草酸钠溶液共热反应,过滤,将固体溶于热盐酸中;再加氨水反应得一水草酸钙沉淀,过滤,热水洗涤,在
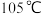 干燥得产品。
干燥得产品。①已知
 溶液的
溶液的 质量浓度为
质量浓度为 ,则该溶液中
,则该溶液中 的物质的量浓度为
的物质的量浓度为②写出上述再加入氨水反应生成一水草酸钙沉淀的化学方程式:
(2)为研究一水草酸钙的热分解性质,进行如下实验:准确称取
 样品加热,样品的固体残留率
样品加热,样品的固体残留率 )随温度的变化如下图所示。
)随温度的变化如下图所示。
①
 时残留固体的成分为
时残留固体的成分为 时残留固体的成分为
时残留固体的成分为②已知
 时固体的成分为
时固体的成分为 和
和 ,则
,则 的质量为
的质量为 的质量为
的质量为
更新时间:2022-12-07 20:55:09
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】聚合硫酸铁[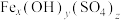 ]是高效水处理剂。以废铁屑(主要成分为铁,杂质为C、Si等)及硫酸为原料,制备聚合硫酸铁的工艺流程如下:
]是高效水处理剂。以废铁屑(主要成分为铁,杂质为C、Si等)及硫酸为原料,制备聚合硫酸铁的工艺流程如下:_______ (一种即可)。
(2)写出反应Ⅰ中生成 的离子方程式为
的离子方程式为_______ 。
(3)已知 溶液脱除空气中
溶液脱除空气中 并再生的原理如图所示。
并再生的原理如图所示。_______ 。
(4)聚合硫酸铁[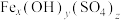 ]的组成可通过下列实验测定:
]的组成可通过下列实验测定:
①称取一定质量的聚合硫酸铁溶于稀盐酸中,往所得溶液中滴加 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;
②另称取与①等质量的聚合硫酸铁溶于稀硫酸中,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗涤液合并配成250.00mL溶液A;
③准确量取25.00mL溶液A,用 的
的 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液8.00mL。该步反应为:
溶液8.00mL。该步反应为: (未配平)。
(未配平)。
通过计算确定该聚合硫酸铁的化学式A_______ (写出计算过程)。
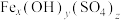 ]是高效水处理剂。以废铁屑(主要成分为铁,杂质为C、Si等)及硫酸为原料,制备聚合硫酸铁的工艺流程如下:
]是高效水处理剂。以废铁屑(主要成分为铁,杂质为C、Si等)及硫酸为原料,制备聚合硫酸铁的工艺流程如下:
(2)写出反应Ⅰ中生成
 的离子方程式为
的离子方程式为(3)已知
 溶液脱除空气中
溶液脱除空气中 并再生的原理如图所示。
并再生的原理如图所示。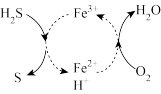
(4)聚合硫酸铁[
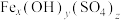 ]的组成可通过下列实验测定:
]的组成可通过下列实验测定:①称取一定质量的聚合硫酸铁溶于稀盐酸中,往所得溶液中滴加
 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;②另称取与①等质量的聚合硫酸铁溶于稀硫酸中,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗涤液合并配成250.00mL溶液A;
③准确量取25.00mL溶液A,用
 的
的 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液8.00mL。该步反应为:
溶液8.00mL。该步反应为: (未配平)。
(未配平)。通过计算确定该聚合硫酸铁的化学式A
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氧化锌为白色粉末,可用于湿疹、癖等皮肤病的治疗。纯化工业级氧化锌[含有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ)等杂质]的流程如下:

提示:在本实验条件下,Ni(II)不能被氧化;高锰酸钾的还原产物是MnO2。回答下列问题:
(1)反应②中除掉的杂质离子所发生的离子方程式为_______ 、_______ ;在加高锰酸钾溶液前,若pH较低,对除杂的影响是_______ 。
(2)反应③的反应类型为_______ ,过滤得到的滤渣中,除了过量的锌外还有_______ 。
(3)反应④中产物的成分是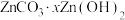 ,取干燥后的滤饼11.2g,煅烧后可得到产品8.1g,则x=
,取干燥后的滤饼11.2g,煅烧后可得到产品8.1g,则x=_______ 。

提示:在本实验条件下,Ni(II)不能被氧化;高锰酸钾的还原产物是MnO2。回答下列问题:
(1)反应②中除掉的杂质离子所发生的离子方程式为
(2)反应③的反应类型为
(3)反应④中产物的成分是
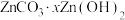 ,取干燥后的滤饼11.2g,煅烧后可得到产品8.1g,则x=
,取干燥后的滤饼11.2g,煅烧后可得到产品8.1g,则x=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制氧气( ),实验装置如下:
),实验装置如下:

实验步骤:
①连接好实验装置。
②___________。
③把适量的氯酸钾粉末和少量的二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为 。
。
④加热,开始反应,直到不再有气体产生为止。
⑤读取量气管读数,测得氧气的体积为 。
。
⑥准确称量试管和残留物的质量为 。
。
回答下列问题:
(1)实验步骤的第②步是___________ 。
(2)实验过程中产生氧气的物质的量是___________  (保留小数点后四位);实验测得氧气的气体摩尔体积是
(保留小数点后四位);实验测得氧气的气体摩尔体积是___________ (保留小数点后两位)。
(3)根据以上实验得出如下结论,其中不正确的是___________ (填字母)
A.气体摩尔体积与气体的温度相关
B.在该实验条件下,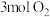 的气体摩尔体积为
的气体摩尔体积为
C.常温常压下,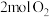 与
与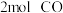 和
和 的混合气体的体积相同
的混合气体的体积相同
(4)为准确读出氧气的体积需进行以下操作,正确的顺序为___________ (填序号)
①调整量气管高度,使其液面高度与水准管液面高度相平;
②气体应恢复到室温下;
③视线与凹液面最低处相平
(5)实验结束读取氧气体积时,若量气管中液面高于水准管中液面,会使测得的氧气的体积___________ (填“偏大”“偏小”或“无影响”)。若有影响,应向___________ (填“上”或“下”)移动乙玻璃管,使甲、乙玻璃管中液面相平(若无影响,则第二空不用填写)。
 ),实验装置如下:
),实验装置如下:
实验步骤:
①连接好实验装置。
②___________。
③把适量的氯酸钾粉末和少量的二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为
 。
。④加热,开始反应,直到不再有气体产生为止。
⑤读取量气管读数,测得氧气的体积为
 。
。⑥准确称量试管和残留物的质量为
 。
。回答下列问题:
(1)实验步骤的第②步是
(2)实验过程中产生氧气的物质的量是
 (保留小数点后四位);实验测得氧气的气体摩尔体积是
(保留小数点后四位);实验测得氧气的气体摩尔体积是(3)根据以上实验得出如下结论,其中不正确的是
A.气体摩尔体积与气体的温度相关
B.在该实验条件下,
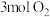 的气体摩尔体积为
的气体摩尔体积为
C.常温常压下,
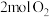 与
与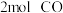 和
和 的混合气体的体积相同
的混合气体的体积相同(4)为准确读出氧气的体积需进行以下操作,正确的顺序为
①调整量气管高度,使其液面高度与水准管液面高度相平;
②气体应恢复到室温下;
③视线与凹液面最低处相平
(5)实验结束读取氧气体积时,若量气管中液面高于水准管中液面,会使测得的氧气的体积
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有8种物质:① ②
② ③CH3CH2OH④HOCH2CH2OH⑤
③CH3CH2OH④HOCH2CH2OH⑤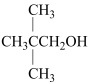 ⑥
⑥ ⑦
⑦ ⑧
⑧
根据要求,回答下列问题:
(1)①分子中含有的官能团的名称为____ ,②分子中最多可能有____ 个原子共平面,⑦分子中碳环上的一溴代物有____ 种。
(2)上述8种物质中,互为同分异构体的是____ (填序号,下同),互为同系物的是____ 。
(3)设NA为阿伏加德罗常数的值。下列关于上述8种物质的说法正确的是____ (填标号)。
(4)⑧的同分异构体中属于芳香族化合物的有____ 种,其中一种同分异构体满足以下条件:核磁共振氢谱图有4组峰,且峰面积之比为3:3:2:2,其结构简式为____ 。
 ②
② ③CH3CH2OH④HOCH2CH2OH⑤
③CH3CH2OH④HOCH2CH2OH⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
根据要求,回答下列问题:
(1)①分子中含有的官能团的名称为
(2)上述8种物质中,互为同分异构体的是
(3)设NA为阿伏加德罗常数的值。下列关于上述8种物质的说法正确的是
| A.②能发生取代反应和加成反应 |
| B.相同条件下,在水中的溶解度:⑤>④ |
| C.常温常压下,23g③中含有的碳氢键的数目为2.5NA |
| D.标准状况下,22.4L⑥与Na反应生成的H2的数目为0.5NA |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】 、金刚石、石墨、
、金刚石、石墨、 和硼化镁的结构模型如图所示。
和硼化镁的结构模型如图所示。

(1)固态 属于
属于___________ (填“原子”、“分子”或“离子”)晶体。
(2) 金刚石中含有
金刚石中含有 单键的数目约是
单键的数目约是___________  。
。
(3)石墨是层状结构,图中仅表示出其中的一层结构,石墨层之间容易发生滑动,请说明原因:___________ 。
(4) 晶体中,每个
晶体中,每个 分子周围有
分子周围有___________ 个与之紧邻且等距的 分子。
分子。
(5)在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体一层的微观结构图,则硼化镁的化学式为___________ 。
 、金刚石、石墨、
、金刚石、石墨、 和硼化镁的结构模型如图所示。
和硼化镁的结构模型如图所示。
(1)固态
 属于
属于(2)
 金刚石中含有
金刚石中含有 单键的数目约是
单键的数目约是 。
。(3)石墨是层状结构,图中仅表示出其中的一层结构,石墨层之间容易发生滑动,请说明原因:
(4)
 晶体中,每个
晶体中,每个 分子周围有
分子周围有 分子。
分子。(5)在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体一层的微观结构图,则硼化镁的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】镓是制作高性能半导体的重要原料,其化合物的性质与铝相似。工业上常从锌矿渣(主要含Zn、Si、Pb、Fe、Ga的氧化物,其中Pb、Fe均以+2价形式存在,Ga以+3价形式存在)中回收镓。工艺流程如图:

回答下面问题:
(1)锌矿渣首先要进行粉碎再浸出,粉碎的目的是_____ 。写出浸出渣I的化学式______ 。
(2)写出浸出液与H2O2反应的离子方程式_____ 。该反应中H2O2的用量比理论值大很多,同时有气泡冒出,原因是_____ 。用离子方程式表示调pH的目的:______ 。
(3)操作①用到的玻璃仪器为______ 。
(4)写出滤渣2与过量NaOH反应的离子方程式______ 。
(5)含[Ga(OH)4]-的溶液中通入过量CO2的离子方程式_____ 。
(6)取28.7 g ZnSO4•7H2O加热至不同温度,剩余固体的质量随温度的变化如图所示。分析数据,推断100℃、930℃时所得固体的化学式分别为______ 、_____ 。


回答下面问题:
(1)锌矿渣首先要进行粉碎再浸出,粉碎的目的是
(2)写出浸出液与H2O2反应的离子方程式
(3)操作①用到的玻璃仪器为
(4)写出滤渣2与过量NaOH反应的离子方程式
(5)含[Ga(OH)4]-的溶液中通入过量CO2的离子方程式
(6)取28.7 g ZnSO4•7H2O加热至不同温度,剩余固体的质量随温度的变化如图所示。分析数据,推断100℃、930℃时所得固体的化学式分别为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】在1到20号元素中,已知五种元素的核电荷数的大小顺序为F>A>B>D>E;A、F具有相同的电子层B、F具有相同的最外层电子数;A与B形成离子化合物A2B,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子分子。
(1)写出D元素形成的单质的结构式______ ;E、F和B三种元素形成的化合物属于____ (填晶体类型);写出B和E形成的化合物的化学式__________ 。
(2)在标准状况下,1克E的单质在足量的B的单质中完全反应,放出142.9kJ的热量,写出该反应的热化学方程式_______________________ 。
(3)元素Y的原子质子数比A多9,假如Y形成的强碱式量为M,把质量为mg的该强碱,在一定条件下,完全溶解在水中得到VmL饱和溶液,若此溶液的密度为 ,则该溶液中OH-离子的物质的量浓度为
,则该溶液中OH-离子的物质的量浓度为_______ 。
(1)写出D元素形成的单质的结构式
(2)在标准状况下,1克E的单质在足量的B的单质中完全反应,放出142.9kJ的热量,写出该反应的热化学方程式
(3)元素Y的原子质子数比A多9,假如Y形成的强碱式量为M,把质量为mg的该强碱,在一定条件下,完全溶解在水中得到VmL饱和溶液,若此溶液的密度为
 ,则该溶液中OH-离子的物质的量浓度为
,则该溶液中OH-离子的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室有化学纯的浓硫酸,其试剂瓶标签上的部分内容如图:
(1)该浓硫酸的物质的量浓度为________________
(2)取用浓硫酸时,不随所取体积的多少而变化的 物理量是_______
(3)配制480mL0.50mol/L的稀硫酸,需用量筒量取该浓硫酸_______ mL。
(4)此实验用到的玻璃仪器除了量筒、烧杯、玻璃棒,还有___________
(5)若实验遇下列情况,对所配制的硫酸溶液的物质的量浓度有何影响?(答“偏高”、“偏低”、“不变”)
①定容时俯视刻度线_______
②定容时液面超出刻度线,取出一点,使液面恰好至刻度线_______
③没有冷却至室温就转移、定容完毕_________
④量取浓硫酸时仰视读数__________
| 硫酸 化学纯 (500mL) 化学式:H2SO4 质量分数:98% 密度:1.84g/cm3 |
(2)取用浓硫酸时,不随所取体积的多少而变化的 物理量是_______
| A.溶液中H2SO4的物质的量 | B.溶液的浓度 |
| C.溶液的质量 | D.溶液的密度 |
(4)此实验用到的玻璃仪器除了量筒、烧杯、玻璃棒,还有
(5)若实验遇下列情况,对所配制的硫酸溶液的物质的量浓度有何影响?(答“偏高”、“偏低”、“不变”)
①定容时俯视刻度线
②定容时液面超出刻度线,取出一点,使液面恰好至刻度线
③没有冷却至室温就转移、定容完毕
④量取浓硫酸时仰视读数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】“84消毒液”能有效杀灭甲型H1N1等病毒,某同学购买了一瓶“威露士”牌“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:“84消毒液”含25%NaClO、1000 mL、密度1.192 g/cm3,稀释100倍(体积比)后使用。

请根据以上信息和相关知识回答下列问题:
(1)该“84消毒液”的物质的量浓度为____ mol/L。
(2)该同学取100 mL稀释后的消毒液用于消毒,稀释后溶液中c(Na+)=____ mol/L。
(3)一瓶“威露士”牌“84消毒液”最多能吸收空气中CO2____ L(标准状况)而变质。
(4)该同学参阅“威露士”牌“84消毒液”的配方,欲用NaClO固体配制480 mL含25% NaClO的消毒液。下列说法正确的是_____ (填编号)。
(5)最近发生多起“84消毒液”和洁厕灵混合使用的安全事故,请解释发生事故的原因是
______________________________________________________

请根据以上信息和相关知识回答下列问题:
(1)该“84消毒液”的物质的量浓度为
(2)该同学取100 mL稀释后的消毒液用于消毒,稀释后溶液中c(Na+)=
(3)一瓶“威露士”牌“84消毒液”最多能吸收空气中CO2
(4)该同学参阅“威露士”牌“84消毒液”的配方,欲用NaClO固体配制480 mL含25% NaClO的消毒液。下列说法正确的是
| A.如图所示的仪器中,有四种是不需要的,还需一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干才能用于溶液配制 |
| C.利用购买的商品NaClO来配制可能导致结果偏低 |
| D.需要称量的NaClO固体质量为143 g |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】铵明矾晶体的化学式为 ,以铵明矾为原料可实现如图转化。
,以铵明矾为原料可实现如图转化。 与题中阳离子不形成配合物,固体A为纯净物。
与题中阳离子不形成配合物,固体A为纯净物。
(1)铵明矾晶体“隔绝空气加热”分解产物中含硫化合物有___________ 。
(2)步骤III中生成白色沉淀C反应的化学方程式为___________ 。
(3)合成铵明矾过程中常使用过量的硫酸铵,一个作用是抑制硫酸铝水解,另一个重要作用是___________ 。
(4)设计实验验证固体A含有的金属元素:___________ 。
(5)步骤I中,铵明矾晶体在各温度段内受热“失重计算值”如表所示。(失重计算值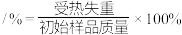 )
)
通过上述数据可判断,在温度区间___________ ℃,铵明矾基本上失去了结晶水。
 ,以铵明矾为原料可实现如图转化。
,以铵明矾为原料可实现如图转化。
 与题中阳离子不形成配合物,固体A为纯净物。
与题中阳离子不形成配合物,固体A为纯净物。(1)铵明矾晶体“隔绝空气加热”分解产物中含硫化合物有
(2)步骤III中生成白色沉淀C反应的化学方程式为
(3)合成铵明矾过程中常使用过量的硫酸铵,一个作用是抑制硫酸铝水解,另一个重要作用是
(4)设计实验验证固体A含有的金属元素:
(5)步骤I中,铵明矾晶体在各温度段内受热“失重计算值”如表所示。(失重计算值
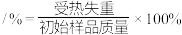 )
)| 温度区间/℃ | 18→190 | 190→430 | 430→505 | 505→900 |
| 失重计算值/% | 39.20 | 7.80 | 13.00 | 26.00 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】用氧化还原滴定法测定 的质量分数:一定条件下,将
的质量分数:一定条件下,将 溶解并还原为
溶解并还原为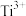 ,再以KSCN溶液作指示剂,用
,再以KSCN溶液作指示剂,用 标准液滴定至
标准液滴定至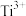 全部生成
全部生成 。
。
(1)配制 标准液的过程中,溶液转移时的操作如图所示。
标准液的过程中,溶液转移时的操作如图所示。
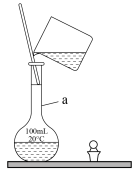
①仪器a的名称为___________ 。
②图中错误的地方有___________ 处,请指出其中一处:___________ 。
(2)滴定时:
① 标准液应盛装在
标准液应盛装在___________ (填“酸”或“碱”)式滴定管中,理由为___________ (用离子方程式表示,写一个即可)。
②滴定过程中,眼睛应注视___________ 。
③到达滴定终点时的现象为___________ 。
④若称取 试样
试样 ,消耗
,消耗 标准溶液VmL,则
标准溶液VmL,则 的质量分数为
的质量分数为___________ (用含m、c、V的代数式表示,不考虑操作过程中质量的损失)。
(3)下列实验误差分析错误的是___________(填标号)。
 的质量分数:一定条件下,将
的质量分数:一定条件下,将 溶解并还原为
溶解并还原为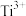 ,再以KSCN溶液作指示剂,用
,再以KSCN溶液作指示剂,用 标准液滴定至
标准液滴定至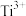 全部生成
全部生成 。
。(1)配制
 标准液的过程中,溶液转移时的操作如图所示。
标准液的过程中,溶液转移时的操作如图所示。
①仪器a的名称为
②图中错误的地方有
(2)滴定时:
①
 标准液应盛装在
标准液应盛装在②滴定过程中,眼睛应注视
③到达滴定终点时的现象为
④若称取
 试样
试样 ,消耗
,消耗 标准溶液VmL,则
标准溶液VmL,则 的质量分数为
的质量分数为(3)下列实验误差分析错误的是___________(填标号)。
| A.滴定前滴定管内无气泡,终点读数时有气泡,所测定的结果偏小 |
| B.刚看到指示剂局部的颜色有变化就停止滴定,所测定的结果偏大 |
| C.读数时,滴定前俯视,滴定后仰视,所测定的结果偏小 |
| D.未用标液溶液润洗滴定管,所测定的结果偏大 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有三种物质A、B、C,其中有一种是酸,一种是碱,一种是盐,溶于水后电离,可以产生下表中的离子:
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果,填空:
(1)物质C的化学式:_______________ 。
(2)鉴别某溶液中是否含有B中阴离子的实验操作方法是:______ 。
(3)完成以下水溶液中的反应的离子方程式:
A溶液与B溶液反应:_____________ ;
B溶液与沉淀E反应:__________ 。
(4)D与E的混合物αg,加入足量盐酸,反应完全生成标准状况时的气体bL,则D在混合物中的质量分数为_____________ 。
| 阳离子 | Na+ | H+ | Ba2+ |
| 阴离子 | OH- | CO | SO |
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果,填空:
(1)物质C的化学式:
(2)鉴别某溶液中是否含有B中阴离子的实验操作方法是:
(3)完成以下水溶液中的反应的离子方程式:
A溶液与B溶液反应:
B溶液与沉淀E反应:
(4)D与E的混合物αg,加入足量盐酸,反应完全生成标准状况时的气体bL,则D在混合物中的质量分数为
您最近一年使用:0次



