我国国标推荐的食品药品中Ca元素含量的测定方法之一为:利用Na2C2O4将处理后的样品中的Ca2+沉淀,过滤洗涤,然后将所得CaC2O4固体溶于过量的强酸,最后使用已知浓度的KMnO4溶液通过滴定来测定溶液中Ca2+的含量。针对该实验中的滴定过程,回答以下问题:
(1)KMnO4溶液应该用________ (填“酸式”或“碱式”)滴定管盛装,除滴定管外,还需要的玻璃仪器有________________________________________________________________
(2)试写出滴定过程中发生反应的离子方程式:__________________________________
(3)如何判断滴定终点________________________________________________________ 。
(4)以下操作会导致测定的结果偏高的是________ (填字母)。
a.装入KMnO4溶液前未润洗滴定管 b.滴定结束后俯视读数
c.滴定结束后,滴定管尖端悬有一滴溶液 d.滴定过程中,振荡时将待测液洒出
(1)KMnO4溶液应该用
(2)试写出滴定过程中发生反应的离子方程式:
(3)如何判断滴定终点
(4)以下操作会导致测定的结果偏高的是
a.装入KMnO4溶液前未润洗滴定管 b.滴定结束后俯视读数
c.滴定结束后,滴定管尖端悬有一滴溶液 d.滴定过程中,振荡时将待测液洒出
更新时间:2019-12-24 19:38:54
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】以废旧锂离子电池的正极材料[活性物质为 、附着物为炭黑、聚乙烯醇粘合剂、淀粉等]为原料,制备纳米钴粉和
、附着物为炭黑、聚乙烯醇粘合剂、淀粉等]为原料,制备纳米钴粉和 。
。

(1)预处理。将正极材料研磨成粉末后进行高温煅烧,高温煅烧的目的是___________ 。
(2)浸出,将煅烧后的粉末(含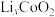 和少量难溶杂质)与硫酸混合,得到悬浊液,加入如图所示的烧瓶中。控制温度为75℃,边搅拌边通过分液漏斗滴加双氧水,充分反应后,滤去少量固体残渣。得到
和少量难溶杂质)与硫酸混合,得到悬浊液,加入如图所示的烧瓶中。控制温度为75℃,边搅拌边通过分液漏斗滴加双氧水,充分反应后,滤去少量固体残渣。得到 、
、 和硫酸的混合溶液。浸出实验中当观察到圆底烧瓶中不再产生气泡时,可以判断反应结束,不再滴加双氧水。则该实验中双氧水是:
和硫酸的混合溶液。浸出实验中当观察到圆底烧瓶中不再产生气泡时,可以判断反应结束,不再滴加双氧水。则该实验中双氧水是:___________ (填“氧化剂”或“还原剂”或“既是氧化剂又是还原剂”)。

(3)制钴粉。向浸出后的溶液中加入 调节pH,接着加入
调节pH,接着加入 可以制取单质钴粉,同时有
可以制取单质钴粉,同时有 生成。已知不同pH时Co(Ⅱ)的物种分布图如图所示。
生成。已知不同pH时Co(Ⅱ)的物种分布图如图所示。 可以和柠檬酸根离子(
可以和柠檬酸根离子( )生成配合物
)生成配合物 。
。

①写出 时制钴粉的离子方程式:
时制钴粉的离子方程式:___________ 。
② 后所制钴粉中由于含有
后所制钴粉中由于含有 而导致纯度降低。若向
而导致纯度降低。若向 的溶液中加入柠檬酸钠(
的溶液中加入柠檬酸钠(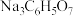 )可以提高钴粉的纯度,其离子方程式为:
)可以提高钴粉的纯度,其离子方程式为:___________ 。
(4)由浸取后滤液先制备 ,然后将
,然后将 加热至
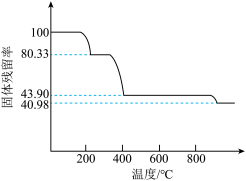
加热至___________ (填温度范围),当固体质量不再改变时制得 。已知:
。已知: 在空气中加热时的固体残留率(
在空气中加热时的固体残留率( ×100%)与随温度的变化如图所示。
×100%)与随温度的变化如图所示。
(5)用下列实验可以测定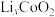 的组成:
的组成:
实验1:准确称取一定质量的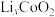 样品,加入盐酸,加热至固体完全溶解(溶液中的金属离子只存在
样品,加入盐酸,加热至固体完全溶解(溶液中的金属离子只存在 和
和 ),冷却后转移到容量瓶中并定容至
),冷却后转移到容量瓶中并定容至 。
。
实验2:移取 实验1容量瓶中溶液,加入指示剂,用
实验1容量瓶中溶液,加入指示剂,用 溶液滴定至终点(滴定反应为
溶液滴定至终点(滴定反应为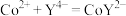 ),平行滴定3次,平均消耗EDTA溶液
),平行滴定3次,平均消耗EDTA溶液 。
。
实验3:移取 实验1容量瓶中溶液,通过火焰原子吸收光谱法测定其中
实验1容量瓶中溶液,通过火焰原子吸收光谱法测定其中 浓度为
浓度为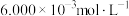 。
。
通过计算可得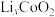 样品的化学式为
样品的化学式为___________ 。
 、附着物为炭黑、聚乙烯醇粘合剂、淀粉等]为原料,制备纳米钴粉和
、附着物为炭黑、聚乙烯醇粘合剂、淀粉等]为原料,制备纳米钴粉和 。
。
(1)预处理。将正极材料研磨成粉末后进行高温煅烧,高温煅烧的目的是
(2)浸出,将煅烧后的粉末(含
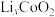 和少量难溶杂质)与硫酸混合,得到悬浊液,加入如图所示的烧瓶中。控制温度为75℃,边搅拌边通过分液漏斗滴加双氧水,充分反应后,滤去少量固体残渣。得到
和少量难溶杂质)与硫酸混合,得到悬浊液,加入如图所示的烧瓶中。控制温度为75℃,边搅拌边通过分液漏斗滴加双氧水,充分反应后,滤去少量固体残渣。得到 、
、 和硫酸的混合溶液。浸出实验中当观察到圆底烧瓶中不再产生气泡时,可以判断反应结束,不再滴加双氧水。则该实验中双氧水是:
和硫酸的混合溶液。浸出实验中当观察到圆底烧瓶中不再产生气泡时,可以判断反应结束,不再滴加双氧水。则该实验中双氧水是:
(3)制钴粉。向浸出后的溶液中加入
 调节pH,接着加入
调节pH,接着加入 可以制取单质钴粉,同时有
可以制取单质钴粉,同时有 生成。已知不同pH时Co(Ⅱ)的物种分布图如图所示。
生成。已知不同pH时Co(Ⅱ)的物种分布图如图所示。 可以和柠檬酸根离子(
可以和柠檬酸根离子( )生成配合物
)生成配合物 。
。
①写出
 时制钴粉的离子方程式:
时制钴粉的离子方程式:②
 后所制钴粉中由于含有
后所制钴粉中由于含有 而导致纯度降低。若向
而导致纯度降低。若向 的溶液中加入柠檬酸钠(
的溶液中加入柠檬酸钠(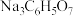 )可以提高钴粉的纯度,其离子方程式为:
)可以提高钴粉的纯度,其离子方程式为:(4)由浸取后滤液先制备
 ,然后将
,然后将 加热至
加热至 。已知:
。已知: 在空气中加热时的固体残留率(
在空气中加热时的固体残留率( ×100%)与随温度的变化如图所示。
×100%)与随温度的变化如图所示。
(5)用下列实验可以测定
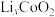 的组成:
的组成:实验1:准确称取一定质量的
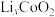 样品,加入盐酸,加热至固体完全溶解(溶液中的金属离子只存在
样品,加入盐酸,加热至固体完全溶解(溶液中的金属离子只存在 和
和 ),冷却后转移到容量瓶中并定容至
),冷却后转移到容量瓶中并定容至 。
。实验2:移取
 实验1容量瓶中溶液,加入指示剂,用
实验1容量瓶中溶液,加入指示剂,用 溶液滴定至终点(滴定反应为
溶液滴定至终点(滴定反应为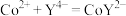 ),平行滴定3次,平均消耗EDTA溶液
),平行滴定3次,平均消耗EDTA溶液 。
。实验3:移取
 实验1容量瓶中溶液,通过火焰原子吸收光谱法测定其中
实验1容量瓶中溶液,通过火焰原子吸收光谱法测定其中 浓度为
浓度为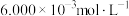 。
。通过计算可得
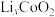 样品的化学式为
样品的化学式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】叠氨化钠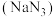 是制备医药、炸药的一种重要原料,
是制备医药、炸药的一种重要原料, 不溶于乙醚,微溶于乙醇,溶于水并能水解。工业上采用“亚硝酸甲酯
不溶于乙醚,微溶于乙醇,溶于水并能水解。工业上采用“亚硝酸甲酯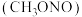 ——水合肼
——水合肼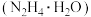 法”制备叠氮化钠的生产流程如下:
法”制备叠氮化钠的生产流程如下:
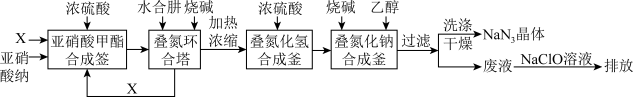
回答下列问题:
(1)叠氮环合塔中生成叠氮化钠的化学方程式为_______ 。
(2)叠氮环合塔中加入的烧碱溶液要适当过量,目的是_______ 。
(3)向“叠氮化钠合成釜”中加入乙醇的目的是_______ ,洗涤操作时选用的洗涤试剂最好的是_______ 。
(4)该生产过程中可循环使用的物质X的结构简式为_______ 。
(5)调节废液的 约为5,加入适量
约为5,加入适量 溶液。
溶液。
① 将废液中的叠氮化钠转化为
将废液中的叠氮化钠转化为 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
②研究发现,废液中叠氮化钠去除率随温度升高呈先升后降趋势。当温度大于 时,废水中叠氮化钠去除率随着温度升高而降低,其原因是
时,废水中叠氮化钠去除率随着温度升高而降低,其原因是_______ 。
(6)测定产品 晶体纯度的实验操作如下:取
晶体纯度的实验操作如下:取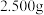 晶体配成
晶体配成 溶液,取
溶液,取 溶液置于锥形瓶中,加入
溶液置于锥形瓶中,加入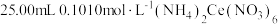 溶液,充分反应后,将溶液稀释,向溶液中加入4mL浓硫酸,滴入3滴指示剂,用
溶液,充分反应后,将溶液稀释,向溶液中加入4mL浓硫酸,滴入3滴指示剂,用 标准溶液滴定过量的
标准溶液滴定过量的 ,消耗溶液体积为
,消耗溶液体积为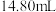 。有关反应为:
。有关反应为: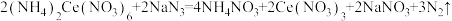 ;
;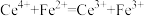 。试样中
。试样中 的质量分数为
的质量分数为_______ (计算结果保留1位小数)。
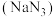 是制备医药、炸药的一种重要原料,
是制备医药、炸药的一种重要原料, 不溶于乙醚,微溶于乙醇,溶于水并能水解。工业上采用“亚硝酸甲酯
不溶于乙醚,微溶于乙醇,溶于水并能水解。工业上采用“亚硝酸甲酯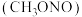 ——水合肼
——水合肼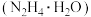 法”制备叠氮化钠的生产流程如下:
法”制备叠氮化钠的生产流程如下:
回答下列问题:
(1)叠氮环合塔中生成叠氮化钠的化学方程式为
(2)叠氮环合塔中加入的烧碱溶液要适当过量,目的是
(3)向“叠氮化钠合成釜”中加入乙醇的目的是
(4)该生产过程中可循环使用的物质X的结构简式为
(5)调节废液的
 约为5,加入适量
约为5,加入适量 溶液。
溶液。①
 将废液中的叠氮化钠转化为
将废液中的叠氮化钠转化为 ,该反应的离子方程式为
,该反应的离子方程式为②研究发现,废液中叠氮化钠去除率随温度升高呈先升后降趋势。当温度大于
 时,废水中叠氮化钠去除率随着温度升高而降低,其原因是
时,废水中叠氮化钠去除率随着温度升高而降低,其原因是(6)测定产品
 晶体纯度的实验操作如下:取
晶体纯度的实验操作如下:取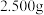 晶体配成
晶体配成 溶液,取
溶液,取 溶液置于锥形瓶中,加入
溶液置于锥形瓶中,加入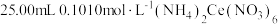 溶液,充分反应后,将溶液稀释,向溶液中加入4mL浓硫酸,滴入3滴指示剂,用
溶液,充分反应后,将溶液稀释,向溶液中加入4mL浓硫酸,滴入3滴指示剂,用 标准溶液滴定过量的
标准溶液滴定过量的 ,消耗溶液体积为
,消耗溶液体积为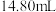 。有关反应为:
。有关反应为: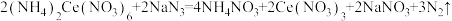 ;
;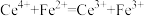 。试样中
。试样中 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】氧钒(IV)碱式碳酸铵晶体化学式为:(NH4)5[(VO)6(CO3)4(OH)9]·10H2O,实验室以V2O5为原料制备该晶体的流程如图:

(1)N2H4的电子式是_______ 。若“还原”后其它产物均绿色环保,写出该反应的化学方程式_______ 。
(2)“转化”可在如图装置中进行。(已知VO2+能被O2氧化)
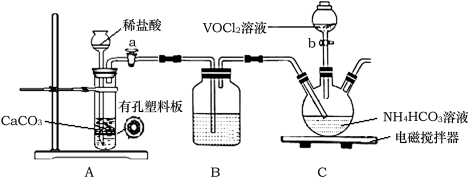
①B中的试剂_______ ;
②装置C中将VOCl2转化并得到产品,实验操作顺序为:先打开活塞_______ ,再打开活塞_______ (填序号),加入VOCl2溶液,持续搅拌一段时间,使反应完全。取出反应液于锥形瓶中,并迅速塞上橡胶塞。静置后过滤,得到紫红色晶体,抽滤,并用饱和NH4HCO3溶液洗涤3次,用无水乙醇(沸点78.5)洗涤2次,再用乙醚(沸点34.5)洗涤2次,抽干称重。用饱和NH4HCO3溶液洗涤除去的阴离子主要是_______ (填离子符号),用乙醚洗涤的目的是_______ 。
(3)称量m g产品于锥形瓶中,先将产品中钒元素转化为VO 。消除其它干扰,再用c mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为V mL(已知滴定反应为VO
。消除其它干扰,再用c mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为V mL(已知滴定反应为VO +Fe2++2H+= VO2++Fe3++H2O)。则产品中钒的质量分数为
+Fe2++2H+= VO2++Fe3++H2O)。则产品中钒的质量分数为_______ (以VO2+的量进行计算,列出计算式)。

(1)N2H4的电子式是
(2)“转化”可在如图装置中进行。(已知VO2+能被O2氧化)

①B中的试剂
②装置C中将VOCl2转化并得到产品,实验操作顺序为:先打开活塞
(3)称量m g产品于锥形瓶中,先将产品中钒元素转化为VO
 。消除其它干扰,再用c mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为V mL(已知滴定反应为VO
。消除其它干扰,再用c mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为V mL(已知滴定反应为VO +Fe2++2H+= VO2++Fe3++H2O)。则产品中钒的质量分数为
+Fe2++2H+= VO2++Fe3++H2O)。则产品中钒的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】红矶钠 是重要的化工原料,工业上以铬铁矿(
是重要的化工原料,工业上以铬铁矿( ,含少量
,含少量 、
、 )为主要原料制备红矾钠的工艺流程如下:
)为主要原料制备红矾钠的工艺流程如下:

已知:i. ii.
ii.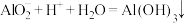
回答下列问题:
(1)焙烧铬铁矿生成 ,并将
,并将 和
和 转化为可溶性钠盐。
转化为可溶性钠盐。
①焙烧时为加快反应速率,可采取的措施是_______ 。
②生成 的化学方程式如下,将其补充完整:
的化学方程式如下,将其补充完整:_______ 。
□ +□
+□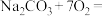 □______+□
□______+□ +□
+□
(2)滤液2中含有的溶质有: 、
、_______ 。
(3)中和时 的理论范围为4.5~9.3,调控
的理论范围为4.5~9.3,调控 不过高也不能过低的理由
不过高也不能过低的理由_______ 。
(4)酸化后所得溶液中主要含有 和
和 。
。

①结晶时,将混合溶液加热浓缩、_______ (填操作)、冷却结晶、过滤得到红矾钠晶体。
②滤液5最适宜返回上述流程_______ 中,参与循环再利用。
(5)工业上还可用膜电解技术(装置如图所示),以 为主要原料制备
为主要原料制备 ,结合化学用语简述制备
,结合化学用语简述制备 的原理:
的原理:_______ 。

(6) 可用于测定水体的COD(COD是指每升水样中还原性物质被氧化所需要
可用于测定水体的COD(COD是指每升水样中还原性物质被氧化所需要 的质量)。现有某水样
的质量)。现有某水样 ,酸化后加入
,酸化后加入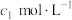 的
的 溶液
溶液 ,使水样中的还原性物质完全被氧化;再用
,使水样中的还原性物质完全被氧化;再用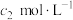 的
的 溶液滴定剩余的
溶液滴定剩余的 ,消耗
,消耗 溶液
溶液 ,则该水样的
,则该水样的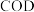 为
为_______  。【
。【 被还原为
被还原为 ;换算关系:
;换算关系: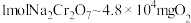 】
】
 是重要的化工原料,工业上以铬铁矿(
是重要的化工原料,工业上以铬铁矿( ,含少量
,含少量 、
、 )为主要原料制备红矾钠的工艺流程如下:
)为主要原料制备红矾钠的工艺流程如下:
已知:i.
 ii.
ii.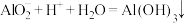
回答下列问题:
(1)焙烧铬铁矿生成
 ,并将
,并将 和
和 转化为可溶性钠盐。
转化为可溶性钠盐。①焙烧时为加快反应速率,可采取的措施是
②生成
 的化学方程式如下,将其补充完整:
的化学方程式如下,将其补充完整:□
 +□
+□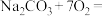 □______+□
□______+□ +□
+□
(2)滤液2中含有的溶质有:
 、
、(3)中和时
 的理论范围为4.5~9.3,调控
的理论范围为4.5~9.3,调控 不过高也不能过低的理由
不过高也不能过低的理由(4)酸化后所得溶液中主要含有
 和
和 。
。
①结晶时,将混合溶液加热浓缩、
②滤液5最适宜返回上述流程
(5)工业上还可用膜电解技术(装置如图所示),以
 为主要原料制备
为主要原料制备 ,结合化学用语简述制备
,结合化学用语简述制备 的原理:
的原理:
(6)
 可用于测定水体的COD(COD是指每升水样中还原性物质被氧化所需要
可用于测定水体的COD(COD是指每升水样中还原性物质被氧化所需要 的质量)。现有某水样
的质量)。现有某水样 ,酸化后加入
,酸化后加入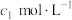 的
的 溶液
溶液 ,使水样中的还原性物质完全被氧化;再用
,使水样中的还原性物质完全被氧化;再用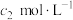 的
的 溶液滴定剩余的
溶液滴定剩余的 ,消耗
,消耗 溶液
溶液 ,则该水样的
,则该水样的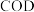 为
为 。【
。【 被还原为
被还原为 ;换算关系:
;换算关系: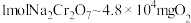 】
】
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】Ⅰ.制备水杨酸对正辛基苯基酯( )的过程如下:
)的过程如下:
步骤一:将水杨酸晶体投入到三颈烧瓶中,再加入适量的氯苯作溶剂并充分搅拌使晶体完全溶解,最后加入少量的无水三氯化铝。
步骤二:按下图所示装置装配好仪器,水浴加热控制温度在20~40℃之间,在搅拌下滴加SOCl2,反应制得水杨酰氯。
该反应方程式为:
 (水杨酸)+SOCl2→
(水杨酸)+SOCl2→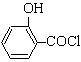 (水杨酰氯)+HCl↑+SO2↑
(水杨酰氯)+HCl↑+SO2↑
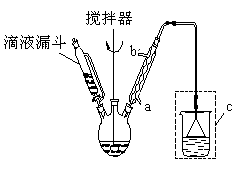
步骤三:将三颈烧瓶中混合液升温至80℃,再加入对正辛苯酚[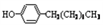 ],温度控制在100℃左右,不断搅拌。
],温度控制在100℃左右,不断搅拌。
步骤四:过滤、蒸馏、减压过滤;酒精洗涤、干燥即得产品。
(1)实验时,冷凝管中的冷却水进口为_______ (选填“a”或“b”);
(2)步骤一中加入无水三氯化铝的作用是___________________________ 。
(3)步骤三中发生反应的化学方程式为_____________________________ 。
Ⅱ.PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
已知下图是实验室制备PCl3的装置(部分仪器已省略),则:
(1)实验室制备Cl2的离子反应方程式为:________________ 。
(2)碱石灰的作用除了防止空气中的O2和水蒸气进入并与产品发生反应外还有:_________ 。
(3)向仪器甲中通入干燥Cl2之前,应先通入一段时间的干燥CO2,其目的是_____________ 。
(4)测定产品中PCl3纯度的方法如下:迅速称取m g产品,水解完全后配成500mL溶液,取出25.00mL加入过量的c1 mol/L V1 mL 碘溶液,充分反应后再用c2 mol/L Na2S2O3溶液滴定过量的碘,终点时消耗V2 mL Na2S2O3溶液。已知:H3PO3+H2O+I2==H3PO4+2HI;I2+2Na2S2O3==2NaI+Na2S4O6;假设测定过程中没有其他反应,则根据上述数据,求出该产品中PCl3的质量分数为___________________ (用含字母的代数式表示、可不化简)。
 )的过程如下:
)的过程如下:步骤一:将水杨酸晶体投入到三颈烧瓶中,再加入适量的氯苯作溶剂并充分搅拌使晶体完全溶解,最后加入少量的无水三氯化铝。
步骤二:按下图所示装置装配好仪器,水浴加热控制温度在20~40℃之间,在搅拌下滴加SOCl2,反应制得水杨酰氯。
该反应方程式为:
 (水杨酸)+SOCl2→
(水杨酸)+SOCl2→ (水杨酰氯)+HCl↑+SO2↑
(水杨酰氯)+HCl↑+SO2↑ 
步骤三:将三颈烧瓶中混合液升温至80℃,再加入对正辛苯酚[
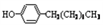 ],温度控制在100℃左右,不断搅拌。
],温度控制在100℃左右,不断搅拌。步骤四:过滤、蒸馏、减压过滤;酒精洗涤、干燥即得产品。
(1)实验时,冷凝管中的冷却水进口为
(2)步骤一中加入无水三氯化铝的作用是
(3)步骤三中发生反应的化学方程式为
Ⅱ.PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
| 熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其他 | |
| 白磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2 2PCl3;2P+5Cl2(过量) 2PCl3;2P+5Cl2(过量)  2PCl5 2PCl5 |
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |
已知下图是实验室制备PCl3的装置(部分仪器已省略),则:
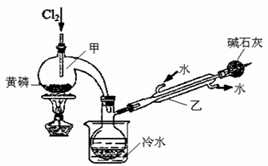
(1)实验室制备Cl2的离子反应方程式为:
(2)碱石灰的作用除了防止空气中的O2和水蒸气进入并与产品发生反应外还有:
(3)向仪器甲中通入干燥Cl2之前,应先通入一段时间的干燥CO2,其目的是
(4)测定产品中PCl3纯度的方法如下:迅速称取m g产品,水解完全后配成500mL溶液,取出25.00mL加入过量的c1 mol/L V1 mL 碘溶液,充分反应后再用c2 mol/L Na2S2O3溶液滴定过量的碘,终点时消耗V2 mL Na2S2O3溶液。已知:H3PO3+H2O+I2==H3PO4+2HI;I2+2Na2S2O3==2NaI+Na2S4O6;假设测定过程中没有其他反应,则根据上述数据,求出该产品中PCl3的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】某兴趣小组在相同条件下,将10.00g下列物质分别置于相同规格的烧杯,并敞口存放于空气中,烧杯中物质质量随时间变化如下表,回答下列问题。

(1)下列图示能反映水在空气中放置时发生变化的微观示意图是_________ (填字母序号)。

图中 表示氧原子,
表示氧原子, 表示氢原子)
表示氢原子)
(2)石灰水在空气中久置后有浑浊现象,写出该反应的化学方程式___________________ 。
(3)为研制一种安全、环保的除湿剂,可选择上表中的__________________ (填溶质的化学式)。
(4)将10.00g氯化钠浓溶液敞口久置后,最终得到2.26g晶体(已知该温度下氯化钠溶解度为36.1g),则该溶液是________ (填“饱和”或“不饱和”)溶液。
(5)为进一步研究稀盐酸敞口久置后浓度变化,该小组开展如下探究。
①甲同学猜想浓度可能会变大,理由是_______________________ 。
②为验证甲同学的猜想是否正确,设计实验方案:_________________________ 。
(6)乙同学取20%的氢氧化钠溶液20.00g,敞口放置一段时间后部分变质,得到18.80g溶液,_________ (填“能”或“不能”)计算所得溶液中溶质组成。

(1)下列图示能反映水在空气中放置时发生变化的微观示意图是

图中
 表示氧原子,
表示氧原子, 表示氢原子)
表示氢原子)(2)石灰水在空气中久置后有浑浊现象,写出该反应的化学方程式
(3)为研制一种安全、环保的除湿剂,可选择上表中的
(4)将10.00g氯化钠浓溶液敞口久置后,最终得到2.26g晶体(已知该温度下氯化钠溶解度为36.1g),则该溶液是
(5)为进一步研究稀盐酸敞口久置后浓度变化,该小组开展如下探究。
①甲同学猜想浓度可能会变大,理由是
②为验证甲同学的猜想是否正确,设计实验方案:
(6)乙同学取20%的氢氧化钠溶液20.00g,敞口放置一段时间后部分变质,得到18.80g溶液,
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】碘被称为“智力元素”,科学合理地补充碘可防治碘缺乏病,KI、KIO3曾先后用于加碘盐中。KI还可用于分析试剂、感光材料、制药等,其制备原理如图:
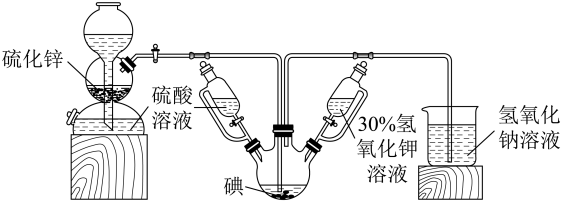
反应I:3I2+6KOH=KIO3+5KI+3H2O
反应II:3H2S+KIO3=3S↓+KI+3H2O
请回答有关问题。
(1)启普发生器中发生反应的离子方程式为____ 。
(2)关闭启普发生器活塞,先滴入30%的KOH溶液,待观察到三颈烧瓶中____ (填现象),停止滴入KOH溶液,然后____ (填操作),待三颈烧瓶和烧杯中的导管口产生气泡的速率接近相等时停止通气。
(3)滴入硫酸溶液,并对三颈烧瓶中的溶液进行水浴加热,其目的____ 。
(4)实验室模拟工业制备KIO3流程如图:
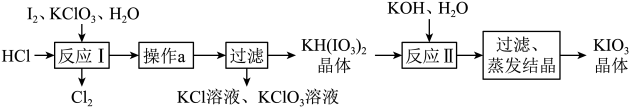
几种物质的溶解度见表:
①由表中数据分析可知,“操作a”为____ 。
②用惰性电极电解KI的碱性溶液也能制备KIO3,阳极反应式为____ ;与电解法相比,上述流程制备KIO3的缺点是____ 。
(5)已知反应:I2+2Na2S2O3=2NaI+Na2S4O6,某同学测定上述流程生产的KIO3样品的纯度。取3.00g样品,加蒸馏水配制成250mL溶液,从中取出20mL溶液于锥形瓶中,用硫酸酸化,再加入过量的KI和少量的淀粉溶液,逐滴滴加0.5mol/LNa2S2O3溶液,恰好完全反应时共消耗12.00mLNa2S2O3溶液。该样品中KIO3的质量分数为____ (结果保留到小数点后一位)。

反应I:3I2+6KOH=KIO3+5KI+3H2O
反应II:3H2S+KIO3=3S↓+KI+3H2O
请回答有关问题。
(1)启普发生器中发生反应的离子方程式为
(2)关闭启普发生器活塞,先滴入30%的KOH溶液,待观察到三颈烧瓶中
(3)滴入硫酸溶液,并对三颈烧瓶中的溶液进行水浴加热,其目的
(4)实验室模拟工业制备KIO3流程如图:

几种物质的溶解度见表:
| KCl | KH(IO3)2 | KClO3 | |
| 25℃时的溶解度(g) | 20.8 | 0.8 | 7.5 |
| 80℃时的溶解度(g) | 37.1 | 12.4 | 16.2 |
②用惰性电极电解KI的碱性溶液也能制备KIO3,阳极反应式为
(5)已知反应:I2+2Na2S2O3=2NaI+Na2S4O6,某同学测定上述流程生产的KIO3样品的纯度。取3.00g样品,加蒸馏水配制成250mL溶液,从中取出20mL溶液于锥形瓶中,用硫酸酸化,再加入过量的KI和少量的淀粉溶液,逐滴滴加0.5mol/LNa2S2O3溶液,恰好完全反应时共消耗12.00mLNa2S2O3溶液。该样品中KIO3的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献,某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备NaHCO3,进一步处理得到产品Na2CO3和NH4Cl,实验流程如图:

回答下列问题:
(1)从A~E中选择合适的仪器制备NaHCO3,正确的连接顺序是_____ (按气流方向,用小写字母表示)。为使A中分液漏斗内的稀盐酸顺利滴下,可将分液漏斗上部的玻璃塞打开或_____ 。
A.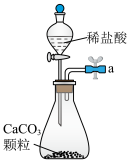 B.
B.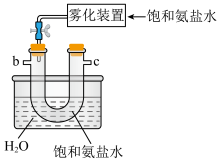 C.
C.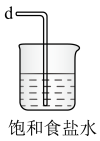 D.
D.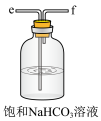 E.
E.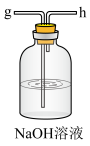
(2)B中使用雾化装置的优点是_____ 。
(3)生成NaHCO3的总反应的化学方程式为_____ 。
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO3和滤液:
①对固体NaHCO3充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.14g,则固体NaHCO3的质量为_____ g。
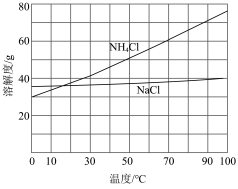
②向滤液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)→NaCl(aq)+NH4Cl(s)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为_____ 、过滤、洗涤、干燥。
(5)无水NaHCO3可作为基准物质标定盐酸浓度。称量前,若无水NaHCO3保存不当,吸收了一定量水分,用其标定盐酸浓度时,会使结果_____ (填标号)。
A.偏高 B.偏低 C.不变

回答下列问题:
(1)从A~E中选择合适的仪器制备NaHCO3,正确的连接顺序是
A.
 B.
B. C.
C. D.
D. E.
E.
(2)B中使用雾化装置的优点是
(3)生成NaHCO3的总反应的化学方程式为
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO3和滤液:
①对固体NaHCO3充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.14g,则固体NaHCO3的质量为
②向滤液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)→NaCl(aq)+NH4Cl(s)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为

(5)无水NaHCO3可作为基准物质标定盐酸浓度。称量前,若无水NaHCO3保存不当,吸收了一定量水分,用其标定盐酸浓度时,会使结果
A.偏高 B.偏低 C.不变
您最近一年使用:0次




