中国青铜文化历史悠久、内容丰富,是世界文化宝库中的精华。古代青铜中含有铜、锡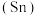 和铅
和铅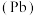 。回答下列问题:
。回答下列问题:
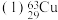 和
和 互称为
互称为________ ,其中 中的中子数与质子数之差为
中的中子数与质子数之差为________ 。
 锡与碳同主族,比碳多三个电子层,锡的原子结构示意图为
锡与碳同主族,比碳多三个电子层,锡的原子结构示意图为________ 。
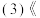 吕氏春秋
吕氏春秋 中的“金柔锡柔,合两柔则为刚”,说明合金的一种性能是
中的“金柔锡柔,合两柔则为刚”,说明合金的一种性能是________ 。
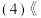 天工开物
天工开物 中关于锡的冶炼及提纯有如下叙述“凡炼煎亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞲熔化
中关于锡的冶炼及提纯有如下叙述“凡炼煎亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞲熔化 ”
” 砂的主要成分为
砂的主要成分为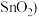 ,“售者杂铅太多,欲取净则熔化,入醋淬八九度,铅尽化灰而去”。生成Sn的化学方程式为
,“售者杂铅太多,欲取净则熔化,入醋淬八九度,铅尽化灰而去”。生成Sn的化学方程式为________ ,除去Sn中Pb的化学方程式为________ ,提纯除铅是利用了铅、锡的________ 的化学性质差异。
 现代工业中可用黄铜矿火法冶炼铜,反应之一为
现代工业中可用黄铜矿火法冶炼铜,反应之一为

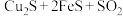 ,该反应每生成
,该反应每生成 转移电子的物质的量为
转移电子的物质的量为________ 。
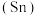 和铅
和铅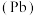 。回答下列问题:
。回答下列问题: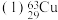 和
和 互称为
互称为 中的中子数与质子数之差为
中的中子数与质子数之差为 锡与碳同主族,比碳多三个电子层,锡的原子结构示意图为
锡与碳同主族,比碳多三个电子层,锡的原子结构示意图为 吕氏春秋
吕氏春秋 中的“金柔锡柔,合两柔则为刚”,说明合金的一种性能是
中的“金柔锡柔,合两柔则为刚”,说明合金的一种性能是 天工开物
天工开物 中关于锡的冶炼及提纯有如下叙述“凡炼煎亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞲熔化
中关于锡的冶炼及提纯有如下叙述“凡炼煎亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞲熔化 ”
” 砂的主要成分为
砂的主要成分为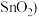 ,“售者杂铅太多,欲取净则熔化,入醋淬八九度,铅尽化灰而去”。生成Sn的化学方程式为
,“售者杂铅太多,欲取净则熔化,入醋淬八九度,铅尽化灰而去”。生成Sn的化学方程式为 现代工业中可用黄铜矿火法冶炼铜,反应之一为
现代工业中可用黄铜矿火法冶炼铜,反应之一为

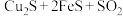 ,该反应每生成
,该反应每生成 转移电子的物质的量为
转移电子的物质的量为
更新时间:2019-12-26 16:33:35
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】有A、B、C、D四种元素,A元素的原子得2个电子,B元素的原子失去1个电子后所形成的微粒为氩原子有相同的电子层结构。C元素的原子只有1个电子,D元素原子的M电子层电子数比N层电子数多6个。试写出:
(1)A、B、C、D的元素名称:A____ 、B____ 、C____ 、D____ 。
(2)画出A元素的原子结构示意图_______ ,D元素的离子结构示意图_______ 。
(3)画出A离子的电子式_______ ,B原子的电子式_______ 。
(1)A、B、C、D的元素名称:A
(2)画出A元素的原子结构示意图
(3)画出A离子的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】应用有关原子或元素的知识解决下列问题:
(1)画出S2-的离子结构示意图___________ 。
(2)核内中子数为N的R+,质量数为A,则该离子的核外电子数为___________ 。
(3)许多元素有多种核素,现有10.0g由1H和18O组成的水分子,其中含中子数为___________ NA。
(4)氯碱工业用电解饱和食盐水制取氯气,该反应的化学方程式是:___________ ;化学需要具备现象分析推理能力,电解硫酸铜溶液的实验现象是:负极上有红色固体生成;正极上收集的气体能使带火星木条复燃;正极附近的溶液能使紫色石蕊溶液变红。据此推断,该反应的化学方程式是:___________ 。(不需要配平)
(1)画出S2-的离子结构示意图
(2)核内中子数为N的R+,质量数为A,则该离子的核外电子数为
(3)许多元素有多种核素,现有10.0g由1H和18O组成的水分子,其中含中子数为
(4)氯碱工业用电解饱和食盐水制取氯气,该反应的化学方程式是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】含氯消毒剂在生产生活中有着广泛的用途。完成下列填空:
(1)工业上将氯气溶于一定浓度的氢氧化钠溶于可制得“84消毒液”,反应的离子方程式为_________ 。
(2)“84消毒液”(主要成分是NaClO)不能和洁厕剂(主要成分是浓盐酸)混用。混用时反应的化学方程式是_______________________________ ;“84消毒液”不能对钢铁制品进行消毒,原因是____________ 。
(3)工业常用石灰乳和氯气反应制取漂粉精,其主要设备是氯化塔,将含有3%-6%水分的石灰乳从塔顶部喷洒而入,氯气从塔的最底层通入。这样加料的目的是__________ ;处理从氯化塔中逸出气体的方法是_____ 。
(4)二氧化氯(ClO2)是一种黄绿色易溶于水的气体。工业上常用NaClO3和Na2SO3溶液混合并加入H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为_________ 。
(5)在用二氧化氯进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+生成ClO2-和MnO2的离子方程式为___________________________ 。
(1)工业上将氯气溶于一定浓度的氢氧化钠溶于可制得“84消毒液”,反应的离子方程式为
(2)“84消毒液”(主要成分是NaClO)不能和洁厕剂(主要成分是浓盐酸)混用。混用时反应的化学方程式是
(3)工业常用石灰乳和氯气反应制取漂粉精,其主要设备是氯化塔,将含有3%-6%水分的石灰乳从塔顶部喷洒而入,氯气从塔的最底层通入。这样加料的目的是
(4)二氧化氯(ClO2)是一种黄绿色易溶于水的气体。工业上常用NaClO3和Na2SO3溶液混合并加入H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为
(5)在用二氧化氯进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+生成ClO2-和MnO2的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有中学化学中常见的几种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生:H2O2→O2
(1)该反应中的还原剂的是________________ 。
(2)该反应中,发生还原反应的过程是__________________________ 。
(3)写出该反应的化学方程式(配平)__________________________________ 。
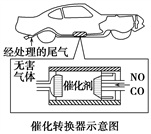
(4)随着人们环保意识的增强,许多汽车都已经装上了如图所示的尾气处理装置。在催化剂的作用下,尾气中两种主要的有毒气体反应生成两种无害气体,两种无害气体均为空气中的成分,写出该反应的化学方程式:___________________________ 。
(1)该反应中的还原剂的是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式(配平)
(4)随着人们环保意识的增强,许多汽车都已经装上了如图所示的尾气处理装置。在催化剂的作用下,尾气中两种主要的有毒气体反应生成两种无害气体,两种无害气体均为空气中的成分,写出该反应的化学方程式:

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求完成下列填空
(1)写出KOH电子式_______ ;写出CO2的结构式_______
(2)短周期主族元素中周期序数和族序数相等的元素有_______ (填元素符号)
(3)用电子式表示下列化合物的形成过程H2S:_______ ;MgF2:_______ 。
(4)A2-原子核内有x个中子,其质量数为m,则n g A2-所含电子的物质的量为_______ 。
(1)写出KOH电子式
(2)短周期主族元素中周期序数和族序数相等的元素有
(3)用电子式表示下列化合物的形成过程H2S:
(4)A2-原子核内有x个中子,其质量数为m,则n g A2-所含电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】填空
(1) 和
和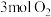 的分子数之比
的分子数之比_____ ,为原子数之比_____ 。
(2)某氯化物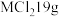 ,含有
,含有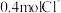 ,M的摩尔质量为
,M的摩尔质量为_____ 。
(3)同温同压下,同体积的 气体和
气体和 气体质量之比为
气体质量之比为_____ ,质子数之比为_____ 。
(4)已知阴离子 的原子核内有n个中子,R原子的质量数为m,则w克
的原子核内有n个中子,R原子的质量数为m,则w克 所含有电子的物质的量是
所含有电子的物质的量是_____  。
。
(1)
 和
和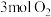 的分子数之比
的分子数之比(2)某氯化物
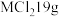 ,含有
,含有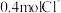 ,M的摩尔质量为
,M的摩尔质量为(3)同温同压下,同体积的
 气体和
气体和 气体质量之比为
气体质量之比为(4)已知阴离子
 的原子核内有n个中子,R原子的质量数为m,则w克
的原子核内有n个中子,R原子的质量数为m,则w克 所含有电子的物质的量是
所含有电子的物质的量是 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下列微粒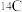 、
、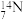 、
、 、
、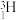 、
、 、
、
(1)共有___________ 种核素,属于___________ 种元素,___________ 和___________ 互为同位素,质量数相等的微粒为___________ 和___________ 。
(2) 的中子数是
的中子数是___________ , 的中子数与质子数之差
的中子数与质子数之差___________ 。
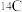 、
、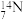 、
、 、
、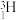 、
、 、
、
(1)共有
(2)
 的中子数是
的中子数是 的中子数与质子数之差
的中子数与质子数之差
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)26Al和27Al_______(选填编号)。
(2)碳元素的一种核素也可以考古断代,其原子符号为_______ ;
(3)10 g10Be所含的中子数与质子数之差为_______ 个。
(4)自然界一共存在三种硅的稳定同位素,分别是28Si、29Si和30Si。计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素的_______ 。硅原子的结构示意图为 _______ ,核外能量最高的电子位于_______ (填电子层符号)层。
(1)26Al和27Al_______(选填编号)。
| A.是同一种元素 | B.是同一种核素 | C.具有相同的中子数 | D.具有相同的化学性质 |
(3)10 g10Be所含的中子数与质子数之差为
(4)自然界一共存在三种硅的稳定同位素,分别是28Si、29Si和30Si。计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】填空:(填编号)A. B.
B.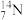 C.
C.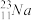 D.
D.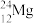 E.
E.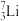 F.
F.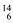 C G.C60 H .CH3CH2COOH I.HO-CH2CH2-CHO J.金刚石 K.P4 L.SiO2 M.NH4Cl
C G.C60 H .CH3CH2COOH I.HO-CH2CH2-CHO J.金刚石 K.P4 L.SiO2 M.NH4Cl
(1)_______ 和________ 互为同位素;
(2)中子数相等,但不是同一种元素的是_______ 和_____ ;
(3)_______ 和______ 互为同素异形体,_______ 和_______ 互为同分异构体。
(4)熔化时需要破坏共价键的是________ ;晶体中既有离子键又有共价键的是________ 。
 B.
B.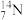 C.
C.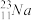 D.
D.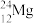 E.
E.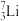 F.
F.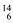 C G.C60 H .CH3CH2COOH I.HO-CH2CH2-CHO J.金刚石 K.P4 L.SiO2 M.NH4Cl
C G.C60 H .CH3CH2COOH I.HO-CH2CH2-CHO J.金刚石 K.P4 L.SiO2 M.NH4Cl(1)
(2)中子数相等,但不是同一种元素的是
(3)
(4)熔化时需要破坏共价键的是
您最近一年使用:0次



