已知:CO2(g)+2NaOH(aq)=Na2CO3(aq)+H2O(l) △H=Q1 kJ·mol-1;CO2(g)+NaOH(aq)=NaHCO3(aq) △H=Q2 kJ·mol-1。将15.68 L(标准状况)CO2气体通入1 L 1.0 mol·L-1氢氧化钠溶液中,反应完全时能量变化为Q3 kJ则Q1、Q2、Q3之间的关系正确的是
| A.Q3=0.3 Q1+0.4Q2 | B.Q3=0.7Q1 | C.Q3=0.7Q2 | D.Q3=0.4Q1+0.3Q2 |
更新时间:2019-12-25 10:01:39
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】2 mol金属钠和l mol氯气反应的能量关系如图所示,下列说法不正确 的是:
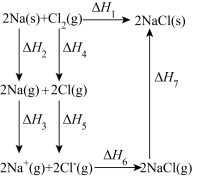

| A.原子失电子为吸热过程,相同条件下,K(s)的(△H2'+△H3')<Na(s)的(△H2+△H3) |
| B.△H4的值数值上和Cl-Cl共价键的键能相等 |
| C.△H2+△H3+△H4+△H5>-(△H6+△H7) |
| D.2Na(s)+Cl2(g)=2NaCl(s)在较低温度下自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.在稀溶液中,1molH2SO4(aq)与1molBa(OH)2(aq)完全反应所放出的热量为中和热 |
| B.等质量的硫粉和硫蒸气分别完全燃烧,后者放出的热量更多 |
| C.乙炔(C2H2)的燃烧热为1299.6kJ•mol-1,则2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g)的△H=-2599.2kJ•mol-1 |
| D.中和热测定实验中,可分多次把NaOH溶液倒入盛有稀盐酸的小烧杯中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示。下列说法正确的是


| A.加入催化剂,减小了反应的热效应 |
| B.加入催化剂,可提高H2O2的平衡转化率 |
C.H2O2分解的热化学方程式:H2O2= H2O+ O2,△H<0 O2,△H<0 |
| D.反应物的总能量高于生成物的总能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是( )
| A.书写热化学方程式时,只要在化学方程式的右端写上热量的符号和数值即可 |
| B.凡是在加热或点燃条件下进行的反应都是吸热反应 |
| C.表明反应所放出或吸收热量的化学方程式叫做热化学方程式 |
D.氢气在氧气中燃烧的热化学方程式是: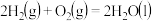 ; ;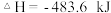 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知(1)H2O(g) = H2O(l) ΔH1=-Q1 kJ·mol-1
(2)CH3OH(g) = CH3OH(l) △H2=-Q2 kJ·mol-1
(3)2CH3OH(g) +3O2(g) = 2CO2(g)+4H2O(g) △H3=-Q3 kJ·mol-1(Q1、Q2、Q3均大于0)若要使1mol液态甲醇完全燃烧,最后恢复到室温,其△H为
(2)CH3OH(g) = CH3OH(l) △H2=-Q2 kJ·mol-1
(3)2CH3OH(g) +3O2(g) = 2CO2(g)+4H2O(g) △H3=-Q3 kJ·mol-1(Q1、Q2、Q3均大于0)若要使1mol液态甲醇完全燃烧,最后恢复到室温,其△H为
| A.Q2- 0.5Q3-2Q1 | B.0.5Q3-Q2+2Q1 | C.Q3-2Q2+4Q1 | D.0.5(Q1+Q2+Q3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol-1
已知:C(s)+O2(g)=CO2(g) ΔH1=a kJ·mol-1
S(s)+2K(s)=K2S(s) ΔH2=b kJ·mol-1
2K(s)+N2(g)+3O2(g)=2KNO3(s) ΔH3=c kJ·mol-1
则x为
S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol-1
已知:C(s)+O2(g)=CO2(g) ΔH1=a kJ·mol-1
S(s)+2K(s)=K2S(s) ΔH2=b kJ·mol-1
2K(s)+N2(g)+3O2(g)=2KNO3(s) ΔH3=c kJ·mol-1
则x为
| A.3a+b-c | B.c +3a-b | C.a+b-c | D.c-a-b |
您最近一年使用:0次






 )
)
 及25℃下,葡萄糖的燃烧热为
及25℃下,葡萄糖的燃烧热为 。图中能正确表示反应:
。图中能正确表示反应: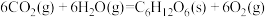 的能量变化曲线是
的能量变化曲线是
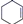 )、环己二烯(
)、环己二烯( )和苯的氢化热数据:
)和苯的氢化热数据: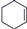 +H2
+H2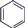 +3H2
+3H2

