(1)向含有Cr2O72-的酸性废水中滴加硫酸亚铁溶液生成Cr3+,反应的离子方程式为____
(2)FeO·Cr2O3+Na2CO3+NaNO3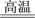 Na2CrO4+Fe2O3+CO2+NaNO2 该反应配平后FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+Fe2O3+CO2+NaNO2 该反应配平后FeO·Cr2O3与NaNO3的系数比为________________ 。
(3)FePO4、Li2CO3、H2C2O4混合后高温煅烧制LiFePO4的化学方程式为_____________
(4)用NaOH、H2O2的混合溶液吸收ClO2生产NaClO2,氧化剂与还原剂的物质的量之比为________ 。
(2)FeO·Cr2O3+Na2CO3+NaNO3
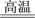 Na2CrO4+Fe2O3+CO2+NaNO2 该反应配平后FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+Fe2O3+CO2+NaNO2 该反应配平后FeO·Cr2O3与NaNO3的系数比为(3)FePO4、Li2CO3、H2C2O4混合后高温煅烧制LiFePO4的化学方程式为
(4)用NaOH、H2O2的混合溶液吸收ClO2生产NaClO2,氧化剂与还原剂的物质的量之比为
更新时间:2020-01-07 08:36:11
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】过碳酸钠( )和
)和 都是常见的消毒剂、漂白剂。其中过碳酸钠具有
都是常见的消毒剂、漂白剂。其中过碳酸钠具有 和
和 的性质;在碱性溶液中,
的性质;在碱性溶液中, 分解较快。请回答下列问题:
分解较快。请回答下列问题:
(1)过碳酸钠在水产品养殖业中可以快速提高水中溶解氧含量的原因是___________ 。
(2)下列物质与过碳酸钠混合,不会使过碳酸钠失效的是___________ 。
a. b.盐酸 c.NaCl
b.盐酸 c.NaCl
(3) 可用作自来水消毒剂的原因是
可用作自来水消毒剂的原因是___________ 。
(4)制备 可用以下方法:
可用以下方法: (未配平),X的化学式是
(未配平),X的化学式是___________ 。
 )和
)和 都是常见的消毒剂、漂白剂。其中过碳酸钠具有
都是常见的消毒剂、漂白剂。其中过碳酸钠具有 和
和 的性质;在碱性溶液中,
的性质;在碱性溶液中, 分解较快。请回答下列问题:
分解较快。请回答下列问题:(1)过碳酸钠在水产品养殖业中可以快速提高水中溶解氧含量的原因是
(2)下列物质与过碳酸钠混合,不会使过碳酸钠失效的是
a.
 b.盐酸 c.NaCl
b.盐酸 c.NaCl(3)
 可用作自来水消毒剂的原因是
可用作自来水消毒剂的原因是(4)制备
 可用以下方法:
可用以下方法: (未配平),X的化学式是
(未配平),X的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO和H2O。已知水是反应产物之一。
(1)该反应中的还原剂是___ 。
(2)该反应中的还原产物是___ 。
(3)写出该反应的化学方程式:___ 。
(4)若反应过程中转移了0.3mol电子,则生成水的质量是___ 。
(1)该反应中的还原剂是
(2)该反应中的还原产物是
(3)写出该反应的化学方程式:
(4)若反应过程中转移了0.3mol电子,则生成水的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题。
(1)火药是中国的四大发明之一,永远值得华夏儿女骄傲,黑火药在发生爆炸时,发生如下反应:S+2KNO3+ 3C= K2S +N2 ↑ + 3CO2↑,其中作氧化剂的是:_______ (填化学式) 。
(2)中国古代著作中有“银针验毒”的记录,其原理为:4Ag + 2H2S + O2=2X + 2H2O,则X的化学式是_______ ,其中H2S在该反应中_______ (填标号)
A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)“侯氏制碱法”的发明,开创了现代制碱技术的新纪元,同时解决了人们的温饱问题。其主要工艺流程如下图所示:

下列说法正确的是 _______ (填序号)
(4)对固体NaHCO3充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.28g,则固体 NaHCO3的质量为_______ g。
(1)火药是中国的四大发明之一,永远值得华夏儿女骄傲,黑火药在发生爆炸时,发生如下反应:S+2KNO3+ 3C= K2S +N2 ↑ + 3CO2↑,其中作氧化剂的是:
(2)中国古代著作中有“银针验毒”的记录,其原理为:4Ag + 2H2S + O2=2X + 2H2O,则X的化学式是
A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)“侯氏制碱法”的发明,开创了现代制碱技术的新纪元,同时解决了人们的温饱问题。其主要工艺流程如下图所示:

下列说法正确的是 _______ (填序号)
| A.用NaCl制取纯碱的过程中,利用了物质溶解度的差异 |
| B.沉淀池中NH3与CO2的通入顺序为先通入 CO2,再通入 NH3 |
| C.侯氏制碱法循环I利用的物质主要是CO2 |
| D.检验产品Na2CO3中是否含有NaCl的操作方法是取少量试样溶于水,加入过量的稀硝酸,再滴加硝酸银溶液,观察是否有白色沉淀生成 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】H2O2、O2、O3在水中可形成具有超强氧化能力的羟基自由基(HO•),可有效去除废水中的H2PO 、CN-、苯酚等物质。
、CN-、苯酚等物质。
(1)弱碱性条件下HO•将H2PO 氧化成PO
氧化成PO ,该反应的离子方程式为
,该反应的离子方程式为____ 。
(2)光催化氧化技术也可生成HO•降解有机污染物,其原理如图1,光照时,价带失去电子产生有强氧化性的空穴,价带上生成HO•的电极反应式为____ 。图中HO•还有另外的产生途径,描述其产生过程____ 。

(3)已知Cu2+可催化过氧化氢氧化废水中的CN-。在含氰废水总量、过氧化氢用量和溶液pH一定的情况下反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化如图2所示。c(Cu2+)超过90mg•L-1时,CN-的氧化去除率有所下降,原因是____ 。

图-2
(4)H2O2在Fe3O4催化剂表面产生HO•除去废水中的苯酚的原理如图3所示。在不同初始pH条件下,研究苯酚的去除率随时间的变化,结果表明:在反应开始时,初始pH=6的溶液中苯酚的去除率明显低于初始pH=3的溶液,但一段时间后两者接近,原因是____ 。

图-3
(5)BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,原理如图4所示。①和②中被降解的苯酚的物质的量之比为____ 。

 、CN-、苯酚等物质。
、CN-、苯酚等物质。(1)弱碱性条件下HO•将H2PO
 氧化成PO
氧化成PO ,该反应的离子方程式为
,该反应的离子方程式为(2)光催化氧化技术也可生成HO•降解有机污染物,其原理如图1,光照时,价带失去电子产生有强氧化性的空穴,价带上生成HO•的电极反应式为

(3)已知Cu2+可催化过氧化氢氧化废水中的CN-。在含氰废水总量、过氧化氢用量和溶液pH一定的情况下反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化如图2所示。c(Cu2+)超过90mg•L-1时,CN-的氧化去除率有所下降,原因是

图-2
(4)H2O2在Fe3O4催化剂表面产生HO•除去废水中的苯酚的原理如图3所示。在不同初始pH条件下,研究苯酚的去除率随时间的变化,结果表明:在反应开始时,初始pH=6的溶液中苯酚的去除率明显低于初始pH=3的溶液,但一段时间后两者接近,原因是

图-3
(5)BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,原理如图4所示。①和②中被降解的苯酚的物质的量之比为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氧化还原反应和复分解反应是高中重要学习的反应类型。
(1)在Fe(OH)3胶体中逐滴加入HI稀溶液,会出现一系列变化:
①先出现红褐色沉淀,原因是:_____ 。
②随后沉淀溶解,溶液呈黄色,写出此过程反应的离子方程式:_____ 。
③最后溶液颜色加深呈黄色,请推测其原因是_____ 。
(2)①若标准状况下,H2S和O2的混合气体120mL,经点燃后,反应至完全,所得气体经干燥后,恢复到原来状况,体积变为30mL,原气体中H2S的体积可能为_____ 。
②已知硫化氢气体在空气中的体积分数为4.3%~45.5%时点燃会发生爆炸,当硫化氢在空气中的体积分数为20%时,其爆炸产物是_____ 。
(3)在硫酸酸化的MnSO4溶液中加入NaBiO3(不溶于冷水),溶液变为紫红色,同时生成无色的Bi3+。写出该反应的离子反应方程式,并标出电子转移的方向和数目:_____ 。
(4)将氯气通入含1molNaOH的溶液中,形成NaClO、NaCl和NaOH的混合溶液。随后用此溶液吸收标准状况下5.6LSO2气体,恰好完全反应得到中性溶液。可知原溶液通入氯气_____ mol。
(5)①足量SO2气体通入Ba(NO3)2溶液中,能使所有NO 转化成NO放出,写出反应的化学方程式
转化成NO放出,写出反应的化学方程式_____ 。
②如果用含等物质的量溶质的下列各溶液分别来吸收SO2,则理论吸收量由多到少的顺序是(用编号排序)_____ 。
A.Na2SO3 B.Ba(NO3)2 C.Na2S D.酸性KMnO4
(1)在Fe(OH)3胶体中逐滴加入HI稀溶液,会出现一系列变化:
①先出现红褐色沉淀,原因是:
②随后沉淀溶解,溶液呈黄色,写出此过程反应的离子方程式:
③最后溶液颜色加深呈黄色,请推测其原因是
(2)①若标准状况下,H2S和O2的混合气体120mL,经点燃后,反应至完全,所得气体经干燥后,恢复到原来状况,体积变为30mL,原气体中H2S的体积可能为
②已知硫化氢气体在空气中的体积分数为4.3%~45.5%时点燃会发生爆炸,当硫化氢在空气中的体积分数为20%时,其爆炸产物是
(3)在硫酸酸化的MnSO4溶液中加入NaBiO3(不溶于冷水),溶液变为紫红色,同时生成无色的Bi3+。写出该反应的离子反应方程式,并标出电子转移的方向和数目:
(4)将氯气通入含1molNaOH的溶液中,形成NaClO、NaCl和NaOH的混合溶液。随后用此溶液吸收标准状况下5.6LSO2气体,恰好完全反应得到中性溶液。可知原溶液通入氯气
(5)①足量SO2气体通入Ba(NO3)2溶液中,能使所有NO
 转化成NO放出,写出反应的化学方程式
转化成NO放出,写出反应的化学方程式②如果用含等物质的量溶质的下列各溶液分别来吸收SO2,则理论吸收量由多到少的顺序是(用编号排序)
A.Na2SO3 B.Ba(NO3)2 C.Na2S D.酸性KMnO4
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】大多数金属硫化物难溶于水,可溶于硝酸。例如:
①FeS +HNO3(稀)→Fe(NO3)3 +NO↑+S↓+H2O(未配平)
②CuS +HNO3(浓)→CuSO4 +NO2↑+H2O(未配平)
(1)配平反应②的方程式:
__ CuS +__ HNO3(浓)→__ CuSO4 +__ NO2↑+__ H2O
(2)反应①中若生成3.2g硫,则电子转移___ 个。
(3)由反应①和②是否能够判断稀硝酸与浓硝酸的氧化性强弱?并说明判断依据。____ 。
(4)反应①和②所涉及的4种非金属元素中,原子半径由大到小的顺序是____ ;未成对电子最多的原子核外电子排布式为___ 。
下列描述,不能用来比较硫、氮两种元素的非金属性强弱的是___ 。
a.单质与氧气化合的难易程度 b.气态氢化物的稳定性
c.含氧酸的酸性强弱 d.S4N4中共用电子对的偏向
(5)写出①NO ②S ③H2O ④NO2四种物质的沸点由高到低的顺序(用编号回答)____ 。若要判断NO2分子的极性,你所需要的信息是___ 。
①FeS +HNO3(稀)→Fe(NO3)3 +NO↑+S↓+H2O(未配平)
②CuS +HNO3(浓)→CuSO4 +NO2↑+H2O(未配平)
(1)配平反应②的方程式:
(2)反应①中若生成3.2g硫,则电子转移
(3)由反应①和②是否能够判断稀硝酸与浓硝酸的氧化性强弱?并说明判断依据。
(4)反应①和②所涉及的4种非金属元素中,原子半径由大到小的顺序是
下列描述,不能用来比较硫、氮两种元素的非金属性强弱的是
a.单质与氧气化合的难易程度 b.气态氢化物的稳定性
c.含氧酸的酸性强弱 d.S4N4中共用电子对的偏向
(5)写出①NO ②S ③H2O ④NO2四种物质的沸点由高到低的顺序(用编号回答)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】劳动教育是学校教育的重要组成部分。阅读下面科普文章,回答相关问题。
科学施肥是农业生产中重要的环节。
I.稻田宜选用 效果较好,而不宜选用
效果较好,而不宜选用 及硝态氮肥。因为硫酸根在水田中易还原为
及硝态氮肥。因为硫酸根在水田中易还原为 ,使稻根发黑甚至腐烂,硝酸根在水田中易随水淋失或反硝化而损失。
,使稻根发黑甚至腐烂,硝酸根在水田中易随水淋失或反硝化而损失。
II.钾肥能提高蔬菜质量,使其色泽鲜亮,外形整齐,口感好,也能提高其糖酸比和维生素C的含量。 适用于各种作物,尤其是马铃薯等“忌氯”作物,效果比
适用于各种作物,尤其是马铃薯等“忌氯”作物,效果比 好。
好。
Ⅲ.尿素 是由碳、氮、氧、氢组成的有机化合物,是哺乳动物和某些鱼类体内
是由碳、氮、氧、氢组成的有机化合物,是哺乳动物和某些鱼类体内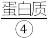 代谢分解的主要含氮终产物。工业上用
代谢分解的主要含氮终产物。工业上用 和
和 在一定条件下合成尿素。
在一定条件下合成尿素。
(1)在上述短文标有序号的物质中,属于电解质的是_______ (填序号,下同),属于有机物的是_______ ,属于酸性氧化物的是_______ 。
(2)某实践小组进行无土栽培丝瓜试验,需配制 溶液做的营养液。用托盘天平称量
溶液做的营养液。用托盘天平称量_______  固体,在小烧杯溶解后将溶液转移至
固体,在小烧杯溶解后将溶液转移至 的容量瓶﹔用蒸馏水洗涤烧杯2~3次;定容时,当液面离容量瓶颈刻度线下
的容量瓶﹔用蒸馏水洗涤烧杯2~3次;定容时,当液面离容量瓶颈刻度线下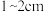 处,改用
处,改用_______ 滴加蒸馏水至液面与刻度线相切。该配制过程中两次用到玻璃棒,其作用分别是_______ 、_______ 。
(3)写出工业上合成尿素的的化学反应方程式_______ 。
科学施肥是农业生产中重要的环节。
I.稻田宜选用
 效果较好,而不宜选用
效果较好,而不宜选用 及硝态氮肥。因为硫酸根在水田中易还原为
及硝态氮肥。因为硫酸根在水田中易还原为 ,使稻根发黑甚至腐烂,硝酸根在水田中易随水淋失或反硝化而损失。
,使稻根发黑甚至腐烂,硝酸根在水田中易随水淋失或反硝化而损失。II.钾肥能提高蔬菜质量,使其色泽鲜亮,外形整齐,口感好,也能提高其糖酸比和维生素C的含量。
 适用于各种作物,尤其是马铃薯等“忌氯”作物,效果比
适用于各种作物,尤其是马铃薯等“忌氯”作物,效果比 好。
好。Ⅲ.尿素
 是由碳、氮、氧、氢组成的有机化合物,是哺乳动物和某些鱼类体内
是由碳、氮、氧、氢组成的有机化合物,是哺乳动物和某些鱼类体内 代谢分解的主要含氮终产物。工业上用
代谢分解的主要含氮终产物。工业上用 和
和 在一定条件下合成尿素。
在一定条件下合成尿素。(1)在上述短文标有序号的物质中,属于电解质的是
(2)某实践小组进行无土栽培丝瓜试验,需配制
 溶液做的营养液。用托盘天平称量
溶液做的营养液。用托盘天平称量 固体,在小烧杯溶解后将溶液转移至
固体,在小烧杯溶解后将溶液转移至 的容量瓶﹔用蒸馏水洗涤烧杯2~3次;定容时,当液面离容量瓶颈刻度线下
的容量瓶﹔用蒸馏水洗涤烧杯2~3次;定容时,当液面离容量瓶颈刻度线下 处,改用
处,改用(3)写出工业上合成尿素的的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】硫代硫酸钠( )俗称大苏打、海波,其中硫的价态为+2价,是一种重要的无机化工原料。
)俗称大苏打、海波,其中硫的价态为+2价,是一种重要的无机化工原料。
Ⅰ.大苏打溶液置于空气中容易发生下列反应而出现黄色浑浊
①
②
(1)从硫的价态的角度分析,硫代硫酸钠_______(填序号)
(2)反应①中的氧化剂是_______ ,还原剂是_______ 。
(3)配制好的大苏打溶液会加入少量 ,吸收
,吸收 生成
生成 来防止发生反应①,涉及的化学方程式为
来防止发生反应①,涉及的化学方程式为_______ 。
(4)为了避免发生反应②,往往还会向配制好的大苏打溶液中加入少量 ,请你猜测加入
,请你猜测加入 的作用是什么?
的作用是什么?_______ 。
Ⅱ.生活中,自来水厂常常利用氟气对水体进行消毒,因而自来水中常有氯气残余。
(5)氯气与水的反应方程式为_______ ,氯气溶于水后,能实际起到漂白杀菌效果的成分是_______ (填名称)。
(6)可以使用大苏打来处理水中残余的氯气。涉及的化学方程式为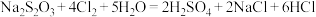
请在方程式中标出反应物电子转移的方向和数目_______ 。
(7)上述 和
和 的反应中,被还原的元素是
的反应中,被还原的元素是_______ ,氧化剂与还原剂的物质的量之比是_______ ,每转移10mol电子,可吸收标况下氯气_______ L。
(8)自来水中的残余的氯气也可以通过太阳暴晒一段时间来除去,请结合化学方程式解释其原理。_______ 。
(9)请分别对上述两种除去水中残余氯气的方法进行评价。_______ 。
Ⅲ.某实验探究小组需要用到0.1000mo/L的 溶液240mL,依据如下步骤配制溶液:
溶液240mL,依据如下步骤配制溶液:
(10)①在电子天平上准确称量_______ g 固体
固体
②将固体转移入_______ 中,加入新煮沸的蒸馏水进行溶解
③待溶液恢复至室温后,将溶液沿玻璃棒注入_______ 中
④加入新煮沸的蒸馏水至液面距离刻度线下1~2cm处,改用胶头滴管加水至凹液面底部与刻度线相切
⑤摇匀
(11)为什么在配制溶液的过程中要使用新煮沸的蒸馏水?_______ 。
(12)该探究小组严格按照上述实验步骤配制溶液,没有操作失误,却还是发现所配溶液浓度偏小,你认为是什么原因造成的?(该小组已排除了在配制的过程中 的变质对实验的影响)
的变质对实验的影响)_______ 。
 )俗称大苏打、海波,其中硫的价态为+2价,是一种重要的无机化工原料。
)俗称大苏打、海波,其中硫的价态为+2价,是一种重要的无机化工原料。Ⅰ.大苏打溶液置于空气中容易发生下列反应而出现黄色浑浊
①

②

(1)从硫的价态的角度分析,硫代硫酸钠_______(填序号)
| A.只有还原性 | B.只有氧化性 |
| C.既有氧化性也有还原性 | D.既没有氧化性也没有还原性 |
(3)配制好的大苏打溶液会加入少量
 ,吸收
,吸收 生成
生成 来防止发生反应①,涉及的化学方程式为
来防止发生反应①,涉及的化学方程式为(4)为了避免发生反应②,往往还会向配制好的大苏打溶液中加入少量
 ,请你猜测加入
,请你猜测加入 的作用是什么?
的作用是什么?Ⅱ.生活中,自来水厂常常利用氟气对水体进行消毒,因而自来水中常有氯气残余。
(5)氯气与水的反应方程式为
(6)可以使用大苏打来处理水中残余的氯气。涉及的化学方程式为
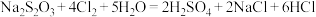
请在方程式中标出反应物电子转移的方向和数目
(7)上述
 和
和 的反应中,被还原的元素是
的反应中,被还原的元素是(8)自来水中的残余的氯气也可以通过太阳暴晒一段时间来除去,请结合化学方程式解释其原理。
(9)请分别对上述两种除去水中残余氯气的方法进行评价。
Ⅲ.某实验探究小组需要用到0.1000mo/L的
 溶液240mL,依据如下步骤配制溶液:
溶液240mL,依据如下步骤配制溶液:(10)①在电子天平上准确称量
 固体
固体②将固体转移入
③待溶液恢复至室温后,将溶液沿玻璃棒注入
④加入新煮沸的蒸馏水至液面距离刻度线下1~2cm处,改用胶头滴管加水至凹液面底部与刻度线相切
⑤摇匀
(11)为什么在配制溶液的过程中要使用新煮沸的蒸馏水?
(12)该探究小组严格按照上述实验步骤配制溶液,没有操作失误,却还是发现所配溶液浓度偏小,你认为是什么原因造成的?(该小组已排除了在配制的过程中
 的变质对实验的影响)
的变质对实验的影响)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】中国自古有“信口雌黄”、“雄黄入药”之说。雌黄As2S3和雄黄As4S4都是自然界中常见的难溶砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。
(1)砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示(雌黄和雄黄中S元素的价态相同)。

①反应Ⅰ、Ⅱ、Ⅲ、Ⅳ中属于氧化还原反应的是:___________ ;属于氧化还原的反应中氧化剂是___________ (填化学式)。
②反应Ⅰ中发生的离子方程式是___________ ,并用单线桥表明电子转移。
③反应Ⅱ中,雄黄在空气中加热会产生As2O3和物质a,若4.28gAs4O4反应转移0.28mole-,则a为___________ (填化学式)
(2)反应Ⅲ中产物亚砷酸H3AsO3可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液的pH关系如图所示。如H3AsO3的物质的量分数记作

①将KOH溶液滴入H3AsO3溶液,在溶液pH由8变至10的过程中,发生反应的离子方程式是___________ 。
②H3AsO3溶液与足量KOH溶液反应所得的正盐是___________ (填化学式)。
(1)砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示(雌黄和雄黄中S元素的价态相同)。

①反应Ⅰ、Ⅱ、Ⅲ、Ⅳ中属于氧化还原反应的是:
②反应Ⅰ中发生的离子方程式是
③反应Ⅱ中,雄黄在空气中加热会产生As2O3和物质a,若4.28gAs4O4反应转移0.28mole-,则a为
(2)反应Ⅲ中产物亚砷酸H3AsO3可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液的pH关系如图所示。如H3AsO3的物质的量分数记作


①将KOH溶液滴入H3AsO3溶液,在溶液pH由8变至10的过程中,发生反应的离子方程式是
②H3AsO3溶液与足量KOH溶液反应所得的正盐是
您最近一年使用:0次



