如图所示,常温下通电5 min后,发现铜电极的质量增加,试回答:
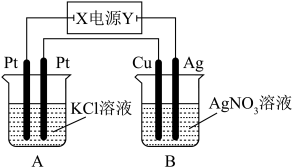
(1)电源电极X的名称为______ (填“正极”或“负极”)。
(2)电解池B中阳极的电极反应式是:__________________________________________ 。
(3)若KCl溶液的体积是200 mL,则当铜电极的质量增加2.16 g时A中溶液的pH=________ (忽略电解前后溶液体积的变化),若要使电解后的溶液恢复
到与电解前完全相同的状态,则应加入________ (填物质的种类及物质的量)。
(4)当铜、银两电极的质量差为2.16 g时,A中生成的气体最多为________ mol。

(1)电源电极X的名称为
(2)电解池B中阳极的电极反应式是:
(3)若KCl溶液的体积是200 mL,则当铜电极的质量增加2.16 g时A中溶液的pH=
到与电解前完全相同的状态,则应加入
(4)当铜、银两电极的质量差为2.16 g时,A中生成的气体最多为
19-20高二上·宁夏中卫·期末 查看更多[2]
更新时间:2020-01-11 12:44:17
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某课外兴趣小组用右图装置进行实验,试回答:
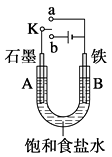
(1)若开始时开关K与a连接,则A电极反应式为________ 。
(2)若开始时开关K与b连接,这种方法经常用于金属的防护,这种防护措施叫做________ ,则A电极反应式为________ ;B电极反应式为________ 。
(3)开关K与b连接,将饱和食盐水换成CuSO4溶液,则A电极反应式为________ ,该反应的离子方程式为________ ,若将电解质溶液恢复至原状,应补充________ 。

(1)若开始时开关K与a连接,则A电极反应式为
(2)若开始时开关K与b连接,这种方法经常用于金属的防护,这种防护措施叫做
(3)开关K与b连接,将饱和食盐水换成CuSO4溶液,则A电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.用惰性电极电解200 mL一定浓度的硫酸铜溶液,实验装置如图①所示,电解过程中的实验数据如图②所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。
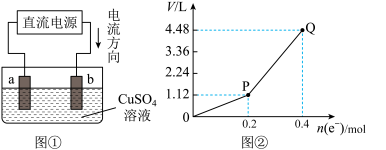
(1)下列说法正确的是______ (填序号)。
A.电解过程中,b电极表面先有红色物质析出,后有气泡产生
B.a电极上发生的反应为2H++2e-==H2↑和4OH--4e-==2H2O+O2↑
C.从P点到Q点时收集到的混合气体的平均摩尔质量为12 g·mol-1
D.OP段表示H2和O2混合气体的体积变化,PQ段表示O2的体积变化
(2)如果向所得的溶液中加入0.1 mol Cu(OH)2后,使溶液恰好恢复到电解前的浓度和pH,电解过程中转移的电子为________ mol。
(3)如果向所得的溶液中加入0.1 mol Cu2(OH)2CO3后,使溶液恰好恢复到电解前的浓度和pH(不考虑CO2的溶解),电解过程中转移的电子为________ mol。
Ⅱ. 金属腐蚀是我们日常生活的常见现象(如图所示)。

(1)如图铜板上铁铆钉处的腐蚀属于____ 腐蚀。
(2)分析此腐蚀过程,下列有关说法中,不正确的是____ 。
A.正极电极反应式为:2H++2e-=H2↑
B.此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3
C.此过程中铜并不被腐蚀
D.此过程中电子从Fe移向Cu

(1)下列说法正确的是
A.电解过程中,b电极表面先有红色物质析出,后有气泡产生
B.a电极上发生的反应为2H++2e-==H2↑和4OH--4e-==2H2O+O2↑
C.从P点到Q点时收集到的混合气体的平均摩尔质量为12 g·mol-1
D.OP段表示H2和O2混合气体的体积变化,PQ段表示O2的体积变化
(2)如果向所得的溶液中加入0.1 mol Cu(OH)2后,使溶液恰好恢复到电解前的浓度和pH,电解过程中转移的电子为
(3)如果向所得的溶液中加入0.1 mol Cu2(OH)2CO3后,使溶液恰好恢复到电解前的浓度和pH(不考虑CO2的溶解),电解过程中转移的电子为
Ⅱ. 金属腐蚀是我们日常生活的常见现象(如图所示)。

(1)如图铜板上铁铆钉处的腐蚀属于
(2)分析此腐蚀过程,下列有关说法中,不正确的是
A.正极电极反应式为:2H++2e-=H2↑
B.此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3
C.此过程中铜并不被腐蚀
D.此过程中电子从Fe移向Cu
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】如右图所示,常温,U形管内盛有100mL的某种溶液,请按要求回答下列问题。
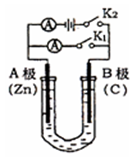
(1)若所盛溶液为CuSO4溶液,打开K2,合并K1,则:
① A为_____ 极,B极的电极反应式为________________ 。
②反应过程中,溶液中SO42-和OH-离子向_____ 极(A或B)移动。
(2)若所盛溶液为滴有酚酞的NaCl溶液,打开K1,合并K2,则:
①A电极可观察到的现象是__________________________ 。
②电解过程总反应的化学方程式是________________________ 。
③反应一段时间后打开K2,若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(折算成标准状况)为11.2mL,将溶液充分混合,溶液的pH为________ 。
④向电解后的电解质溶液中加入或通入_______ (填试剂名称),能使溶液复原。

(1)若所盛溶液为CuSO4溶液,打开K2,合并K1,则:
① A为
②反应过程中,溶液中SO42-和OH-离子向
(2)若所盛溶液为滴有酚酞的NaCl溶液,打开K1,合并K2,则:
①A电极可观察到的现象是
②电解过程总反应的化学方程式是
③反应一段时间后打开K2,若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(折算成标准状况)为11.2mL,将溶液充分混合,溶液的pH为
④向电解后的电解质溶液中加入或通入
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】硫元素及其化合物在工农业生产中有着重要的应用。
(1)在工业废水的处理过程中,常用FeS(s)、MnS(s)等难溶物作为沉淀剂除去废水中的Cu2+、Hg2+、Pb2+等重金属离子。写出FeS(s)作沉淀剂除去废水中Cu2+的离子反应方程式___________ 。
(2)威尔曼-洛德工艺,是采用亚硫酸钠水溶液吸收SO2的烟气脱硫工艺。具体操作如下:先用Na2SO3吸收SO2生成NaHSO3,再将吸收液进行加热得到增浓的SO2,回收的SO2可以生产液态SO2、液态SO3和硫酸。已知室温下H2SO3的电离平衡常数Ka1=1.54×10-2;Ka2=1.02×10-7。
①0.1mol·L-1NaHSO3溶液呈___________ (填“酸性”、“中性”或“碱性”);理由是___________ 。
②焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛,由NaHSO3过饱和溶液经结晶脱水可以制得焦亚硫酸钠(Na2S2O5)。写出该过程的化学方程式___________ 。
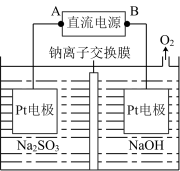
(3)连二亚硫酸钠(Na2S2O4)又称保险粉;工业上可用如图所示装置电解Na2SO3溶液制备Na2S2O4,其阴极的电极反应式为___________ ;标准状况下,当阳极产生224mL气体时,理论上左侧可制得Na2S2O4___________ g,右侧电解液质量变化了___________ g。
(1)在工业废水的处理过程中,常用FeS(s)、MnS(s)等难溶物作为沉淀剂除去废水中的Cu2+、Hg2+、Pb2+等重金属离子。写出FeS(s)作沉淀剂除去废水中Cu2+的离子反应方程式
(2)威尔曼-洛德工艺,是采用亚硫酸钠水溶液吸收SO2的烟气脱硫工艺。具体操作如下:先用Na2SO3吸收SO2生成NaHSO3,再将吸收液进行加热得到增浓的SO2,回收的SO2可以生产液态SO2、液态SO3和硫酸。已知室温下H2SO3的电离平衡常数Ka1=1.54×10-2;Ka2=1.02×10-7。
①0.1mol·L-1NaHSO3溶液呈
②焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛,由NaHSO3过饱和溶液经结晶脱水可以制得焦亚硫酸钠(Na2S2O5)。写出该过程的化学方程式
(3)连二亚硫酸钠(Na2S2O4)又称保险粉;工业上可用如图所示装置电解Na2SO3溶液制备Na2S2O4,其阴极的电极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列反应合成甲醇:CO(g)+2H2(g) CH3OH(g) ΔH
CH3OH(g) ΔH
①下列数据是在不同温度下的化学平衡常数(K)。
由表中数据判断ΔH____ 0(填“>”、“=”或“<”。)
②250℃,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得:CO剩余0.4mol,求K1__________ 。
(2)已知在常温常压下:①CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=-442.8KJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0kJ/mol
写出甲醇燃烧热的热化学方程式____________________________________________ ,
(3)某实验小组依据甲醇燃烧的反应原理,设计如图(A)所示的燃料电池装置。则:
①该燃料电池负极的电极反应为:___________________________ ,
②用该甲醇燃料电池对B池进行电解,已知c、d是质量相同的铜棒,电解2min后,取出c、d,洗净、烘干、称量,质量差为0.64g,在通电过程中,电路中通过的电子为_________ mol。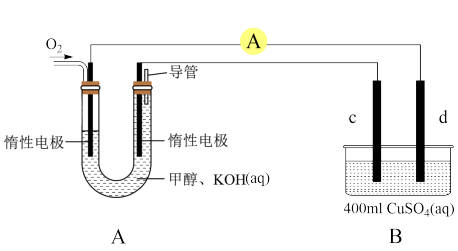
(1)工业上一般采用下列反应合成甲醇:CO(g)+2H2(g)
 CH3OH(g) ΔH
CH3OH(g) ΔH①下列数据是在不同温度下的化学平衡常数(K)。
| 250℃:K1=__________ | 300℃:K2=0.270 | 350℃:K3=0.012 |
由表中数据判断ΔH
②250℃,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得:CO剩余0.4mol,求K1
(2)已知在常温常压下:①CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=-442.8KJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0kJ/mol
写出甲醇燃烧热的热化学方程式
(3)某实验小组依据甲醇燃烧的反应原理,设计如图(A)所示的燃料电池装置。则:
①该燃料电池负极的电极反应为:
②用该甲醇燃料电池对B池进行电解,已知c、d是质量相同的铜棒,电解2min后,取出c、d,洗净、烘干、称量,质量差为0.64g,在通电过程中,电路中通过的电子为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】Ⅰ.甲醇燃料电池是符合绿色化学理念的新型燃料电池,如图是以甲醇燃料电池(甲池)为电源的电解装置。已知:A、B、C、D、E、F都是惰性电极,丙中为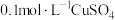 溶液(假设反应前后溶液体积不变),当向甲池通入物质a和b时,D极附近呈红色。
溶液(假设反应前后溶液体积不变),当向甲池通入物质a和b时,D极附近呈红色。___________ 。
(2)乙装置中D电极方程式为___________ 。
(3)丙装置中总反应的离子方程式为___________ 。
(4)当乙装置中C电极收集到224mL(标况)气体时,丙中溶液的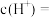
___________ mol。
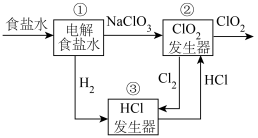
Ⅱ.二氧化氯(ClO2)是一种高效、广谱、安全、会与碱反应的杀菌、消毒剂。利用食盐水制取ClO2的工业流程如下图所示: 的装置。写出阳极产生
的装置。写出阳极产生 的电极反应式:
的电极反应式:___________ 。电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为___________ mol。
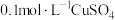 溶液(假设反应前后溶液体积不变),当向甲池通入物质a和b时,D极附近呈红色。
溶液(假设反应前后溶液体积不变),当向甲池通入物质a和b时,D极附近呈红色。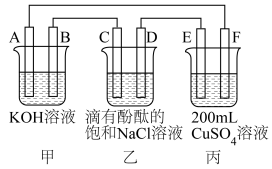
(2)乙装置中D电极方程式为
(3)丙装置中总反应的离子方程式为
(4)当乙装置中C电极收集到224mL(标况)气体时,丙中溶液的
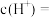
Ⅱ.二氧化氯(ClO2)是一种高效、广谱、安全、会与碱反应的杀菌、消毒剂。利用食盐水制取ClO2的工业流程如下图所示:
 的装置。写出阳极产生
的装置。写出阳极产生 的电极反应式:
的电极反应式: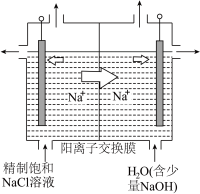
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)如图1为某原电池装置示意图,若A为Cu,B为石墨,电解质为 溶液,工作时的总反应为:
溶液,工作时的总反应为: 写出B的电极反应式
写出B的电极反应式______ ;该电池在工作时,A电极的质量将______ (填“增加”或“减少”或“不变”)。
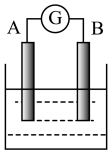
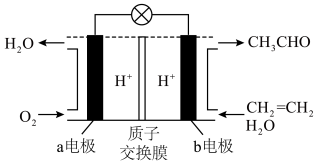
图1 图2
(2)一种新型燃料电池可用于制取乙醛( ),总反应式为
),总反应式为 ,电池的主要构成要素如图2所示,请回答下列问题:
,电池的主要构成要素如图2所示,请回答下列问题:
①a电极为燃料电池的______ 极,该电极的电极反应式为______ 。
②电池工作时, 由
由______ 电极(填“a”或“b”,下同)移向______ 电极。
③生成2.2g乙醛时,需要消耗标准状况下的氧气______ mL。
(1)如图1为某原电池装置示意图,若A为Cu,B为石墨,电解质为
 溶液,工作时的总反应为:
溶液,工作时的总反应为: 写出B的电极反应式
写出B的电极反应式

图1 图2
(2)一种新型燃料电池可用于制取乙醛(
 ),总反应式为
),总反应式为 ,电池的主要构成要素如图2所示,请回答下列问题:
,电池的主要构成要素如图2所示,请回答下列问题:①a电极为燃料电池的
②电池工作时,
 由
由③生成2.2g乙醛时,需要消耗标准状况下的氧气
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:
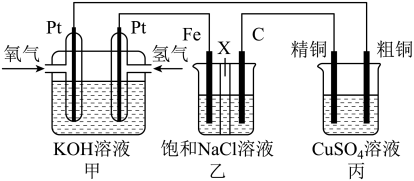
(1)石墨电极为_______ (填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入”酚酞溶液,_______ (填“铁极”或“石墨极”)区的溶液先变红。乙池中电解总反应化学方程式为_______ 。
(2)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,溶液中硫酸铜浓度将_______ (填“增大”“减小”或“不变”)。精铜电极上的电极反应式为_______ 。
(3)若在标准状况下,有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下体积为_______ mL;丙装置中阴极析出铜的质量为_______ g。
(4)若将甲改用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得燃料电池,则该电池正极反应式为_______ 。

(1)石墨电极为
(2)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,溶液中硫酸铜浓度将
(3)若在标准状况下,有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下体积为
(4)若将甲改用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得燃料电池,则该电池正极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】如下图所示的装置,C、D、E、F都是惰性电极。将电源接通后,向乙中滴入酚酞试液.在F极附近显红色。
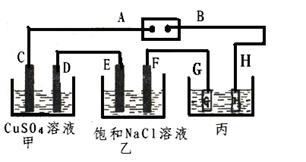
试回答以下问题:
(1)电极A的名称是__________ 。
(2)甲装置中D电极的电极反应式:________________ 。
(3) 在25℃时若用惰性电极电解饱和NaCl溶液一段时间,当阳极产生5.6L(标准状况下)一种气体,电解后溶液体积为50L时,求所得溶液在25℃时的氢氧化钠物质的量浓度=_____________ 。
(4)欲用丙装置给铜镀银,G应该是___________ (填“银”或“铜”), 电镀液的主要成分是(填化学式)_____________ 。

试回答以下问题:
(1)电极A的名称是
(2)甲装置中D电极的电极反应式:
(3) 在25℃时若用惰性电极电解饱和NaCl溶液一段时间,当阳极产生5.6L(标准状况下)一种气体,电解后溶液体积为50L时,求所得溶液在25℃时的氢氧化钠物质的量浓度=
(4)欲用丙装置给铜镀银,G应该是
您最近一年使用:0次



