利用铝热反应焊接钢轨的原理是2Al+Fe2O3 2Fe+Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褐色硬块的组成。
2Fe+Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褐色硬块的组成。
(1)将褐色硬块处理成粉末状。研究小组首先排除了含有单质Al杂质的可能性,实验方法是__ ,证明不含单质铝的现象是__ 。
(2)该褐色硬块的组成基本确定为Fe、Fe2O3,Al2O3。请以上述粉末为样品,验证其组成。限选实验仪器与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、过滤器;20%KSCN、3 mol·L-1NaOH、3mol·L-1HCl、3mol·L-1HNO3、3mol·L-1CuSO4、0.01mol·L-1KMnO4、蒸馏水。
根据你设计的实验方案,叙述实验操作、预期现象和结论。_____ 。
 2Fe+Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褐色硬块的组成。
2Fe+Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褐色硬块的组成。(1)将褐色硬块处理成粉末状。研究小组首先排除了含有单质Al杂质的可能性,实验方法是
(2)该褐色硬块的组成基本确定为Fe、Fe2O3,Al2O3。请以上述粉末为样品,验证其组成。限选实验仪器与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、过滤器;20%KSCN、3 mol·L-1NaOH、3mol·L-1HCl、3mol·L-1HNO3、3mol·L-1CuSO4、0.01mol·L-1KMnO4、蒸馏水。
根据你设计的实验方案,叙述实验操作、预期现象和结论。
| 实验操作 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: | |
| 步骤3: | |
| 步骤4: |
更新时间:2020-01-29 17:45:15
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】某小组在实验室中模拟侯氏制碱法制备NaHCO3,并探究钠及其常见化合物的相关性质和应用,实验流程如图所示:
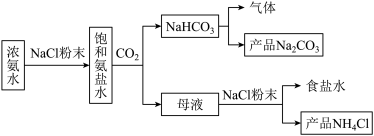
(1)写出由浓氨水生成NaHCO3的总反应的离子方程式:______ 。
(2)侯氏制碱法中NH3和CO2的通入顺序为先通入______ (填化学式,下同),后通入_____ 。
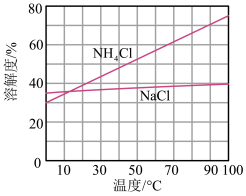
(3)向母液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)→NaCl(aq)+NH4Cl(s)过程,为了充分析出并分离出NH4Cl,根据如图中物质溶解度曲线知,需采取的操作为_____ 、过滤、洗涤、干燥。
(4)NaHCO3长期放置在空气中会变质(部分转变为Na2CO3),现欲测定某NaHCO3样品中NaHCO3的质量分数,设计如下实验方案(假设产生的气体全部与Na2O2反应):
i.取一定质量的样品加水溶解后与如图所示的硫酸VmL恰好反应。
ii.将i中产生的气体用浓硫酸干燥后缓慢地通入足量的Na2O2粉末中充分反应,Na2O2粉末增重mg
①图中硫酸的物质的量浓度是______ 。
②标准状况下i中产生气体的体积为______ L(用含m的代数式表示)。样品中小苏打的物质的量是______ mol(用含m、V的代数式表示)。

(1)写出由浓氨水生成NaHCO3的总反应的离子方程式:
(2)侯氏制碱法中NH3和CO2的通入顺序为先通入
(3)向母液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)→NaCl(aq)+NH4Cl(s)过程,为了充分析出并分离出NH4Cl,根据如图中物质溶解度曲线知,需采取的操作为

(4)NaHCO3长期放置在空气中会变质(部分转变为Na2CO3),现欲测定某NaHCO3样品中NaHCO3的质量分数,设计如下实验方案(假设产生的气体全部与Na2O2反应):
i.取一定质量的样品加水溶解后与如图所示的硫酸VmL恰好反应。
ii.将i中产生的气体用浓硫酸干燥后缓慢地通入足量的Na2O2粉末中充分反应,Na2O2粉末增重mg
| 名称:硫酸 分子式:H2SO4 密度:1.84 g·cm-3 质量分数:98% |
②标准状况下i中产生气体的体积为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】化学兴趣小组的同学为测定某Na2CO3和NaCl的固体混合物样品中Na2CO3的质量分数进行了以下实验,请你参与并完成对有关问题的解答。
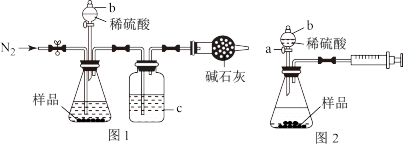
(1)甲同学用图1所示装置测定CO2的质量。实验时稀硫酸是与样品中的__________ (填“Na2CO3”或"NaCl”)发生反应。仪器b的名称是_____________ 。洗气瓶c中盛装的是浓硫酸,此浓硫酸的作用是__________________________________________ 。
(2)乙同学用图2所示装置,取一定质量的样品(为m g;已测得)和足量稀硫酸反应进行实验,完成样品中Na2CO3质量分数的测定。
①实验前,检查该装置气密性的方法是先打开活塞a,由b注入水至其下端玻璃管中形成一段水柱,再将针筒活塞向内推压,若b下端玻璃管中的________ 上升,则装置气密性良好。
②在实验完成时,能直接测得的数据是CO2的___________ (填“体积”或“质量”)。
(3)丙同学用下图所示方法和步骤实验:
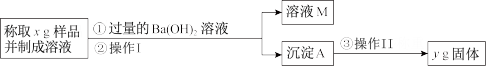
①操作I涉及的实验名称有___________ 、洗涤;操作Ⅱ涉及的实验名称有干燥、____________ 。
②丙测得的样品中Na2CO3质量分数的计算式为___________________________ 。

(1)甲同学用图1所示装置测定CO2的质量。实验时稀硫酸是与样品中的
(2)乙同学用图2所示装置,取一定质量的样品(为m g;已测得)和足量稀硫酸反应进行实验,完成样品中Na2CO3质量分数的测定。
①实验前,检查该装置气密性的方法是先打开活塞a,由b注入水至其下端玻璃管中形成一段水柱,再将针筒活塞向内推压,若b下端玻璃管中的
②在实验完成时,能直接测得的数据是CO2的
(3)丙同学用下图所示方法和步骤实验:

①操作I涉及的实验名称有
②丙测得的样品中Na2CO3质量分数的计算式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】某化学自主实验小组通过实验探究NO2、NH3的性质
探究I:利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持及固定装置略去)。
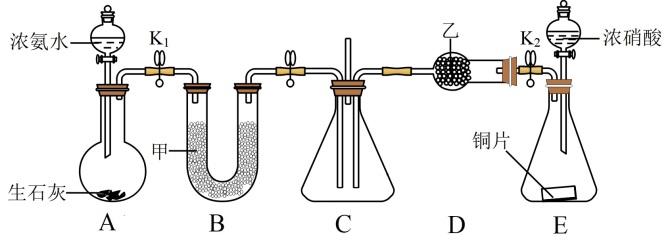
(1)按图示连接好实验装置,检查A装置气密性的方法是_______
(2)U形管中的药品是_______ (填名称)
(3)可用NH3将NO2转化为无毒气体,写出该反应的化学方程式:_______ ,此反应中氧化产物和还原产物的质量之比为_______ 。
(4)此实验装置存在的一个明显缺陷是_______ 。
探究Ⅱ:采用如图装置收集NO2和O2的混合气体,探究NO2、O2混合气体的喷泉实验(装置已略去)。
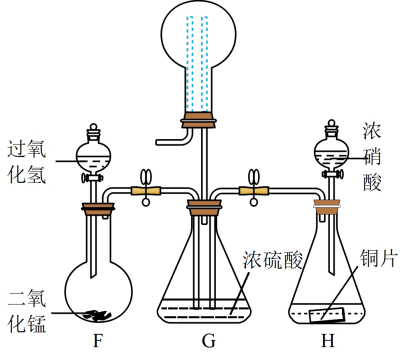
(5)G装置圆底烧瓶中的虚线表示导管,左侧导管_______ (填“长”或“短”,下同),右侧导管_______
(6)将G装置上面的圆底烧瓶收集满气体进行喷泉实验,若混合气体全部被吸收(Vm≈22.4L/mol),则所得溶液物质的量浓度为_______ mol∙L−1 (保留两位有效数字)
探究I:利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持及固定装置略去)。

(1)按图示连接好实验装置,检查A装置气密性的方法是
(2)U形管中的药品是
(3)可用NH3将NO2转化为无毒气体,写出该反应的化学方程式:
(4)此实验装置存在的一个明显缺陷是
探究Ⅱ:采用如图装置收集NO2和O2的混合气体,探究NO2、O2混合气体的喷泉实验(装置已略去)。

(5)G装置圆底烧瓶中的虚线表示导管,左侧导管
(6)将G装置上面的圆底烧瓶收集满气体进行喷泉实验,若混合气体全部被吸收(Vm≈22.4L/mol),则所得溶液物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
(1)将镁、铝、铁各0.1 mol分别投入到过量且等量的0.1 mol·L-1的盐酸中,写出与盐酸反应最慢的金属发生反应的化学方程式__________________ 。
(2)利用下图装置可以验证非金属性的变化规律。

①实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属比硫强;装置B中所装药品为_____________ ,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_________________________ 。
②若要证明非金属性:C>Si,则A中加________ 、B中加Na2CO3、C中加Na2SiO3,观察到C中的实验现象为有白色沉淀物生成。离子方程式为_____________ (所通气体过量)。
(1)将镁、铝、铁各0.1 mol分别投入到过量且等量的0.1 mol·L-1的盐酸中,写出与盐酸反应最慢的金属发生反应的化学方程式
(2)利用下图装置可以验证非金属性的变化规律。

①实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属比硫强;装置B中所装药品为
②若要证明非金属性:C>Si,则A中加
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】分别向盛有①紫色石蕊溶液 ②NaOH溶液 ③品红溶液 ④酸性高锰酸钾溶液的试管中通入SO2气体。
(1)试管①中的现象:___________ 发生反应的化学方程式是:_________________ 。
(2)试管②中发生反应的化学方程式是:_____________________ ,如果通入过量的SO2,则发生反应的化学方程式为:_______________________________ 。
(5)上述实验中,SO2表现出酸性氧化物性质的是___________ (填试管标号,下同),SO2表现出漂白性的是___________ 。SO2表现出还原性的是___________ 。
(1)试管①中的现象:
(2)试管②中发生反应的化学方程式是:
(3)试管③中的现象:
(4)试管④中的现象:
(5)上述实验中,SO2表现出酸性氧化物性质的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】为了讲授“氯气的性质和用途”,某老师利用二氧化锰和浓盐酸为主要原料,设计一套如图所示的实验装置进行教学。试回答下列问题:
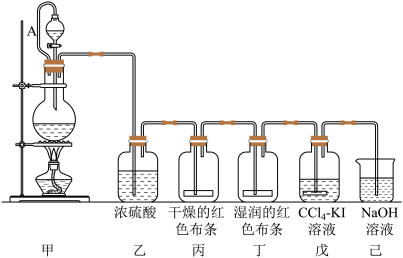
(1)乙中浓硫酸的作用是_______ ;
(2)丙中的现象是_______ ,丁中的现象是_______ ;
(3)戊中发生的离子方程式为_______ ,充分反应后戊中液体分两层,上层_______ 色,下层_______ 色,分离戊中液体的方法是_______ ;
(4)利用甲装置也可以制HCl气体,吸收多余的HCl气体合适的装置是_______ ;
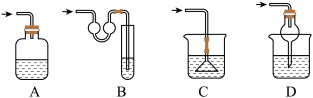
(5)标准状况下,制得11.2L的Cl2,将其通入足量NaOH溶液中完全吸收,则消耗NaOH的物质的量为_______ 。

(1)乙中浓硫酸的作用是
(2)丙中的现象是
(3)戊中发生的离子方程式为
(4)利用甲装置也可以制HCl气体,吸收多余的HCl气体合适的装置是

(5)标准状况下,制得11.2L的Cl2,将其通入足量NaOH溶液中完全吸收,则消耗NaOH的物质的量为
您最近一年使用:0次



