为了讲授“氯气的性质和用途”,某老师利用二氧化锰和浓盐酸为主要原料,设计一套如图所示的实验装置进行教学。试回答下列问题:
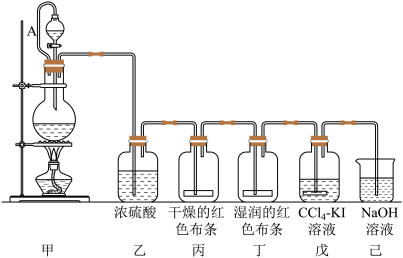
(1)乙中浓硫酸的作用是_______ ;
(2)丙中的现象是_______ ,丁中的现象是_______ ;
(3)戊中发生的离子方程式为_______ ,充分反应后戊中液体分两层,上层_______ 色,下层_______ 色,分离戊中液体的方法是_______ ;
(4)利用甲装置也可以制HCl气体,吸收多余的HCl气体合适的装置是_______ ;
(5)标准状况下,制得11.2L的Cl2,将其通入足量NaOH溶液中完全吸收,则消耗NaOH的物质的量为_______ 。

(1)乙中浓硫酸的作用是
(2)丙中的现象是
(3)戊中发生的离子方程式为
(4)利用甲装置也可以制HCl气体,吸收多余的HCl气体合适的装置是

(5)标准状况下,制得11.2L的Cl2,将其通入足量NaOH溶液中完全吸收,则消耗NaOH的物质的量为
21-22高一上·上海静安·期中 查看更多[3]
上海市风华中学2021-2022学年高一上学期期中考试化学试题(已下线)2.1.2 氯气的性质-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)(已下线)第2章能力提升测评-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)
更新时间:2022-08-25 18:45:28
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
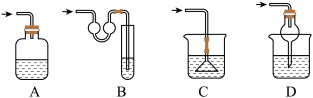
【推荐1】根据实验室制备氯气的装置(如下),回答下列问题;

(1)仪器A 和 B名称___________ ;____________
(2)写出B中发生反应的离子方程式_____________________________________
(3)装置C的作用__________________________________________
(4)装置D的作用________________________________________________
(5)检验E中氯气已经收集满的方法_________________________________________
(6)写出F中发生的反应方程式______________________________________________
(7)每生成0.5mol氯气转移________________ 个电子

(1)仪器A 和 B名称
(2)写出B中发生反应的离子方程式
(3)装置C的作用
(4)装置D的作用
(5)检验E中氯气已经收集满的方法
(6)写出F中发生的反应方程式
(7)每生成0.5mol氯气转移
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
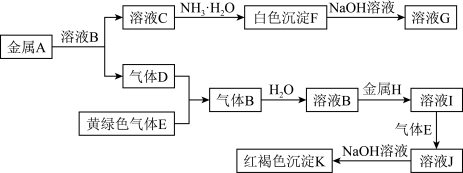
【推荐2】常温下,A是可用来对自来水进行消毒的黄绿色气体单质,A、B、C、D、E都含X元素,其转化关系如图所示。

(1)请分别写出A、B、C、D、E的化学式(如为溶液请填溶质的化学式):A._______ ,C._______ ,E. _______ 。
(2)写出下列反应的化学方程式:A+H2O:_______ 。
(3)通常情况下,为了防止污染环境,在做完实验后,多余的气体A应用NaOH溶液吸收,其反应化学方程式为_______ 。
(4)漂白粉的有效成分是_______ (填化学式),漂白粉溶于水后,受空气中的CO2作用,产生有漂白、杀菌作用的次氯酸,反应化学方程式为_______ 。

(1)请分别写出A、B、C、D、E的化学式(如为溶液请填溶质的化学式):A.
(2)写出下列反应的化学方程式:A+H2O:
(3)通常情况下,为了防止污染环境,在做完实验后,多余的气体A应用NaOH溶液吸收,其反应化学方程式为
(4)漂白粉的有效成分是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质。甲同学设计了如图所示的实验装置(注:氯气可溶于四氯化碳溶液)。
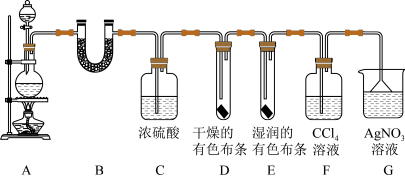
请按要求回答下列问题:
(1)若用含0.2molHCl的浓盐酸与足量的MnO2反应制取Cl2,制得的Cl2体积总是小于1.12L(标准状况下)的原因是___________ 。
(2)①装置B中盛放的试剂为无水硫酸铜,其作用是___________ ,现象是___________ 。
②装置D和E中出现的不同现象说明的问题是___________ 。
③写出装置G中发生反应的离子方程式___________ 。
(3)乙同学认为甲同学设计的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在F和G两个装置之间再加一个装置。你认为该装置中应放入___________ (填试剂或药品名称)。

请按要求回答下列问题:
(1)若用含0.2molHCl的浓盐酸与足量的MnO2反应制取Cl2,制得的Cl2体积总是小于1.12L(标准状况下)的原因是
(2)①装置B中盛放的试剂为无水硫酸铜,其作用是
②装置D和E中出现的不同现象说明的问题是
③写出装置G中发生反应的离子方程式
(3)乙同学认为甲同学设计的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在F和G两个装置之间再加一个装置。你认为该装置中应放入
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】 是安全高效的灭菌消毒剂,下图是实验室制备较纯净的
是安全高效的灭菌消毒剂,下图是实验室制备较纯净的 的装置(某些夹持装置省略)。
的装置(某些夹持装置省略)。

已知:①通常情况下, 是一种有刺激性气味的黄绿色气体,遇热或见光不稳定。
是一种有刺激性气味的黄绿色气体,遇热或见光不稳定。
②氯气和二氧化氯的沸点。
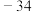 ℃
℃  11℃。
11℃。
(1)导管a的作用是___________ 。装置b的名称为___________ 。
(2)A中发生反应的离子方程式为___________ 。
(3)为制得纯净的氯气,B、C中试剂依次为___________ 、___________ 。(填名称)
(4)D为 的发生装置。化学方程式为
的发生装置。化学方程式为___________ 。
(5)E中装置选择___________ (填“G”或“H”)。

 是安全高效的灭菌消毒剂,下图是实验室制备较纯净的
是安全高效的灭菌消毒剂,下图是实验室制备较纯净的 的装置(某些夹持装置省略)。
的装置(某些夹持装置省略)。
已知:①通常情况下,
 是一种有刺激性气味的黄绿色气体,遇热或见光不稳定。
是一种有刺激性气味的黄绿色气体,遇热或见光不稳定。②氯气和二氧化氯的沸点。

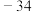 ℃
℃  11℃。
11℃。(1)导管a的作用是
(2)A中发生反应的离子方程式为
(3)为制得纯净的氯气,B、C中试剂依次为
(4)D为
 的发生装置。化学方程式为
的发生装置。化学方程式为(5)E中装置选择

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】DCCNa( )是一种高效、安全的消毒杀菌剂。它常温下为白色固体,难溶于冷水,受热易分解。利用NaClO溶液和氰尿酸
)是一种高效、安全的消毒杀菌剂。它常温下为白色固体,难溶于冷水,受热易分解。利用NaClO溶液和氰尿酸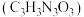 溶液反应制备DCCNa。实验装置如图所示:
溶液反应制备DCCNa。实验装置如图所示:


回答下列问题:
(1)装置Ⅰ中发生反应的化学方程式为
(2)仪器b的名称为
(3)装置Ⅱ中溶液a为
(4)当装置Ⅲ中的三颈烧瓶内液面上方有黄绿色气体时,再加入氰尿酸溶液。并在整个过程中不断通入一定量的氯气,其原因是
(5)装置Ⅳ中的试剂可选用
a.
 b.NaCl c.
b.NaCl c. d.
d.
(6)反应结束后,装置Ⅲ中三颈烧瓶内的浊液经过滤、
(7)有效氯含量是判断产品质量的标准。通过下列方法测定有效氯含量的原理为:
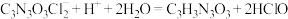


准确称取1.2000g样品,配成250mL溶液。取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min,用
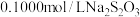 标准溶液滴定至溶液呈微黄色,加入淀粉溶液作指示剂继续滴定至终点,消耗
标准溶液滴定至溶液呈微黄色,加入淀粉溶液作指示剂继续滴定至终点,消耗 溶液20.00mL。该样品的有效氯为
溶液20.00mL。该样品的有效氯为已知:该样品的有效氯

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐1】以黄铜矿(CuFeS2)为主要原料的炼铜方法有火法炼铜、氧化浸出、生物浸出、配位浸出、电化学浸出法等。
Ⅰ.火法炼铜:8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2 ΔH<0
8Cu+4FeO+2Fe2O3+16SO2 ΔH<0
(1)反应中被氧化的元素是________________ (填元素符号)。
(2)实际生产是在沸腾炉中进行,反应温度为 600~620℃。控制反应温度的方法是________________ 。
(3)冶炼过程中产生大量SO2,下列处理方案中合理的是________ (填字母)。
A.高空排放 B.制备硫酸
C.用纯碱溶液吸收制Na2SO3 D.用浓硫酸吸收
Ⅱ.氧化浸出:在硫酸介质中用双氧水将黄铜矿氧化,测得有 生成。
生成。
(4)配平该反应方程式:___ CuFeS2+___ H2O2+___ H+
___ Cu2++___ Fe3++___  +
+___ H2O。
(5)该反应在25~50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,除温度较高双氧水分解之外,还可能的原因是__________________________________________________ 。
Ⅲ.生物浸出:
在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,反应釜中各物质的转化关系如图所示。
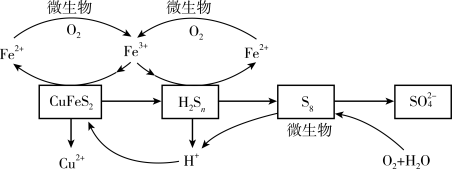
(6)在微生物的作用下,可以循环使用的物质有_________ (填化学式)。
(7)假如黄铜矿中的铁元素最终全部转化为Fe3+,当有2 mol 生成时,理论上消耗O2的物质的量为
生成时,理论上消耗O2的物质的量为_______________________ 。
Ⅰ.火法炼铜:8CuFeS2+21O2
 8Cu+4FeO+2Fe2O3+16SO2 ΔH<0
8Cu+4FeO+2Fe2O3+16SO2 ΔH<0(1)反应中被氧化的元素是
(2)实际生产是在沸腾炉中进行,反应温度为 600~620℃。控制反应温度的方法是
(3)冶炼过程中产生大量SO2,下列处理方案中合理的是
A.高空排放 B.制备硫酸
C.用纯碱溶液吸收制Na2SO3 D.用浓硫酸吸收
Ⅱ.氧化浸出:在硫酸介质中用双氧水将黄铜矿氧化,测得有
 生成。
生成。(4)配平该反应方程式:

 +
+(5)该反应在25~50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,除温度较高双氧水分解之外,还可能的原因是
Ⅲ.生物浸出:
在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,反应釜中各物质的转化关系如图所示。

(6)在微生物的作用下,可以循环使用的物质有
(7)假如黄铜矿中的铁元素最终全部转化为Fe3+,当有2 mol
 生成时,理论上消耗O2的物质的量为
生成时,理论上消耗O2的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】轻质碳酸钙(CaCO3)是一种重要的化工产品,广泛应用于油漆、塑料、橡胶和造纸等工业。一种以低品位石灰石(含CaCO3、MnCO3、Fe2O3及A12O3)为原料生产高纯度轻质碳酸钙的循环工艺流程如图:
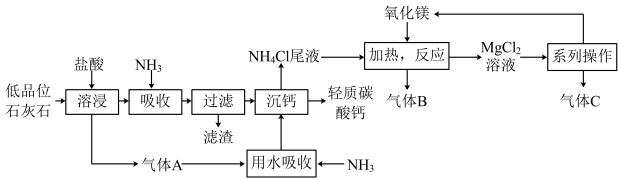
回答下列问题:
(1)气体A为:______ ,滤渣的主要成分是______ 。
(2)“沉钙”过程中发生的化学反应方程式为______ 。
(3)在NH4C1尾液中加入氧化镁并加热,发生反应的离子方程式为______ 。
(4)“系列操作”包含有:______ 。
(5)氧化镁可以在尾液处理中循环使用,______ 和_______ 可循环使用于石灰石制备轻质碳酸钙的过程中。
(6)轻质碳酸钙的工业生产还可以使用“石灰碳化法”:用高品位石灰石焙烧制得生石灰,生石灰消化制得氢氧化钙,再通入二氧化碳制得碳酸钙;本题工艺流程与“石灰碳化法,相比,优点是:______ ,______ 。

回答下列问题:
(1)气体A为:
(2)“沉钙”过程中发生的化学反应方程式为
(3)在NH4C1尾液中加入氧化镁并加热,发生反应的离子方程式为
(4)“系列操作”包含有:
(5)氧化镁可以在尾液处理中循环使用,
(6)轻质碳酸钙的工业生产还可以使用“石灰碳化法”:用高品位石灰石焙烧制得生石灰,生石灰消化制得氢氧化钙,再通入二氧化碳制得碳酸钙;本题工艺流程与“石灰碳化法,相比,优点是:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】FeCl3是一种常用的净水剂,化学研究小组用如图装置制备无水FeCl3。已知无水FeCl3在空气中易潮解,加热易升华。结合下列制备无水FeCl3的装置,回答以下问题:

(1)A中发生反应的离子方程式为_____ 。
(2)装置接口的连接顺序为a→ → → → → → →b(用b、c……i表示)_____ 。
(3)装置B的作用_____ 。
(4)如果拆去E和F装置,可能的后果是_____ 。
(5)证明产品中存在Fe3+的操作是_____ 。

(1)A中发生反应的离子方程式为
(2)装置接口的连接顺序为a→ → → → → → →b(用b、c……i表示)
(3)装置B的作用
(4)如果拆去E和F装置,可能的后果是
(5)证明产品中存在Fe3+的操作是
您最近一年使用:0次