在银锌原电池中,以硫酸铜溶液为电解质溶液。
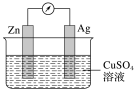
(1)锌为____ 极,电极上发生的是____ (填“氧化”或“还原”)反应。电极反应式为____ ,锌片上观察到的现象为________ 。
(2)银为________ 极,电极上发生的是_____ (填“氧化”或“还原”)反应,电极反应式是________ ,银片上观察到的现象是________ 。
(3)该电池中,每有2mol电子流过导线,负极___ (填“减少”或“增加”)___ g,正极____ (填“减少”或“增加”)________ g。

(1)锌为
(2)银为
(3)该电池中,每有2mol电子流过导线,负极
更新时间:2020-01-30 11:53:33
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某化学兴趣小组的同学为了探究铝电极在电池中的作用,设计并进行了以下一系列实验,实验结果记录如表:
试根据表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极(正极或负极)______ (填“相同”或“不相同”)。
(2)对实验3完成下列填空:
①铝为_____ 极,电极反应式:______ 。
②石墨为_____ 极,电极反应式:______ 。
③电池总反应方程式:______ 。
(3)实验4中铝作______ ,理由是______ 。写出铝电极的电极反应式:______ 。
(4)解释实验5中电流计指针偏向铝的原因:______ 。
(5)根据实验结果总结出影响铝在原电池中作正极或负极的因素:______ 。
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
(1)实验1、2中Al所作的电极(正极或负极)
(2)对实验3完成下列填空:
①铝为
②石墨为
③电池总反应方程式:
(3)实验4中铝作
(4)解释实验5中电流计指针偏向铝的原因:
(5)根据实验结果总结出影响铝在原电池中作正极或负极的因素:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
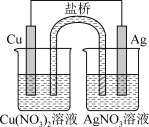
(1)某同学用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂—KNO3的U形管)设计成一个原电池,如图。下列判断中正确的是 。
(2)利用电化学原理,将CO、O2和熔融K2CO3制成燃料电池,模拟工业电解法处理含Cr2O 的废水,如图。电解过程中溶液中发生如下反应:Cr2O
的废水,如图。电解过程中溶液中发生如下反应:Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O。
+6Fe2++14H+=2Cr3++6Fe3++7H2O。

①甲池内阳离子向石墨___ 移动。(填“Ⅰ”或者“Ⅱ”)
②如图,CO在石墨Ⅰ电极放电生成Y,Y可循环使用。甲池工作时,石墨Ⅱ附近发生的电极反应式为___ 。
③Fe(Ⅰ)的电极反应式为___ 。
④甲中消耗0.12 molCO,最多可以处理含Cr2O
___ mol的废水。
(1)某同学用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂—KNO3的U形管)设计成一个原电池,如图。下列判断中正确的是 。

A.实验过程中,左侧烧杯NO 变大 变大 |
| B.若用U形铜代替盐桥,装置中无电流产生 |
| C.若用U形铜代替盐桥,则左池中电能转化成化学能,右池中化学能转化成电能 |
| D.若用U形铜代替盐桥,一段时间之后U形铜的质量减小 |
 的废水,如图。电解过程中溶液中发生如下反应:Cr2O
的废水,如图。电解过程中溶液中发生如下反应:Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O。
+6Fe2++14H+=2Cr3++6Fe3++7H2O。
①甲池内阳离子向石墨
②如图,CO在石墨Ⅰ电极放电生成Y,Y可循环使用。甲池工作时,石墨Ⅱ附近发生的电极反应式为
③Fe(Ⅰ)的电极反应式为
④甲中消耗0.12 molCO,最多可以处理含Cr2O

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学电源广泛地应用于现代社会的生产和生活。请回答下列问题:
(1)原电池的设计原理与某类化学反应有关。你认为下列化学反应,可以设计成原电池的是_______(填字母)。
(2)化学反应均涉及相应的能量变化,为探究这些能量变化,某同学设计了如图实验。

①该实验过程涉及的能量变化是_______ 。
②Zn棒是_______ 极,电流方向是从_______ 棒流向_______ 棒。
(3)若将两个金属棒用导线相连在一起,总质量为80.00 g的锌片和银片同时浸入稀硫酸中,工作一段时间后,取出金属片,进行洗涤、干燥、称量,得金属片的总质量为63.75 g,则装置工作时锌片上的电极反应式为_______ ,工作时间内装置所产生氢气的体积为_______ L(标准状况)。
(4)回答下列问题:

①该燃料电池中正极通入的物质是_______ ,负极发生的反应式为_______ 。
②电池工作时,OH-移向_______ 电极(填“a”或“b”)。
③当电池放电转移10 mol电子时,至少消耗燃料肼_______ g。
(1)原电池的设计原理与某类化学反应有关。你认为下列化学反应,可以设计成原电池的是_______(填字母)。
| A.CaO+H2O=Ca(OH)2 | B.C+CO2 2CO 2CO |
| C.NaOH+HCl=NaCl+H2O | D.2FeCl3+Cu=2FeCl2+CuCl2 |

①该实验过程涉及的能量变化是
②Zn棒是
(3)若将两个金属棒用导线相连在一起,总质量为80.00 g的锌片和银片同时浸入稀硫酸中,工作一段时间后,取出金属片,进行洗涤、干燥、称量,得金属片的总质量为63.75 g,则装置工作时锌片上的电极反应式为
(4)回答下列问题:

①该燃料电池中正极通入的物质是
②电池工作时,OH-移向
③当电池放电转移10 mol电子时,至少消耗燃料肼
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氮及其化合物在化肥、医药、材料等领域具有广泛应用,一定温度下,在容积固定为2L的密闭容器内充入4molN2,发生反应: ,测得不同时刻N4的浓度如下表:
,测得不同时刻N4的浓度如下表:
请回答下列问题。
(1)10min时,该反应的化学反应速率
___________  (填“>”、“=”或“<”)。从反应开始到15min,用N4表示的平均反应速率为
(填“>”、“=”或“<”)。从反应开始到15min,用N4表示的平均反应速率为___________ 。
(2)该反应达到平衡时,N2的转化率为___________ 。
(3)以下操作可以使化学反应速率变快的是___________ (填字母)。
A.将容器体积变为1L B.适当降低温度 C.加入合适的催化剂
D.恒压条件下通入He E.恒容条件下通入He
(4)N4分子呈正四面体结构,结构如图所示。已知断裂1molN—N键吸收170kJ热量,断裂 键吸收942kJ热量,则1molN2气体转化为N4时要
键吸收942kJ热量,则1molN2气体转化为N4时要________ (填“吸收”或“放出”)热量_________ kJ。

(5)若在恒容绝热条件下发生上述反应,下列叙述能判断该反应达到平衡状态的是_______(填字母)。
(6)有人设想以N2和H2为反应物,以溶有A的盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。

①A是___________ (填化学式)。
②该电池正极的电极反应式是___________ 。
 ,测得不同时刻N4的浓度如下表:
,测得不同时刻N4的浓度如下表:| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
N4的浓度/ | 0 | 0.21 | 0.38 | 0.45 | 0.48 | 0.50 | 0.50 |
(1)10min时,该反应的化学反应速率

 (填“>”、“=”或“<”)。从反应开始到15min,用N4表示的平均反应速率为
(填“>”、“=”或“<”)。从反应开始到15min,用N4表示的平均反应速率为(2)该反应达到平衡时,N2的转化率为
(3)以下操作可以使化学反应速率变快的是
A.将容器体积变为1L B.适当降低温度 C.加入合适的催化剂
D.恒压条件下通入He E.恒容条件下通入He
(4)N4分子呈正四面体结构,结构如图所示。已知断裂1molN—N键吸收170kJ热量,断裂
 键吸收942kJ热量,则1molN2气体转化为N4时要
键吸收942kJ热量,则1molN2气体转化为N4时要
(5)若在恒容绝热条件下发生上述反应,下列叙述能判断该反应达到平衡状态的是_______(填字母)。
A. | B.温度不变 |
| C.混合气体的密度不变 | D.混合气体的平均相对分子质量不变 |

①A是
②该电池正极的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电池与工农业生产、日常生活有着密切的关联。请回答下列问题:
(1)燃料电池是目前电池研究的热点之一、某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。

①负极是___________ (填“a”或“b”),该电极上发生___________ (填“氧化”或“还原”)反应。
②b极发生的电极反应式是___________ 。
③标准状况下,消耗11.2L 时,转移的电子数为
时,转移的电子数为___________ 。
(2)某同学利用家中废旧材料制作可使扬声器发出声音的电池,装置如下图所示。下列说法正确的是___________ (填字母)。

A.电子由铝制易拉罐经导线流向碳棒 B.在碳棒上有气体生成,该气体可能为氢气
C.铝质易拉罐逐渐被腐蚀,说明铝失去电子 D.扬声器发声,说明该装置将电能转化为化学能
(3)铁及其化合物应用广泛,如 可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
①写出 溶液腐蚀印刷电路铜板的离子方程式:
溶液腐蚀印刷电路铜板的离子方程式:___________ 。
②若将①中的反应设计成原电池,请画出该原电池的装置图,标出正、负极和电解质溶液___________ 。
(1)燃料电池是目前电池研究的热点之一、某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。

①负极是
②b极发生的电极反应式是
③标准状况下,消耗11.2L
 时,转移的电子数为
时,转移的电子数为(2)某同学利用家中废旧材料制作可使扬声器发出声音的电池,装置如下图所示。下列说法正确的是

A.电子由铝制易拉罐经导线流向碳棒 B.在碳棒上有气体生成,该气体可能为氢气
C.铝质易拉罐逐渐被腐蚀,说明铝失去电子 D.扬声器发声,说明该装置将电能转化为化学能
(3)铁及其化合物应用广泛,如
 可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。①写出
 溶液腐蚀印刷电路铜板的离子方程式:
溶液腐蚀印刷电路铜板的离子方程式:②若将①中的反应设计成原电池,请画出该原电池的装置图,标出正、负极和电解质溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】美国圣路易斯大学研制新型的乙醇燃料电池,用质子(H+)溶剂,在200 ℃左右供电。电池总反应为C2H5OH+3O2=2CO2+3H2O,如图是该电池的示意图,回答以下问题
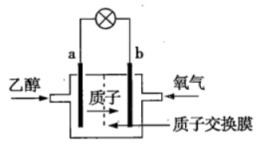
(1)该电池的正极为_________ (“a”或“b”),
(2)电池正极的电极反应为______________________________ ;负极的电极反应为_______________________________ 。
(3)电池工作时,1 mol乙醇被氧化时,有________ mol电子转移;
(4)电池工作一段时间后,a极附近溶液的pH________ (“增大”或“减小”)

(1)该电池的正极为
(2)电池正极的电极反应为
(3)电池工作时,1 mol乙醇被氧化时,有
(4)电池工作一段时间后,a极附近溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如下图所示,装置Ⅰ为甲醇燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。

(1)b处应通入______ (填“CH3OH”或“O2”),a处电极上发生的电极反应式是______ ;
(2)电镀结束后,装置Ⅰ中溶液的pH______ (填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度______ ;
(3)若铜电极质量减小6.4 g,则消耗标况下的O2的体积为______ 。
(4)若将装置I中电解质溶液换成硫酸溶液,则在工作过程中H+ 移向______ 电极(填“a”或“b”)。

(1)b处应通入
(2)电镀结束后,装置Ⅰ中溶液的pH
(3)若铜电极质量减小6.4 g,则消耗标况下的O2的体积为
(4)若将装置I中电解质溶液换成硫酸溶液,则在工作过程中H+ 移向
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】2017年12月,我省多地对除电能汽车外的其他小型车辆实行限行,这将大力推动电能汽车时代的开启。请回答下列有关电化学问题。
(1)下图原电池装置中,正极反应式为__________ 。若在工作过程中右侧电极质量增加3.2g,左侧电极质量减少2.4g,则该电池工作时化学能转化为电能的百分比为__________ 。

(2)若将上述电池改进成如下图的装置,可以大大提高电能的转化率,其理由是__________ 。若起始两侧溶液的体积均为100mL,(放电过程中的体积变化忽略不计),当左侧消耗2.8gFe时,左侧溶液中
__________ 。

(3)工业上采用电解NO的方法制备 ,其工作原理如下图。两极均为Pt电极,为使电解产物全部转化为
,其工作原理如下图。两极均为Pt电极,为使电解产物全部转化为 ,需补充
,需补充 。
。

①阴极上的电极反应式为__________ 。
②若两极上共有22.4L(标准状况 发生反应,则生成
发生反应,则生成 的质量为
的质量为_______ g。
(1)下图原电池装置中,正极反应式为

(2)若将上述电池改进成如下图的装置,可以大大提高电能的转化率,其理由是


(3)工业上采用电解NO的方法制备
 ,其工作原理如下图。两极均为Pt电极,为使电解产物全部转化为
,其工作原理如下图。两极均为Pt电极,为使电解产物全部转化为 ,需补充
,需补充 。
。
①阴极上的电极反应式为
②若两极上共有22.4L(标准状况
 发生反应,则生成
发生反应,则生成 的质量为
的质量为
您最近一年使用:0次


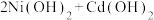 ,已知
,已知 和
和 均难溶于水但能溶于酸。
均难溶于水但能溶于酸。 )和
)和 组合形成的质子交换膜燃料电池的结构示意图如下图所示,已知该燃料电池的总反应
组合形成的质子交换膜燃料电池的结构示意图如下图所示,已知该燃料电池的总反应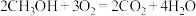 。
。


