回答下列问题:
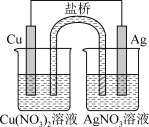
(1)某同学用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂—KNO3的U形管)设计成一个原电池,如图。下列判断中正确的是 。
(2)利用电化学原理,将CO、O2和熔融K2CO3制成燃料电池,模拟工业电解法处理含Cr2O 的废水,如图。电解过程中溶液中发生如下反应:Cr2O
的废水,如图。电解过程中溶液中发生如下反应:Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O。
+6Fe2++14H+=2Cr3++6Fe3++7H2O。

①甲池内阳离子向石墨___ 移动。(填“Ⅰ”或者“Ⅱ”)
②如图,CO在石墨Ⅰ电极放电生成Y,Y可循环使用。甲池工作时,石墨Ⅱ附近发生的电极反应式为___ 。
③Fe(Ⅰ)的电极反应式为___ 。
④甲中消耗0.12 molCO,最多可以处理含Cr2O
___ mol的废水。
(1)某同学用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂—KNO3的U形管)设计成一个原电池,如图。下列判断中正确的是 。

A.实验过程中,左侧烧杯NO 变大 变大 |
| B.若用U形铜代替盐桥,装置中无电流产生 |
| C.若用U形铜代替盐桥,则左池中电能转化成化学能,右池中化学能转化成电能 |
| D.若用U形铜代替盐桥,一段时间之后U形铜的质量减小 |
 的废水,如图。电解过程中溶液中发生如下反应:Cr2O
的废水,如图。电解过程中溶液中发生如下反应:Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O。
+6Fe2++14H+=2Cr3++6Fe3++7H2O。
①甲池内阳离子向石墨
②如图,CO在石墨Ⅰ电极放电生成Y,Y可循环使用。甲池工作时,石墨Ⅱ附近发生的电极反应式为
③Fe(Ⅰ)的电极反应式为
④甲中消耗0.12 molCO,最多可以处理含Cr2O

更新时间:2021-10-25 20:26:17
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,将除去表面氧化膜的 AI、Cu片插入电解质A溶液中组成原电池,如图所示。
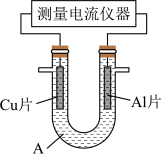
(1)若A 为稀盐酸,则Al片做____ 极,Cu片电极反应式为________ 。
(2)若A为NaOH 溶液, 则 Al片做_____ 极,该电极的电极反应式为___________ 。
(3)若A 为浓 HNO3,反应过程中有红棕色气体产生。开始时,原电池的负极是________ ,正极的电极反应式为_________ ,一段时间后,原电池中电子流动方向发生改变,此时负极的电极反应式为_____ 。

(1)若A 为稀盐酸,则Al片做
(2)若A为NaOH 溶液, 则 Al片做
(3)若A 为浓 HNO3,反应过程中有红棕色气体产生。开始时,原电池的负极是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图所示为原电池装置示意图。回答下列问题:

(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是____ (填字母)。
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出A电极反应式:____ ;该电池在工作时,B电极的质量将____ (填“增加”“减小”或“不变”)。若该电池反应消耗了0.1molH2SO4,则转移电子的数目为____ 。
(3)若A、B均为铂片,电解质为H2SO4溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:____ ;该电池在工作过程中,正极附近溶液的pH值____ (填“增大”、“减小”或“不变”)若该电池工作时转移了0.4mol电子,则生成水的质量为____ 。

(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是
| A.铝片、铜片 | B.铜片、铝片 | C.铝片、铝片 | D.铜片、铜片 |
(3)若A、B均为铂片,电解质为H2SO4溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.光合作用是由二氧化碳与水合成葡萄糖,同时放出氧气。设想将该反应倒过来,可设计成一个原电池,产生电流,这样就将太阳能转变成了电能。
(1)写出该原电池的总反应式:______________________________________
(2)写出该电池在酸性介质中放电的电极反应式:
负极:_____________________________________________
正极:_____________________________________________
Ⅱ.类比思维是学习化学的重要方法,但结果是否正确必须经受检验。在进行类比思维的时候,不能机械类比,一定要注意一些物质的特殊性,以防止类比出错误的结论。凭已有的化学知识,下列类比结果正确的是:(填标序号)___________________ 。若错误,在其后写出正确的。
①在相同条件下,Na2CO3溶解度比NaHCO3大
类比:在相同条件下,CaCO3溶解度比Ca(HCO3)2大
正确的应该为(若类比正确,此处不写,下同。):______________________________ 。
②向次氯酸钙溶液中通过量CO2:CO2 + ClO- + H2O = HCO3- + HClO
类比:向次氯酸钠溶液中通过量SO2:SO2 + ClO- +H2O = HSO3- + HClO
正确的应该为:___________________________________________ 。
③根据化合价Fe3O4可表示为:FeO·Fe2O3类比:Fe3I8也可表示为FeI2·2FeI3
正确的应该为:________________________________ 。
④CaC2能水解:CaC2+2H2O =Ca(OH)2 + C2H2↑
类比:Al4C3也能水解:Al4C3+ 12H2O = 4Al(OH)3↓+ 3CH4↑
正确的应该为:________________________________ 。
Ⅲ.常温下,某水溶液M中存在的离子有:Na+、A-、H+、OH-。若该溶液M由 pH=3的HA溶液 mL与pH=11的NaOH溶液
mL与pH=11的NaOH溶液 mL混合反应而得,则下列说法中正确的是
mL混合反应而得,则下列说法中正确的是_____________________ (填字母)。
A. 若溶液M呈中性,则溶液M中C(H+)+C(OH-)=2×10-7mol·L-1
B. 若V1=V2,则溶液M的pH一定等于7
C. 若溶液M呈酸性,则V1一定大于V2
D. 若溶液M呈碱性,则V1一定小于V2
(1)写出该原电池的总反应式:
(2)写出该电池在酸性介质中放电的电极反应式:
负极:
正极:
Ⅱ.类比思维是学习化学的重要方法,但结果是否正确必须经受检验。在进行类比思维的时候,不能机械类比,一定要注意一些物质的特殊性,以防止类比出错误的结论。凭已有的化学知识,下列类比结果正确的是:(填标序号)
①在相同条件下,Na2CO3溶解度比NaHCO3大
类比:在相同条件下,CaCO3溶解度比Ca(HCO3)2大
正确的应该为(若类比正确,此处不写,下同。):
②向次氯酸钙溶液中通过量CO2:CO2 + ClO- + H2O = HCO3- + HClO
类比:向次氯酸钠溶液中通过量SO2:SO2 + ClO- +H2O = HSO3- + HClO
正确的应该为:
③根据化合价Fe3O4可表示为:FeO·Fe2O3类比:Fe3I8也可表示为FeI2·2FeI3
正确的应该为:
④CaC2能水解:CaC2+2H2O =Ca(OH)2 + C2H2↑
类比:Al4C3也能水解:Al4C3+ 12H2O = 4Al(OH)3↓+ 3CH4↑
正确的应该为:
Ⅲ.常温下,某水溶液M中存在的离子有:Na+、A-、H+、OH-。若该溶液M由 pH=3的HA溶液
 mL与pH=11的NaOH溶液
mL与pH=11的NaOH溶液 mL混合反应而得,则下列说法中正确的是
mL混合反应而得,则下列说法中正确的是A. 若溶液M呈中性,则溶液M中C(H+)+C(OH-)=2×10-7mol·L-1
B. 若V1=V2,则溶液M的pH一定等于7
C. 若溶液M呈酸性,则V1一定大于V2
D. 若溶液M呈碱性,则V1一定小于V2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题。
(1)理论上不能设计为原电池的化学反应是___________ 。
a.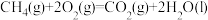
b.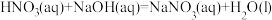
c.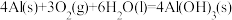
d.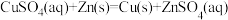
(2)某小组为探究 与
与 能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和 溶液的琼脂)。该装置石墨棒上发生的电极反应式为
溶液的琼脂)。该装置石墨棒上发生的电极反应式为___________ ,盐桥中 向
向___________ 烧杯移动(填“甲”或“乙”)。___________ ,B电极的电极反应方程式为___________ 。 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式___________ 。
(5)汽车尾气中含有的 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气史
传感器可监测汽车尾气史 含量,其工作原理如图所示:
含量,其工作原理如图所示: 电极为
电极为___________ (填“正极”或“负极), 电极上发生的电极反应式为
电极上发生的电极反应式为___________ 。
(1)理论上不能设计为原电池的化学反应是
a.
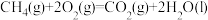
b.
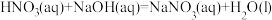
c.
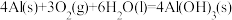
d.
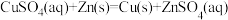
(2)某小组为探究
 与
与 能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和 溶液的琼脂)。该装置石墨棒上发生的电极反应式为
溶液的琼脂)。该装置石墨棒上发生的电极反应式为 向
向
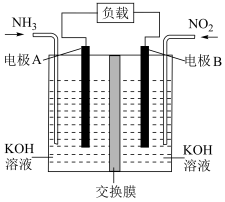
 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式(5)汽车尾气中含有的
 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气史
传感器可监测汽车尾气史 含量,其工作原理如图所示:
含量,其工作原理如图所示:
 电极为
电极为 电极上发生的电极反应式为
电极上发生的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】据报道,摩托罗拉公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。下图是一个电化学过程的示意图。已知甲池的总反应式为:2CH3OH+3O2+4KOH 2K2CO3+6H2O
2K2CO3+6H2O

请填空:
(1)放电时:负极的电极反应式为_____________________________________________ 。
(2)充电时:①原电池的负极与电源_________ 极相连。
②阳极的电极反应为__________________ 。
(3)在此过程中若完全反应,乙池中B极的质量升高648g,则甲池中理论上消耗O2_________ L(标准状况下)。
 2K2CO3+6H2O
2K2CO3+6H2O
请填空:
(1)放电时:负极的电极反应式为
(2)充电时:①原电池的负极与电源
②阳极的电极反应为
(3)在此过程中若完全反应,乙池中B极的质量升高648g,则甲池中理论上消耗O2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】甲烷水蒸气催化重整是制高纯氢的方法之一
(1)反应器中初始反应的生成物为H2和CO2,其物质的量之比为4:1,甲烷和水蒸气反应的方程式是___________ 。
(2)该反应认为是可逆反应。某温度时,在容积为2L的密闭容器中发生这一反应。其中,H2O(g)和CO2的物质的量随时间变化的曲线如右图所示。分析图中数据,回答下列问题。___________
②4min时,正反应速率___________ 逆反应速率(填“>”“<或“=”)
(3)已知反应器中还存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) △H1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) △H2
iii.CH4(g)=C(s)+2H2(g) △H3
……
iii为积炭反应,利用△H1和△H2计算△H3时,还需要利用___________ 反应的△H.
(4)对于反应C(s)+CO2(g) 2CO(g),一定温度下,足量的碳与一定量CO2发生上述反应,下列可判断反应已达到平衡状态的是
2CO(g),一定温度下,足量的碳与一定量CO2发生上述反应,下列可判断反应已达到平衡状态的是___________ 。
a.v正(CO2)=2v逆(CO)
b.CO2与CO的体积分数之比保持不变
c.恒容条件下,混合气体的平均密度不变
d.恒压条件下,混合气体的平均密度不变
(5)利用太阳能实现室温下甲烷重整制氢,电解质为稀硫酸。如图所示。___________ 极(填“正”或“负”)。
②写出负极的电极反应式___________ 。
(1)反应器中初始反应的生成物为H2和CO2,其物质的量之比为4:1,甲烷和水蒸气反应的方程式是
(2)该反应认为是可逆反应。某温度时,在容积为2L的密闭容器中发生这一反应。其中,H2O(g)和CO2的物质的量随时间变化的曲线如右图所示。分析图中数据,回答下列问题。
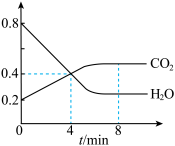
②4min时,正反应速率
(3)已知反应器中还存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) △H1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) △H2
iii.CH4(g)=C(s)+2H2(g) △H3
……
iii为积炭反应,利用△H1和△H2计算△H3时,还需要利用
(4)对于反应C(s)+CO2(g)
 2CO(g),一定温度下,足量的碳与一定量CO2发生上述反应,下列可判断反应已达到平衡状态的是
2CO(g),一定温度下,足量的碳与一定量CO2发生上述反应,下列可判断反应已达到平衡状态的是a.v正(CO2)=2v逆(CO)
b.CO2与CO的体积分数之比保持不变
c.恒容条件下,混合气体的平均密度不变
d.恒压条件下,混合气体的平均密度不变
(5)利用太阳能实现室温下甲烷重整制氢,电解质为稀硫酸。如图所示。
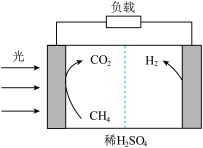
②写出负极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】电化学普遍应用于生活和生产中,前途广泛,是科研的重点方向。
(1)铅蓄电池为常见的二次电池,其原理为:Pb+PbO2+H2SO4 2PbSO4↓+2H2O。放电时,能量转化形式为
2PbSO4↓+2H2O。放电时,能量转化形式为___________ (填“化学能转化为电能”或“电能转化为化学能”),正极反应式为___________ ,外电路每流过1mole-,负极质量的改变为___________ g。充电时,原负极应接外接电源的___________ 极。
(2)工业上采用Fe、C为电极电解碱性 溶液制备
溶液制备 。电解时,应以
。电解时,应以___________ (填“Fe”、“C”)作阴极 ,电解时阳极 反应式为___________ ,电解过程中阴极 附近溶液pH将会___________ (填“增大”、“减小”或“不变”)。
(3)用原电池原理可以除去酸性废水中的三氯乙烯和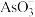 ,其原理如图所示(导电壳内部为纳米铁)。
,其原理如图所示(导电壳内部为纳米铁)。
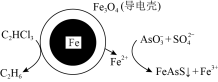
正极电极反应式为___________ 。
(1)铅蓄电池为常见的二次电池,其原理为:Pb+PbO2+H2SO4
 2PbSO4↓+2H2O。放电时,能量转化形式为
2PbSO4↓+2H2O。放电时,能量转化形式为(2)工业上采用Fe、C为电极电解碱性
 溶液制备
溶液制备 。电解时,应以
。电解时,应以(3)用原电池原理可以除去酸性废水中的三氯乙烯和
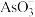 ,其原理如图所示(导电壳内部为纳米铁)。
,其原理如图所示(导电壳内部为纳米铁)。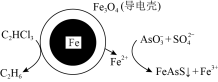
正极电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列问题
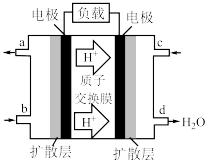
(1)最近,我国在甲烷燃料电池的相关技术上获得了新突破,原理如图所示。甲烷燃料应从___________ 填字母)口通入,发生的电极反应式为___________ 。
(2)人工肾脏可采用电化学方法除去代谢产物中的尿素【化学式为 】,其原理如图所示。
】,其原理如图所示。
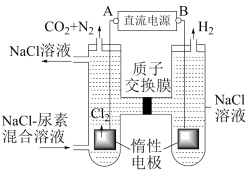
直流电源的负极为___________ (填“A”或“B”)。写出阳极室中生成的氯气氧化尿素的化学反应方程式:___________ 。电解结束后,阴极室中溶液的 与电解前相比将
与电解前相比将___________ (填“升高”“降低”或“不变”);
(3) 资源化利用是实现碳中和的重要途径。
资源化利用是实现碳中和的重要途径。
电化学法将 转化为甲酸:科学家近年发明了一种新型
转化为甲酸:科学家近年发明了一种新型 水介质电池。如图所示,电极分别为金属锌和选择性催化材料,放电时,
水介质电池。如图所示,电极分别为金属锌和选择性催化材料,放电时, 被转化为储氢物质甲酸。
被转化为储氢物质甲酸。
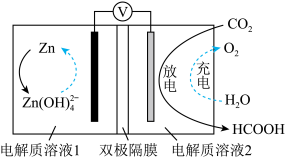
注:双极隔膜为一层阳离子交换膜和一层阴离子交换膜复合而成,中间为水,作为电解质溶液中 和
和 的来源。
的来源。
①放电时,正极电极反应式为___________ 。
②充电时每生成 ,理论上阴极获得Zn的物质的量为
,理论上阴极获得Zn的物质的量为___________  。
。
③与 极室相连的离子交换膜为
极室相连的离子交换膜为___________ 。
(1)最近,我国在甲烷燃料电池的相关技术上获得了新突破,原理如图所示。甲烷燃料应从

(2)人工肾脏可采用电化学方法除去代谢产物中的尿素【化学式为
 】,其原理如图所示。
】,其原理如图所示。
直流电源的负极为
 与电解前相比将
与电解前相比将(3)
 资源化利用是实现碳中和的重要途径。
资源化利用是实现碳中和的重要途径。电化学法将
 转化为甲酸:科学家近年发明了一种新型
转化为甲酸:科学家近年发明了一种新型 水介质电池。如图所示,电极分别为金属锌和选择性催化材料,放电时,
水介质电池。如图所示,电极分别为金属锌和选择性催化材料,放电时, 被转化为储氢物质甲酸。
被转化为储氢物质甲酸。
注:双极隔膜为一层阳离子交换膜和一层阴离子交换膜复合而成,中间为水,作为电解质溶液中
 和
和 的来源。
的来源。①放电时,正极电极反应式为
②充电时每生成
 ,理论上阴极获得Zn的物质的量为
,理论上阴极获得Zn的物质的量为 。
。③与
 极室相连的离子交换膜为
极室相连的离子交换膜为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】对某滴有酚酞的饱和NaCl溶液在如图装置中进行电解,回答下列问题:

(1)C极现象为___________ ,Fe极(含其周围的溶液)现象为:_____________________ 。
(2)若电解一段时间以后,将电源反接,C极电极反应式为:___________________ ,溶液中可以观察到的现象是:_____________________________________________ 。再向该溶液中通入O2,又会观察到的现象是:________________________________________________ 。

(1)C极现象为
(2)若电解一段时间以后,将电源反接,C极电极反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下图是几种电化学装置,请答下列问题。
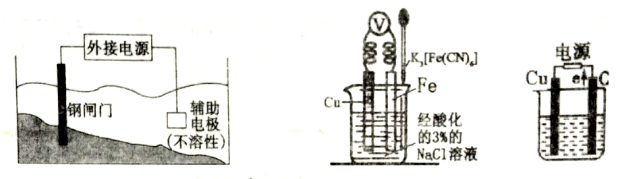
(1)图一被保护的钢闸门应与外接电源的_______ 极相连,这种方法称之为___________ ;
(2)图二往Fe极区滴入2滴黄色的K3[Fe(CN) 6]溶液,一段时间后的现象________________ 。
(3)图三烧杯中盛放足量的CuSO4溶液总反应的离子方程式为_____________________ ;25℃,若起始时盛放100mLpH =5的CuSO4溶液,一段时间后溶液的pH变为1,此时仍只有一个电极上产生气体,若要使溶液恢复到起始时的浓度(忽略溶液体积的变化),可向溶液中加入_____ (填写物质的化学式)___________ g。

(1)图一被保护的钢闸门应与外接电源的
(2)图二往Fe极区滴入2滴黄色的K3[Fe(CN) 6]溶液,一段时间后的现象
(3)图三烧杯中盛放足量的CuSO4溶液总反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某蓄电池的反应为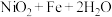

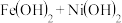
(1)放电时,正极的电极反应式为_______ ,电路中转移电子 时,生成氧化产物
时,生成氧化产物_______ g;充电时,发生氧化反应的物质是_______ ,阳极附近溶液pH_______
(2)为防止远洋轮船的钢铁船体在海水中发生腐蚀,通常在船体上镶嵌Zn块,或与该蓄电池的_______  填“正”或“负”
填“正”或“负” 极相连。
极相连。
(3)以该蓄电池作电源,实验小组同学用如图所示的装置在实验室模拟铝制品表面“钝化” 在表面形成氧化物保护膜
在表面形成氧化物保护膜 。“钝化”时阳极的电极反应为
。“钝化”时阳极的电极反应为_______ ,但有同学在实验过程中发现溶液逐渐变浑浊,并有气泡产生,其原因是_______  用电极反应式表示
用电极反应式表示

(4)精炼铜过程中,电解质溶液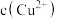 逐渐减小,
逐渐减小,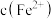 、
、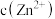 增大,会影响进一步电解精炼铜。甲同学设计如图除杂方案:
增大,会影响进一步电解精炼铜。甲同学设计如图除杂方案:

已知:
加入 的目的是
的目的是_______ ,加入CuO调节 可除去的离子是
可除去的离子是_______ ,其原因是_______  用平衡移动原理说明
用平衡移动原理说明
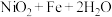

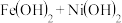
(1)放电时,正极的电极反应式为
 时,生成氧化产物
时,生成氧化产物(2)为防止远洋轮船的钢铁船体在海水中发生腐蚀,通常在船体上镶嵌Zn块,或与该蓄电池的
 填“正”或“负”
填“正”或“负” 极相连。
极相连。(3)以该蓄电池作电源,实验小组同学用如图所示的装置在实验室模拟铝制品表面“钝化”
 在表面形成氧化物保护膜
在表面形成氧化物保护膜 。“钝化”时阳极的电极反应为
。“钝化”时阳极的电极反应为 用电极反应式表示
用电极反应式表示

(4)精炼铜过程中,电解质溶液
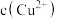 逐渐减小,
逐渐减小,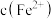 、
、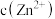 增大,会影响进一步电解精炼铜。甲同学设计如图除杂方案:
增大,会影响进一步电解精炼铜。甲同学设计如图除杂方案:
已知:
| 沉淀物 |  |  |  |  |
| 开始沉淀时的pH |  |  | 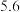 |  |
| 完全沉淀时的pH | 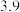 | 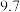 |  |  |
加入
 的目的是
的目的是 可除去的离子是
可除去的离子是 用平衡移动原理说明
用平衡移动原理说明
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理。

根据要求回答相关问题:
(1)甲装置中,通入氢气的电极为_______ (填“正极”或“负极”),该极电极反应式为_______ ;若将KOH溶液换成硫酸溶液,则正极电极反应式为_______ 。
(2)关于乙装置,下列说法正确的是_______ (填序号);
①溶液中Na+向C极移动
②从C极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后通入适量HCl可恢复到电解前电解质的浓度
④若标准状况下Fe极产生2.24L气体,则溶液中转移0.2mol电子
该装置中发生的总反应的离子方程式为_______ 。
(3)乙装置中,X为阳离子交换膜,反应一段时间后交换膜左侧溶液中pH_______ (填“增大”、“减小”或“不变”);若用饱和MgCl2溶液代替饱和氯化钠溶液,则该装置中发生的总反应_______ (填“改变”或“不变”)。
(4)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将_______ (填“增大”“减小”或“不变”),精铜电极上的电极反应式为_______ 。

根据要求回答相关问题:
(1)甲装置中,通入氢气的电极为
(2)关于乙装置,下列说法正确的是
①溶液中Na+向C极移动
②从C极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后通入适量HCl可恢复到电解前电解质的浓度
④若标准状况下Fe极产生2.24L气体,则溶液中转移0.2mol电子
该装置中发生的总反应的离子方程式为
(3)乙装置中,X为阳离子交换膜,反应一段时间后交换膜左侧溶液中pH
(4)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
您最近一年使用:0次



