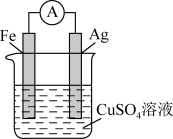
某同学根据离子反应方程式2Fe3++Fe=3Fe2+来设计原电池。下列设计方案中可行的是
| A.电极材料为铁和锌,电解质溶液为氯化铁溶液 |
| B.电极材料为铁和铜,电解质溶液为硝酸铁溶液 |
| C.电极材料为铁和石墨,电解质溶液为氯化亚铁溶液 |
| D.电极材料为石墨,电解质溶液为氯化铁溶液 |
更新时间:2020-01-29 16:05:11
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列过程中的离子反应方程式正确的是
| A.向Ca(ClO)2溶液中通入少量SO2的反应:Ca2++2ClO-+H2O+SO2=CaSO3↓+2HClO |
| B.铅蓄电池(H2SO4作电解质溶液)放电时正极上的反应:PbO2+2e-+4H+=Pb2++2H2O |
C.NaOH溶液中加入足量Ca(HCO3)2:OH-+HCO +Ca2+=CaCO3↓+H2O +Ca2+=CaCO3↓+H2O |
D.醋酸苯甲酯与足量的NaOH溶液共热: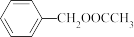 +2OH-→CH3COO-+[ +2OH-→CH3COO-+[ ]-+H2O ]-+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列叙述正确的是
①原电池是把化学能转化成电能的一种装置
②原电池的正极发生氧化反应,负极发生还原反应
③能自发进行的氧化还原反应可设计成原电池
④碳棒不能用来作原电池的正极
⑤反应Cu+2Ag+=Cu2++2Ag可以自发进行
①原电池是把化学能转化成电能的一种装置
②原电池的正极发生氧化反应,负极发生还原反应
③能自发进行的氧化还原反应可设计成原电池
④碳棒不能用来作原电池的正极
⑤反应Cu+2Ag+=Cu2++2Ag可以自发进行
| A.①③⑤ | B.①⑤ | C.②③④ | D.②⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示。反应过程中有红棕色气体产生。下列说法错误的是
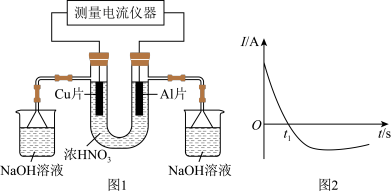

A. 时刻前,Al片的电极反应为: 时刻前,Al片的电极反应为: |
B. 时,因Al在浓硝酸中钝化,氧化膜阻碍了Al继续反应 时,因Al在浓硝酸中钝化,氧化膜阻碍了Al继续反应 |
C. 之后,正极Cu失电子,电流方向发生改变 之后,正极Cu失电子,电流方向发生改变 |
D.烧杯中NaOH溶液的作用为吸收 ,防止污染空气 ,防止污染空气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】合成氨反应为N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1。对于合成氨的反应,下列说法正确的是
2NH3(g) ΔH=-92.4 kJ·mol-1。对于合成氨的反应,下列说法正确的是
 2NH3(g) ΔH=-92.4 kJ·mol-1。对于合成氨的反应,下列说法正确的是
2NH3(g) ΔH=-92.4 kJ·mol-1。对于合成氨的反应,下列说法正确的是| A.1 mol N2和3 mol H2充分反应生成2molNH3时,会放出92.4 kJ的能量 |
| B.合成氨反应可以设计成原电池 |
| C.合成氨生产中将NH3液化分离,可加快反应速率 |
| D.在恒温、恒容条件下,N2、H2、NH3的浓度之比为1∶3∶2时说明已处于平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】关于如图装置的说法中正确的是
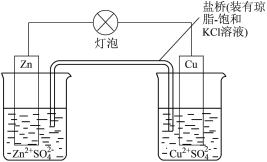
| A.该装置将锌置换铜反应中的化学能转变为电能,属于电解池 |
| B.盐桥的存在使内电路离子流动不畅,因此灯泡忽明忽暗 |
| C.相比于单池单液原电池,该装置电流更持续和稳定 |
| D.盐桥中K+向左侧烧杯移动,因为左侧是负极区 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】有一种纸电池只需滴上两滴水即可激活,为一个带有 LED 的闹钟供电 1 小时。如图所示,该电池的纸片上分布着氯化钠晶体,正面印有含有石墨薄片的油墨,反面印有含锌粉的油墨。以下说法错误的是
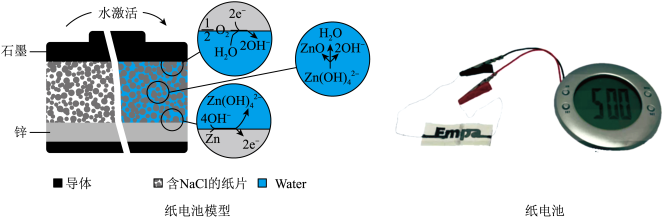

| A.石墨上发生还原反应 |
| B.电流从石墨经闹钟流向锌 |
| C.NaCl不损耗 |
| D.该电池有质量小、柔韧性好、可重复利用的优点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
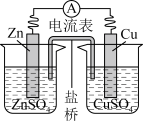
【推荐2】铜锌原电池的装置如下图,其中盐桥为内含 的琼脂凝胶,下列说法
的琼脂凝胶,下列说法不正确 的是
 的琼脂凝胶,下列说法
的琼脂凝胶,下列说法
A. 是负极反应物,发生氧化反应 是负极反应物,发生氧化反应 | B.电子从锌片流向铜片 |
C.铜电极上发生反应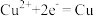 | D.盐桥中 进入 进入 溶液 溶液 |
您最近一年使用:0次