合成氨反应为N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1。对于合成氨的反应,下列说法正确的是
2NH3(g) ΔH=-92.4 kJ·mol-1。对于合成氨的反应,下列说法正确的是
 2NH3(g) ΔH=-92.4 kJ·mol-1。对于合成氨的反应,下列说法正确的是
2NH3(g) ΔH=-92.4 kJ·mol-1。对于合成氨的反应,下列说法正确的是| A.1 mol N2和3 mol H2充分反应生成2molNH3时,会放出92.4 kJ的能量 |
| B.合成氨反应可以设计成原电池 |
| C.合成氨生产中将NH3液化分离,可加快反应速率 |
| D.在恒温、恒容条件下,N2、H2、NH3的浓度之比为1∶3∶2时说明已处于平衡状态 |
更新时间:2023-05-02 10:22:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验中,反应速率加快是由催化剂引起的是( )
| A.把煤块变成煤粉燃烧更为剧烈 |
| B.锌与稀硫酸反应制H2时加入少量CuSO4溶液而使反应速率加快 |
| C.双氧水中加入少量MnO2,即可迅速放出气体 |
| D.固态FeCl3和固态NaOH混合后,加入水能迅速产生沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】100mL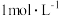 的硫酸和锌粉恰好完全反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向溶液中加入的试剂是
的硫酸和锌粉恰好完全反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向溶液中加入的试剂是
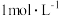 的硫酸和锌粉恰好完全反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向溶液中加入的试剂是
的硫酸和锌粉恰好完全反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向溶液中加入的试剂是| A.金属钠 | B.冰醋酸 | C.加 固体 固体 | D.硫酸铜溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 是阿伏加德罗常数的值。下列说法正确的是
是阿伏加德罗常数的值。下列说法正确的是
 是阿伏加德罗常数的值。下列说法正确的是
是阿伏加德罗常数的值。下列说法正确的是A.标准状况下,  溶于水制成饱和氯水,转移电子数目为 溶于水制成饱和氯水,转移电子数目为 |
B.   溶液中含有的 溶液中含有的 离子数为 离子数为 |
C.  氯化铵水溶液中 氯化铵水溶液中 与 与 离子数之和大于 离子数之和大于 |
D.  和 和  充分反应,生成 充分反应,生成 的数目为 的数目为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验中,对应的现象及结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向Al2(SO4)3溶液中逐滴加入NaOH溶液至过量 | 先生成白色沉淀,后沉淀消失 | Al(OH)3具有两性 |
| B | 取5mL0.1mol·L−1KI溶液于试管中,加入1mL0.1mol·L−1FeCl3溶液,充分反应后滴入5滴KSCN溶液 | 溶液变红色 | KI与FeCl3的反应存在一定的限度 |
| C | 在盛有红褐色Fe(OH)3胶体的U形管的两个管口,各插入一个电极,并使两极与直流电源相连 | 红褐色向阴极(电源负极)移动 | Fe(OH)3胶体带有正电荷 |
| D | 将新切的绿豆粒大小的Na投入到MgCl2溶液中 | 析出银白色固体 | 固体为Mg |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】 为阿伏加德罗常数的值.下列说法正确的是
为阿伏加德罗常数的值.下列说法正确的是
 为阿伏加德罗常数的值.下列说法正确的是
为阿伏加德罗常数的值.下列说法正确的是A.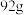 甲苯中 甲苯中 键总数为 键总数为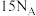 |
B.标准状况下,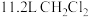 中含有的原子总数为 中含有的原子总数为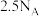 |
C.常温下,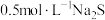 溶液中 溶液中 数目小于 数目小于 |
D.一定条件下, 和 和 充分反应后转移电子总数为 充分反应后转移电子总数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】工业制硫酸中的一步重要反应为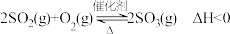 ,下列说法正确的是
,下列说法正确的是
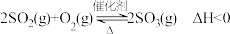 ,下列说法正确的是
,下列说法正确的是A.提高反应时的温度,可以实现 的完全转化 的完全转化 |
B.仅适当降低温度,可减小 的平衡转化率 的平衡转化率 |
| C.该反应的反应物中的化学键断裂时吸收的总能量小于生成物中的化学键形成时释放的总能量 |
| D.当混合气体的总质量不再随时间改变时,该反应达到平衡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】T °C时气体A与气体B在某容器中反应生成气体C和固体D,每1 mol A与足量B完全反应时生成1 mol D,反应过程中A、B、C浓度变化如图①所示。若保持其他条件不变,温度分别为T1和T2时,B的体积百分含量与时间的关系如图②所示。
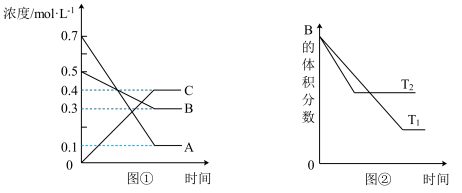
则下列结论正确的是
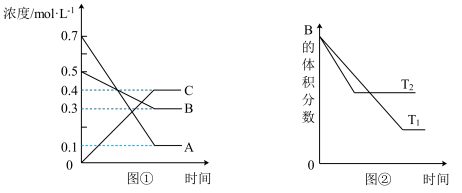
则下列结论正确的是
A.该反应的化学方程式是 A+3B 2C+D 2C+D |
| B.T°C时,保持容器体积不变,若向上述平衡体系中加入0.2 mol C,则重新达平衡时B的浓度小于0.3 mol/L |
| C.相同时间内,消耗0.3 mol/L A时,生成了0.1 mol/L B,则反应达到平衡 |
| D.其它条件不变,升高温度时,正、逆反应速率均增大,且A的转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】公元1799年,伏打以含食盐水的湿抹布,夹在银和锌的圆形板中间,堆积成圆柱状,制造出最早的电池—伏打电池(如图)。下面关于伏打电池不正确的是


| A.食盐水是电解质溶液,可以导电 | B.锌是电池的负极 |
| C.电子从银流向锌 | D.该装置实现了化学能向电能的转化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
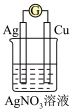
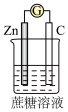
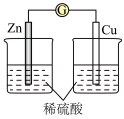
【推荐2】下列图示的装置属于原电池的是( )
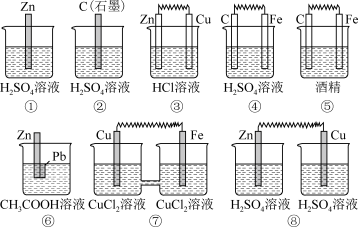

| A.①②⑥⑧ |
| B.③④⑤⑦ |
| C.③④⑥⑦ |
| D.③④⑤⑥⑦⑧ |
您最近一年使用:0次