将正确答案的序号填在空白处。
(1)用经 消毒的自来水配制下列溶液:①
消毒的自来水配制下列溶液:① ;②
;②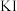 ;③
;③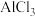 ;④
;④ ;⑤
;⑤ ;⑥稀盐酸,发现部分药品变质,它们是
;⑥稀盐酸,发现部分药品变质,它们是 ______ 。
(2)下列反应必须加入氧化剂且一步反应就能完成的是______ 。
① ②
② ③
③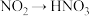 ④
④ ⑤
⑤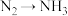
(3)在如图所示的8个装置中,属于原电池的是______ 。

(4) ①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池。
①②相连时,外电路电流从②流向①;
②③相连时,③为正极;
②④相连时,②上有气泡逸出;
③④相连时,③的质量减少.
据此判断这四种金属活动性由大到小的顺序是______ 。
(5)下列物质中,不能由单质直接化合生成的是______ 。
①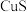 ②
②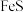 ③
③ ④
④ ⑤
⑤
(6)下列物质中,属于强电解质的是______ ;属于非电解质的是 ______ 。
①氨气 ②氨水 ③盐酸 ④醋酸 ⑤硫酸钡 ⑥氯化银 ⑦氯化钠 ⑧二氧化碳 ⑨醋酸铵⑩氢气 水
水
(1)用经
 消毒的自来水配制下列溶液:①
消毒的自来水配制下列溶液:① ;②
;②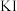 ;③
;③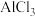 ;④
;④ ;⑤
;⑤ ;⑥稀盐酸,发现部分药品变质,它们是
;⑥稀盐酸,发现部分药品变质,它们是 (2)下列反应必须加入氧化剂且一步反应就能完成的是
①
 ②
② ③
③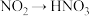 ④
④ ⑤
⑤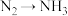
(3)在如图所示的8个装置中,属于原电池的是

(4) ①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池。
①②相连时,外电路电流从②流向①;
②③相连时,③为正极;
②④相连时,②上有气泡逸出;
③④相连时,③的质量减少.
据此判断这四种金属活动性由大到小的顺序是
(5)下列物质中,不能由单质直接化合生成的是
①
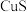 ②
②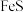 ③
③ ④
④ ⑤
⑤
(6)下列物质中,属于强电解质的是
①氨气 ②氨水 ③盐酸 ④醋酸 ⑤硫酸钡 ⑥氯化银 ⑦氯化钠 ⑧二氧化碳 ⑨醋酸铵⑩氢气
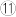 水
水
更新时间:2020-02-05 20:45:18
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有以下物质:①NaHSO4晶体,②液态氯气,③氯化氢,④水银,⑤CaCO3固体,⑥食盐水,⑦酒精(C2H5OH),⑧熔化KNO3,⑨氨水,请回答下列问题(用序号):
(1)以上物质中能导电的是__________ 。
(2)以上物质属于化合物的是_____________ 。
(3)以上物质中属于电解质的是_______ 。
(4)物质①中阴阳离子的个数比为__________ , ①在水中的电离方程式为_____________________________ 。
(5)写出③和⑨在水溶液中反应的离子方程式___________________________________
(1)以上物质中能导电的是
(2)以上物质属于化合物的是
(3)以上物质中属于电解质的是
(4)物质①中阴阳离子的个数比为
(5)写出③和⑨在水溶液中反应的离子方程式
您最近一年使用:0次
【推荐2】回答下列问题
(1)下列物质中:①NH3 ②Cu ③乙醇 ④石墨 ⑤熔融NaCl ⑥CuCl2溶液 ⑦Na2O ⑧CO2。A.属于电解质的是_______ (只填序号,下同)。B.属于非电解质的是_______ 。
(2)写出下列电解质在水中的电离方程式:
NaHCO3_______ ; BaCl2_______ 。
(3)写出下列物质间反应的离子方程式:
氢氧化铁固体溶于足量稀盐酸:_______ ;铝溶于氢氧化钠溶液中:_______ 。
(4)工业上冶炼铁的原理为:Fe2O3+3CO 2Fe+3CO2,该反应中氧化剂是
2Fe+3CO2,该反应中氧化剂是_______ (填化学式),碳元素被_______ (填“氧化”或“还原”)。
(1)下列物质中:①NH3 ②Cu ③乙醇 ④石墨 ⑤熔融NaCl ⑥CuCl2溶液 ⑦Na2O ⑧CO2。A.属于电解质的是
(2)写出下列电解质在水中的电离方程式:
NaHCO3
(3)写出下列物质间反应的离子方程式:
氢氧化铁固体溶于足量稀盐酸:
(4)工业上冶炼铁的原理为:Fe2O3+3CO
 2Fe+3CO2,该反应中氧化剂是
2Fe+3CO2,该反应中氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求回答下列问题。
(1)现有以下物质:a.NaOH溶液b.液氨c.Ba(OH)2固体d.NaHSO4e.Fe(OH)3胶体f.铜g.CO2h.盐酸
①以上物质中属于非电解质的是_____ (填序号,下同),属于电解质的有______ 。
②在足量d的水溶液中加入少量c的水溶液,发生反应的离子方程式为_____ 。
(2)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,每生成1molNa2FeO4转移的电子数为______ 。
(3)一场突如其来的新冠肺炎疫情,给人们的生活带来了巨大的冲击,“84消毒液”是家居常用的防疫用品,某小组同学查看包装说明,得到如图信息:

回答下列问题:
稀释:将“84清毒液”原液稀释配制成980mLc(NaClO)=0.05mol•L-1的溶液。
①稀释过程中,需要用到的玻璃仪器有烧杯,玻璃棒、量筒、胶头滴管、_____ 。
②稀释时,需要用量筒量取“84消毒液”原液的体积为_____ mL。
③下列操作会使配制溶液中NaClO浓度偏高的是_____ (填标号)。
A.取用久置的“84消毒液”原液进行稀释
B.量取“84消毒液”原液时,仰视读数
C.容量瓶未干燥直接使用
D.定容时,仰视刻度线
E.定容摇匀后,液面低于刻度线,再加水至刻度线
(1)现有以下物质:a.NaOH溶液b.液氨c.Ba(OH)2固体d.NaHSO4e.Fe(OH)3胶体f.铜g.CO2h.盐酸
①以上物质中属于非电解质的是
②在足量d的水溶液中加入少量c的水溶液,发生反应的离子方程式为
(2)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,每生成1molNa2FeO4转移的电子数为
(3)一场突如其来的新冠肺炎疫情,给人们的生活带来了巨大的冲击,“84消毒液”是家居常用的防疫用品,某小组同学查看包装说明,得到如图信息:

回答下列问题:
稀释:将“84清毒液”原液稀释配制成980mLc(NaClO)=0.05mol•L-1的溶液。
①稀释过程中,需要用到的玻璃仪器有烧杯,玻璃棒、量筒、胶头滴管、
②稀释时,需要用量筒量取“84消毒液”原液的体积为
③下列操作会使配制溶液中NaClO浓度偏高的是
A.取用久置的“84消毒液”原液进行稀释
B.量取“84消毒液”原液时,仰视读数
C.容量瓶未干燥直接使用
D.定容时,仰视刻度线
E.定容摇匀后,液面低于刻度线,再加水至刻度线
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌(含有Fe(Ⅱ), Mn(Ⅱ), Ni(Ⅱ)等杂质)的流程如图:
工业ZnO 浸出液
浸出液
 滤液
滤液
 滤液
滤液
 滤饼
滤饼 ZnO
ZnO
已知:在本实验条件下,Ni(Ⅱ)不能被氧化,高锰酸钾的还原产物是MnO2
反应④中产物的成分可能是ZnCO3·xZn(OH)2 。取干燥后的滤饼11.2g,煅烧后可得到产品8.1 g。 则x等于_______ 。
工业ZnO
 浸出液
浸出液
 滤液
滤液
 滤液
滤液
 滤饼
滤饼 ZnO
ZnO已知:在本实验条件下,Ni(Ⅱ)不能被氧化,高锰酸钾的还原产物是MnO2
反应④中产物的成分可能是ZnCO3·xZn(OH)2 。取干燥后的滤饼11.2g,煅烧后可得到产品8.1 g。 则x等于
您最近一年使用:0次
【推荐2】氢氧化钠是白色固体,易潮解,具有强腐蚀性,所以又叫火碱、烧碱、苛性钠。是常用的碱性干燥剂,是重要的化工原料。
工业制法:氯碱工业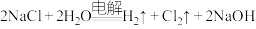
苛化法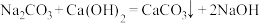
在实验室,钠、氧化钠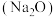 、过氧化钠
、过氧化钠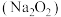 分别与水反应都生成
分别与水反应都生成
回答下列问题:
(1)在“氯碱工业”反应中,反应前后氯元素的化合价变化是_______ (填“升高”、“降低”、“不变”)。
(2) 可拆写,苛化法反应前后
可拆写,苛化法反应前后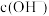
___________ (填“变大”、“变小”、“不变”)。
(3)写出 与水反应的化学方程式
与水反应的化学方程式___________ 。
(4)补项:过氧化钠与水反应为: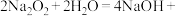
___________ ↑。
(5) 固体不能干燥酸性气体。能用
固体不能干燥酸性气体。能用 固体干燥的气体是
固体干燥的气体是___________ (填序号)。
a. b.
b. c.
c. (碱性气体) d.
(碱性气体) d.
(6)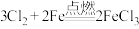 ,氯化铁能催化双氧水分解
,氯化铁能催化双氧水分解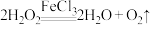 其反应机理为:①
其反应机理为:① ;②
;② 。在反应①中,
。在反应①中, 是还原剂,在反应②中,
是还原剂,在反应②中, 是
是___________ 剂(填“氧化”或“还原”)。
工业制法:氯碱工业
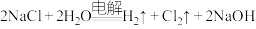
苛化法
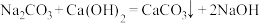
在实验室,钠、氧化钠
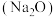 、过氧化钠
、过氧化钠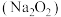 分别与水反应都生成
分别与水反应都生成
回答下列问题:
(1)在“氯碱工业”反应中,反应前后氯元素的化合价变化是
(2)
 可拆写,苛化法反应前后
可拆写,苛化法反应前后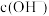
(3)写出
 与水反应的化学方程式
与水反应的化学方程式(4)补项:过氧化钠与水反应为:
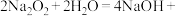
(5)
 固体不能干燥酸性气体。能用
固体不能干燥酸性气体。能用 固体干燥的气体是
固体干燥的气体是a.
 b.
b. c.
c. (碱性气体) d.
(碱性气体) d.
(6)
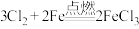 ,氯化铁能催化双氧水分解
,氯化铁能催化双氧水分解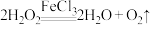 其反应机理为:①
其反应机理为:① ;②
;② 。在反应①中,
。在反应①中, 是还原剂,在反应②中,
是还原剂,在反应②中, 是
是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】金属加工后的废弃液中含2%~5%的NaNO2,它是一种环境污染物。人们用NH4Cl溶液来处理此废弃液,使 NaNO2溶液转化为无毒物质。该反应分两步进行。
第一步:NaNO2+NH4Cl=NaCl+NH4NO2,第二步:NH4NO2 N2↑+2H2O。
N2↑+2H2O。
①第一步属于__________ 反应,第二步属于__________ 反应。(填基本反应类型)
②在上述氧化还原反应中,__________ 被氧化,__________ 被还原;__________ 是氧化剂,__________ 是氧化产物。
③用双线桥法分析上述氧化还原反应:___________________ 。
第一步:NaNO2+NH4Cl=NaCl+NH4NO2,第二步:NH4NO2
 N2↑+2H2O。
N2↑+2H2O。①第一步属于
②在上述氧化还原反应中,
③用双线桥法分析上述氧化还原反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】依据与水反应情况对某些物质进行分类,如下图所示。回答下列问题:
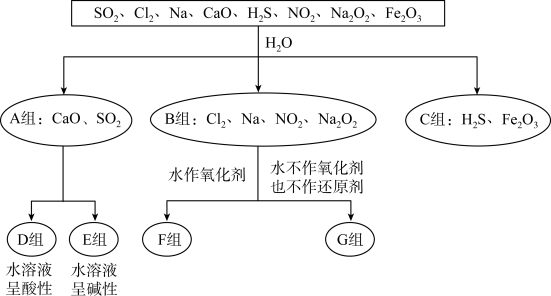
(1)上述物质中属于碱性氧化物的有___________ (填化学式);D组物质属于___________ (填“电解质”或“非电解质”)。
(2) 组物质与水反应的离子方程式为
组物质与水反应的离子方程式为___________ 。
(3)将 通入紫色石蕊溶液中,现象为
通入紫色石蕊溶液中,现象为___________ ;将 通入
通入 溶液中,反应的化学方程式为
溶液中,反应的化学方程式为___________ 。
(4) 和
和 都是常见的消毒剂。工业上可通过反应:
都是常见的消毒剂。工业上可通过反应: 制备
制备 ,其中
,其中 的氧化性比
的氧化性比
___________ (填“强”或“弱”),当消耗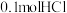 时,转移电子的数目为
时,转移电子的数目为___________ 。

(1)上述物质中属于碱性氧化物的有
(2)
 组物质与水反应的离子方程式为
组物质与水反应的离子方程式为(3)将
 通入紫色石蕊溶液中,现象为
通入紫色石蕊溶液中,现象为 通入
通入 溶液中,反应的化学方程式为
溶液中,反应的化学方程式为(4)
 和
和 都是常见的消毒剂。工业上可通过反应:
都是常见的消毒剂。工业上可通过反应: 制备
制备 ,其中
,其中 的氧化性比
的氧化性比
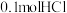 时,转移电子的数目为
时,转移电子的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列6种物质:①硫酸②纯碱③二氧化碳④蔗糖⑤熔融NaOH⑥氨水
(1)上述物质中属于电解质的是__ (填序号,下同),属于非电解质的是__ ,能导电的是__ 。
(2)写出①在水中的电离方程式__ ,①能与上述物质中的某一种在溶液中发生离子反应:H++OH-=H2O,则该物质是__ (填序号)。
(3)向氯水中滴加②的溶液,有气体生成,请解释该现象产生的原因__ 。
(1)上述物质中属于电解质的是
(2)写出①在水中的电离方程式
(3)向氯水中滴加②的溶液,有气体生成,请解释该现象产生的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】中国疾控中心指出,消毒是疫情防控的重要措施。含氯消毒剂是一种高效、安全的杀菌消毒剂。
(1)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气-氯水体系,该体系中Cl2(aq)、HClO和ClO-的物质的量分数(α)随pH变化的关系如图所示。
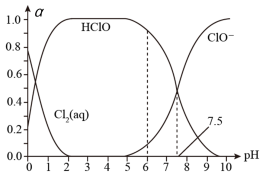
由图分析,用氯气处理饮用水时,pH=7.5与pH=6时杀菌效果强的是pH为___________ ,当pH=7.5时,氯水中含氯元素的微粒有___________ 。
(2)Ca(ClO)2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,NaClO2中Cl元素的化合价为___________ ,写出工业上用氯气与石灰乳反应生产漂白粉的化学方程式:___________ 。
(3)ClO2是国际上公认的高效、安全的杀菌消毒剂。
①工业制备ClO2的反应原理为:2KClO3+H2C2O4+H2SO4=K2SO4+2ClO2+2X+2H2O,X的化学式为___________ ,每生成1mol ClO2,反应中转移电子___________ mol。
②消毒能力可用单位质量消毒剂得电子多少来衡量。则ClO2与Cl2消毒能力比为___________ (整数比)。二氧化氯(ClO2)、高铁酸钠(Na2FeO4)等新型水处理剂可用于城市自来水的处理。ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+。那么ClO2、Na2FeO4、Cl2三种消毒杀菌剂的消毒效率由大到小的顺序是___________ 。
(4)工业上以CH3OH和NaClO3为原料在酸性条件下制取ClO2,同时产生CO2气体。已知该反应分两步进行,第一步反应为2ClO +2Cl-+4H+=2ClO2↑+Cl2↑+2H2O。
+2Cl-+4H+=2ClO2↑+Cl2↑+2H2O。
①第二步反应为___________ (写离子方程式)。
②工业生产时,需在反应物中加入少量Cl-,其作用是___________ 。
③生产中会发生副反应ClO +Cl−+H+→Cl2↑+H2O (未配平)若测得反应后的混合气体中Cl2的体积分数为
+Cl−+H+→Cl2↑+H2O (未配平)若测得反应后的混合气体中Cl2的体积分数为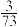 ,则起始投料时CH3OH与NaClO3的物质的量之比为
,则起始投料时CH3OH与NaClO3的物质的量之比为___________ 。
(1)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气-氯水体系,该体系中Cl2(aq)、HClO和ClO-的物质的量分数(α)随pH变化的关系如图所示。

由图分析,用氯气处理饮用水时,pH=7.5与pH=6时杀菌效果强的是pH为
(2)Ca(ClO)2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,NaClO2中Cl元素的化合价为
(3)ClO2是国际上公认的高效、安全的杀菌消毒剂。
①工业制备ClO2的反应原理为:2KClO3+H2C2O4+H2SO4=K2SO4+2ClO2+2X+2H2O,X的化学式为
②消毒能力可用单位质量消毒剂得电子多少来衡量。则ClO2与Cl2消毒能力比为
(4)工业上以CH3OH和NaClO3为原料在酸性条件下制取ClO2,同时产生CO2气体。已知该反应分两步进行,第一步反应为2ClO
 +2Cl-+4H+=2ClO2↑+Cl2↑+2H2O。
+2Cl-+4H+=2ClO2↑+Cl2↑+2H2O。①第二步反应为
②工业生产时,需在反应物中加入少量Cl-,其作用是
③生产中会发生副反应ClO
 +Cl−+H+→Cl2↑+H2O (未配平)若测得反应后的混合气体中Cl2的体积分数为
+Cl−+H+→Cl2↑+H2O (未配平)若测得反应后的混合气体中Cl2的体积分数为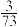 ,则起始投料时CH3OH与NaClO3的物质的量之比为
,则起始投料时CH3OH与NaClO3的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】电池是人类生产和生活中重要的能量来源,电池的发明是化学对人类的一项重大贡献。
(1)依据 NaOH与HCl的反应原理设计原电池,你认为是否可行?________ 填“是”或“否”),理由是_______________________________________________________________ 。
(2)理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Fe+Cu 2+ =Cu+Fe2+ ”设计一个化学电池(正极材料用碳棒),回答下列问题:
①电池的负极材料是__________ ,发生_____________ 反应(填“氧化”或“还原”),电解质溶液是_____________ ;
②正极上出现的现象是____________________________________________ ;
③若导线上转移电子1 mol,则生成铜___________ 克。
(3)设计一个实验方案,使如图装置中的铁棒上析出铜,而铁不溶解(作图表示)。

____________
(1)依据 NaOH与HCl的反应原理设计原电池,你认为是否可行?
(2)理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Fe+Cu 2+ =Cu+Fe2+ ”设计一个化学电池(正极材料用碳棒),回答下列问题:
①电池的负极材料是
②正极上出现的现象是
③若导线上转移电子1 mol,则生成铜
(3)设计一个实验方案,使如图装置中的铁棒上析出铜,而铁不溶解(作图表示)。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学电池在通信、交通及日常生活中有着广泛的应用。
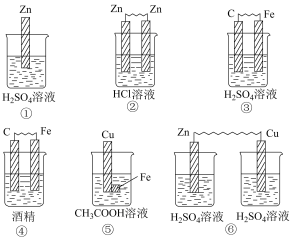
(1)下列装置中能够组成原电池的是_______ (填序号)。
(2)现有如下两个反应:A、 ;B、
;B、 。
。
①根据两反应本质,判断能否设计成原电池_______ 。
②如果不能,说明其原因_______ 。
③如果可以,请在下面方框内画出原电池装置图,注明电极材料和电解质溶液等___ 。

(3)如图是某锌锰干电池的基本构造图。
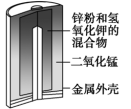
①该碱性锌锰干电池的总反应式为 ,该电池工作时负极的电极反应式是
,该电池工作时负极的电极反应式是_______ 。
②关于该电池的使用和性能,下列说法正确的是_______ 。(填字母,下同)
A.该电池属于蓄电池
B.电池工作时 向负极移动
向负极移动
C.该电池的电解质溶液是 溶液
溶液
D.该电池用完后可随意丢弃,不需要回收处理
(4)另一种常用的电池——锂电池由于比容量(单位质量电极材料所能转换的电量)特别大而广泛用于心脏起搏器,它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用化学方程式 表示不能用水溶液的原因:_______ 。
(1)下列装置中能够组成原电池的是

(2)现有如下两个反应:A、
 ;B、
;B、 。
。①根据两反应本质,判断能否设计成原电池
②如果不能,说明其原因
③如果可以,请在下面方框内画出原电池装置图,注明电极材料和电解质溶液等

(3)如图是某锌锰干电池的基本构造图。

①该碱性锌锰干电池的总反应式为
 ,该电池工作时负极的电极反应式是
,该电池工作时负极的电极反应式是②关于该电池的使用和性能,下列说法正确的是
A.该电池属于蓄电池
B.电池工作时
 向负极移动
向负极移动C.该电池的电解质溶液是
 溶液
溶液D.该电池用完后可随意丢弃,不需要回收处理
(4)另一种常用的电池——锂电池由于比容量(单位质量电极材料所能转换的电量)特别大而广泛用于心脏起搏器,它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】原电池是直接把化学能转化为电能的装置。
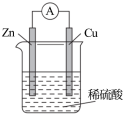
(1)如图所示:按照构成原电池的基本要素来看,Zn的作用是(填字母,下同)___________ ;稀硫酸的作用是___________ 。
a.负极反应物 b.负极材料 c.正极反应物 d.正极材料 e.离子导体 f.电子导体
(2)在Cu-Zn原电池中,能证明化学能转化为电能的实验现象为___________ 。
(3)某原电池的总反应为Zn+Cu2+=Cu+Zn2+,该原电池正确的组成是___________。
(4)从化学的角度分析,原电池装置产生电流的原因是:原电池可将___________ ,并通过能导电的物质形成闭合回路,产生电流。
(1)如图所示:按照构成原电池的基本要素来看,Zn的作用是(填字母,下同)

a.负极反应物 b.负极材料 c.正极反应物 d.正极材料 e.离子导体 f.电子导体
(2)在Cu-Zn原电池中,能证明化学能转化为电能的实验现象为
(3)某原电池的总反应为Zn+Cu2+=Cu+Zn2+,该原电池正确的组成是___________。
A.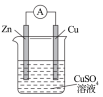 | B.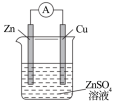 | C.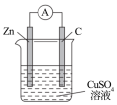 | D.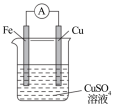 |
您最近一年使用:0次



