原电池是直接把化学能转化为电能的装置。
(1)如图所示:按照构成原电池的基本要素来看,Zn的作用是(填字母,下同)___________ ;稀硫酸的作用是___________ 。
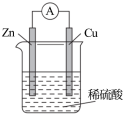
a.负极反应物 b.负极材料 c.正极反应物 d.正极材料 e.离子导体 f.电子导体
(2)在Cu-Zn原电池中,能证明化学能转化为电能的实验现象为___________ 。
(3)某原电池的总反应为Zn+Cu2+=Cu+Zn2+,该原电池正确的组成是___________。
(4)从化学的角度分析,原电池装置产生电流的原因是:原电池可将___________ ,并通过能导电的物质形成闭合回路,产生电流。
(1)如图所示:按照构成原电池的基本要素来看,Zn的作用是(填字母,下同)

a.负极反应物 b.负极材料 c.正极反应物 d.正极材料 e.离子导体 f.电子导体
(2)在Cu-Zn原电池中,能证明化学能转化为电能的实验现象为
(3)某原电池的总反应为Zn+Cu2+=Cu+Zn2+,该原电池正确的组成是___________。
A.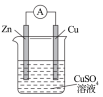 | B.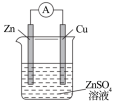 | C.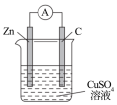 | D.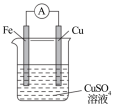 |
更新时间:2022-03-10 19:20:43
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH + HCl = NaCl+ H2O,B.2FeCl3+ Cu = 2FeCl2 + CuCl2
判断能否设计成原电池A._________ B.___________ 。(填“能”或“不能”)
(2)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生原电池腐蚀,一段时间后某电极产生3.36L标准状况下的气体。
①负极是________ (填“锌”或“铜”),发生_________ 反应(填“氧化”或“还原”);
②正极的电极反应式为________________ ;
③产生这些气体共需转移电子_______________ mol。
(1)现有如下两个反应:A.NaOH + HCl = NaCl+ H2O,B.2FeCl3+ Cu = 2FeCl2 + CuCl2
判断能否设计成原电池A.
(2)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生原电池腐蚀,一段时间后某电极产生3.36L标准状况下的气体。
①负极是
②正极的电极反应式为
③产生这些气体共需转移电子
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】理论上讲,任何自发的氧化还原反应都可以设计成原电池。请你利用下列反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池,并回答下列问题:
(1)该电池的正极材料是___________ ,负极材料是___________ ,电解质溶液是___________ 溶液。
(2)在外电路中,电流方向是从___________ 极到___________ 极。(填“正”或“负”)
(3)正极反应是___________ ,负极反应是___________ 。
(4)若有1mol的Ag析出,转移电子的数目为___________ 。
(1)该电池的正极材料是
(2)在外电路中,电流方向是从
(3)正极反应是
(4)若有1mol的Ag析出,转移电子的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组用下图装置研究原电池的工作原理。
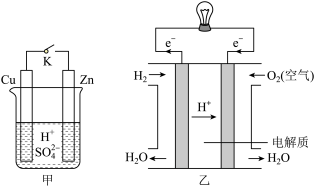
(1)甲中K断开时,装置中发生反应的离子方程式为_______________________ ;K闭合时,Cu棒上的现象为________ ,它为原电池的________ (填“正”或“负”)极。
(2)乙图为氢氧燃料电池构造示意图,其中通入氢气的一极为电池的________ (填“正”或“负”)极,发生________ (填“氧化”或“还原”)反应。
(3)某同学欲把反应Fe+2FeCl3=3FeCl2设计成原电池,请写出负极的电极反应式:_______________________________________________ 。

(1)甲中K断开时,装置中发生反应的离子方程式为
(2)乙图为氢氧燃料电池构造示意图,其中通入氢气的一极为电池的
(3)某同学欲把反应Fe+2FeCl3=3FeCl2设计成原电池,请写出负极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的项重大贡献。
(1)某课外实验小组欲探究铝和铜的金属性(原子失电子能力)强弱,同学们提出了如下实验方案:
A.比较铝和铜的硬度和熔点
B.比较二者在稀硫酸中的表现
C.用铝片、铜片、硫酸铝溶液、硫酸铜溶液,比较二者的活动性
D.分别做铝片、铜片与NaOH溶液反应的实验
E.将铝片、铜片用导线连接后共同投入稀盐酸中接入电流计,观察电流方向
上述方案中能达到实验目的的是_________________ 。
(2)现有如下两个反应:A.NaOH+HCl=NaCl+H2O B.Zn+H2SO4=ZnSO4+H2↑。上述反应中能设计成原电池的是________ (填字母代号),作负极的物质发生了________ 反应(填“氧化”或“还原”)。
(3)将纯锌片和纯铜片按如图所示方式插入100mL相同浓度的稀硫酸一段时间,回答下列问题:
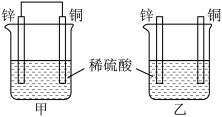
①下列说法正确的是________ (填字母代号)。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的酸性均减弱
②在相同时间内,两烧杯中产生气泡的速度:甲________ 乙(填“>”、“<”或“=”)。原因是________ 。
③当甲中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1L,测得溶液中c(H+)=0.1mol/L(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为____________ 。
(1)某课外实验小组欲探究铝和铜的金属性(原子失电子能力)强弱,同学们提出了如下实验方案:
A.比较铝和铜的硬度和熔点
B.比较二者在稀硫酸中的表现
C.用铝片、铜片、硫酸铝溶液、硫酸铜溶液,比较二者的活动性
D.分别做铝片、铜片与NaOH溶液反应的实验
E.将铝片、铜片用导线连接后共同投入稀盐酸中接入电流计,观察电流方向
上述方案中能达到实验目的的是
(2)现有如下两个反应:A.NaOH+HCl=NaCl+H2O B.Zn+H2SO4=ZnSO4+H2↑。上述反应中能设计成原电池的是
(3)将纯锌片和纯铜片按如图所示方式插入100mL相同浓度的稀硫酸一段时间,回答下列问题:

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的酸性均减弱
②在相同时间内,两烧杯中产生气泡的速度:甲
③当甲中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1L,测得溶液中c(H+)=0.1mol/L(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学电池在通信、交通及日常生活中有着广泛的应用。
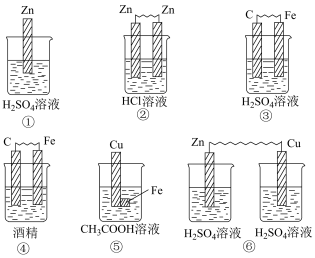
(1)下列装置中能够组成原电池的是_______ (填序号)。 ;B、
;B、 。
。
①根据两反应本质,判断能否设计成原电池。如果不能,说明其原因_______ 。
②如果可以,请在下面方框内画出原电池装置图,注明电极材料和电解质溶液等_______ 。 ,该电池工作时正极的电极反应式是
,该电池工作时正极的电极反应式是_______ 。
②关于该电池的使用和性能,下列说法正确的是_______ 。(填字母,下同)
A.该电池属于蓄电池
B.电池工作时 向负极移动
向负极移动
C.该电池的电解质溶液是 溶液
溶液
D.该电池用完后可随意丢弃,不需要回收处理
(4)另一种常用的电池——锂电池由于比容量(单位质量电极材料所能转换的电量)特别大而广泛用于心脏起搏器,它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用化学方程式 表示不能用水溶液的原因:_______ 。
(1)下列装置中能够组成原电池的是
 ;B、
;B、 。
。①根据两反应本质,判断能否设计成原电池。如果不能,说明其原因
②如果可以,请在下面方框内画出原电池装置图,注明电极材料和电解质溶液等

 ,该电池工作时正极的电极反应式是
,该电池工作时正极的电极反应式是②关于该电池的使用和性能,下列说法正确的是
A.该电池属于蓄电池
B.电池工作时
 向负极移动
向负极移动C.该电池的电解质溶液是
 溶液
溶液D.该电池用完后可随意丢弃,不需要回收处理
(4)另一种常用的电池——锂电池由于比容量(单位质量电极材料所能转换的电量)特别大而广泛用于心脏起搏器,它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)下列装置中能够组成原电池的是______ (填序号)。

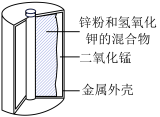
(2)如图是某锌锰干电池的基本构造图。该碱性锌锰干电池的总反应式为2MnO2+Zn+2H2O=2MnO(OH)+Zn(OH)2,该电池工作时正极的电极反应式为______ 。

(3)尿素[CO(NH2)2]燃料电池可直接去除城市废水中的尿素,既能产生净化水,又能发电。其装置如图所示:负极电极反应为:______ 。

(4)肼—空气燃料电池是一种无污染,能量高,有广泛的应用前景的燃料电池。我校高一年级化学课外活动小组设计一种肼—空气燃料电池,除将化学能转化为电能外,还能将饱和食盐水淡化,同时还可获得盐酸和NaOH两种副产品。其工作原理如图所示:

①该燃料电池A电极名称是______ ,A电极的电极反应式为_______ 。
②N膜为_____ (填“阳离子交换膜”或“阴离子交换膜”)。
③当电路中有0.2mol电子转移时,正极室质量增加_____ g。
(5)NO2、O2和熔融KNO3可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则正极反应式为_______ 。

(1)下列装置中能够组成原电池的是

(2)如图是某锌锰干电池的基本构造图。该碱性锌锰干电池的总反应式为2MnO2+Zn+2H2O=2MnO(OH)+Zn(OH)2,该电池工作时正极的电极反应式为

(3)尿素[CO(NH2)2]燃料电池可直接去除城市废水中的尿素,既能产生净化水,又能发电。其装置如图所示:负极电极反应为:

(4)肼—空气燃料电池是一种无污染,能量高,有广泛的应用前景的燃料电池。我校高一年级化学课外活动小组设计一种肼—空气燃料电池,除将化学能转化为电能外,还能将饱和食盐水淡化,同时还可获得盐酸和NaOH两种副产品。其工作原理如图所示:

①该燃料电池A电极名称是
②N膜为
③当电路中有0.2mol电子转移时,正极室质量增加
(5)NO2、O2和熔融KNO3可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则正极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】随着工业的发展,如何高效处理污水成为人类亟待解决的问题。
(1)利用原电池原理,酸性废水中的 在水处理剂(主要成分为铁粉、炭粉)表面的变化如图所示。
在水处理剂(主要成分为铁粉、炭粉)表面的变化如图所示。
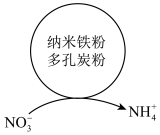
①图中,纳米铁粉作__________ (填“正极”或“负极”),多孔炭粉的作用为__________ 。
②正极上的电极反应式为__________ 。
(2)科研人员利用垃圾渗透液实现发电、环保二位一体,装置如图(a、b为离子交换膜)。
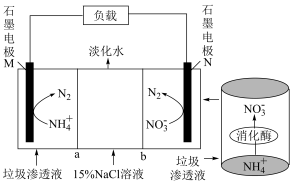
①石墨电极M上的电极反应式为__________ 。
②a为__________ (填“阴离子”或“阳离子”)交换膜。
③在放电过程中, 由中间室向
由中间室向__________ (填“M”或“N”)极室移动。
④理论上M极每处理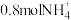 ,电路中通过的电子数为
,电路中通过的电子数为__________  。
。
(1)利用原电池原理,酸性废水中的
 在水处理剂(主要成分为铁粉、炭粉)表面的变化如图所示。
在水处理剂(主要成分为铁粉、炭粉)表面的变化如图所示。
①图中,纳米铁粉作
②正极上的电极反应式为
(2)科研人员利用垃圾渗透液实现发电、环保二位一体,装置如图(a、b为离子交换膜)。

①石墨电极M上的电极反应式为
②a为
③在放电过程中,
 由中间室向
由中间室向④理论上M极每处理
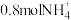 ,电路中通过的电子数为
,电路中通过的电子数为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学设计如图所示装置研究原电池原理。
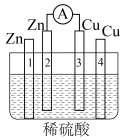
(1)正极发生的电极反应式为____________________ 。
(2)Cu(3)与Cu (4)上现象有何不同?_________ 。
(3)若保持正负极发生的反应不变,正极材料还可以是_________ (填序号)。
①碳棒②铝片③银棒
(4)溶液中 的移动方向是
的移动方向是_________ (填序号)(①从左往右②从右往左③不动)
(5)若将稀硫酸换为稀硝酸,Cu (4)上反应的离子方程式为____________________ 。

(1)正极发生的电极反应式为
(2)Cu(3)与Cu (4)上现象有何不同?
(3)若保持正负极发生的反应不变,正极材料还可以是
①碳棒②铝片③银棒
(4)溶液中
 的移动方向是
的移动方向是(5)若将稀硫酸换为稀硝酸,Cu (4)上反应的离子方程式为
您最近一年使用:0次
【推荐2】化学反应所提供的能量大大促进了社会的发展,研究化学反应中的能量变化有重要意义,回答下列问题:
(1)生活中常见燃料的燃烧热如下表所示:
①写出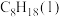 燃烧热的热化学方程式:
燃烧热的热化学方程式:___________ 。
②“热值”指单位质量的燃料完全燃烧放出的热量,则 的热值为
的热值为___________ kJ/kg。
③已知:
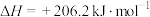

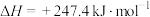
则 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
④碱性氢气燃料电池可大大提高氢气的能量利用率,请写出该燃料电池负极的电极反应式:___________ 。该燃料电池转移2 mol电子时,实际提供的电能为200.06 kJ,则该电池的能量转化率为___________ %(保留整数)。
(2)火箭推进剂常用液态过氧化氢作氧化剂,液态肼( )作还原剂,二者混合即可剧烈反应生成氮气和水,若0.5 mol肼完全被氧化放出408.8 kJ的热量。则6.4 g液态肼完全被氧化转移电子的数目为
)作还原剂,二者混合即可剧烈反应生成氮气和水,若0.5 mol肼完全被氧化放出408.8 kJ的热量。则6.4 g液态肼完全被氧化转移电子的数目为___________  ,放出的热量为
,放出的热量为___________ kJ(保留两位小数)。
(1)生活中常见燃料的燃烧热如下表所示:
| 燃料 |  | CO |  | 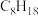 |
燃烧热/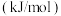 | 285.8 | 283.0 | 890.3 | 5518 |
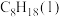 燃烧热的热化学方程式:
燃烧热的热化学方程式:②“热值”指单位质量的燃料完全燃烧放出的热量,则
 的热值为
的热值为③已知:

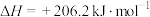

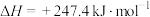
则
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为④碱性氢气燃料电池可大大提高氢气的能量利用率,请写出该燃料电池负极的电极反应式:
(2)火箭推进剂常用液态过氧化氢作氧化剂,液态肼(
 )作还原剂,二者混合即可剧烈反应生成氮气和水,若0.5 mol肼完全被氧化放出408.8 kJ的热量。则6.4 g液态肼完全被氧化转移电子的数目为
)作还原剂,二者混合即可剧烈反应生成氮气和水,若0.5 mol肼完全被氧化放出408.8 kJ的热量。则6.4 g液态肼完全被氧化转移电子的数目为 ,放出的热量为
,放出的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(如图)。有关反应一段时间后的实验现象,下列说法正确的是_______。
(3)请利用反应“Cu+2Ag+=Cu2++2Ag”设计一个化学电池(正极材料用碳棒),该电池的负极材料是_______ ,发生的电极反应是_______ ,电解质溶液是_______ 。
(4)正极上出现的现象是_______ 。
(5)若导线上转移电子1 mol,则生成银_______  。
。
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
A.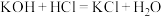 | B. |
C.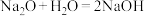 | D. |
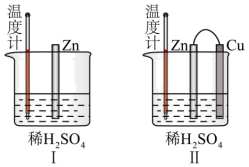
| A.图Ⅰ中温度计的示数高于图Ⅱ的示数 |
| B.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温 |
| C.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面 |
| D.图Ⅱ中产生气体的速率比Ⅰ慢 |
(4)正极上出现的现象是
(5)若导线上转移电子1 mol,则生成银
 。
。
您最近一年使用:0次


 在硫氧化菌作用下转化为
在硫氧化菌作用下转化为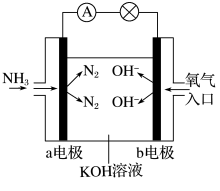
 ,请依据反应原理解释原因:
,请依据反应原理解释原因:

