海藻中提取碘的流程如图,已知氧化过程发生反应的化学方程式为:Cl2+2KI=2KCl+I2。请回答下列问题:

(1)指出提取碘的过程中有关实验操作①和②的名称:___ ;___ 。
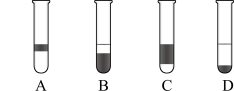
(2)在3 mL含碘的水溶液中加入1mL四氯化碳,振荡静置后观察到试管里的分层现象是图中的___ (注:试管中深色区为有色溶液),上层无色溶液的溶质是___ ,下层颜色是___ 。
(3)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过的操作是___ 。


(1)指出提取碘的过程中有关实验操作①和②的名称:
(2)在3 mL含碘的水溶液中加入1mL四氯化碳,振荡静置后观察到试管里的分层现象是图中的
(3)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过的操作是
更新时间:2020-02-11 20:33:42
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性。
【制备FeBr2固体】
实验室用如图所示装置制取溴化亚铁。其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两个耐高温的瓷皿,其中盛有细铁粉。
实验开始时,先将干燥、纯净的CO2气流通入D中,再将铁粉加热至600—700℃,E管中铁粉开始反应。不断将d中液溴滴入温度为100—120℃的D中,经过一段时间的连续反应,在不锈钢管内产生黄绿色鳞片状溴化亚铁。

(1)若在A中盛固体CaCO3,a中盛有6 mol/L的盐酸。为使导入D中的CO2为干燥纯净的气体,则图中B、C处的洗气瓶中装有的试剂分别是:B中为____________ ,C中为_________ 。若进入E装置中的CO2未干燥,则可能发生的副反应的化学方程式为__________ 。
(2)E管中的反应开始后持续通入CO2的主要作用是______________ 。
【探究FeBr2的还原性】
(3)已知:Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色。Cl2既能氧化Br-,也能氧化Fe2+。取10 mL0.1mol/LFeBr2溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为血红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。以上实验结论表明还原性:Fe2+_________ Br-(填“>”或“<”)。
(4)若在40 mL上述FeBr2溶液中通入标准状况下67.2 mL的 C12,取少量反应后的溶液加入CCl4,振荡后下层液体呈_______ 色,写出该反应的离子方程式______ 。
【制备FeBr2固体】
实验室用如图所示装置制取溴化亚铁。其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两个耐高温的瓷皿,其中盛有细铁粉。
实验开始时,先将干燥、纯净的CO2气流通入D中,再将铁粉加热至600—700℃,E管中铁粉开始反应。不断将d中液溴滴入温度为100—120℃的D中,经过一段时间的连续反应,在不锈钢管内产生黄绿色鳞片状溴化亚铁。

(1)若在A中盛固体CaCO3,a中盛有6 mol/L的盐酸。为使导入D中的CO2为干燥纯净的气体,则图中B、C处的洗气瓶中装有的试剂分别是:B中为
(2)E管中的反应开始后持续通入CO2的主要作用是
【探究FeBr2的还原性】
(3)已知:Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色。Cl2既能氧化Br-,也能氧化Fe2+。取10 mL0.1mol/LFeBr2溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为血红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。以上实验结论表明还原性:Fe2+
(4)若在40 mL上述FeBr2溶液中通入标准状况下67.2 mL的 C12,取少量反应后的溶液加入CCl4,振荡后下层液体呈
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某同学完成如下实验。
(1)实验记录(请补全表格中空格 )
(2)该实验的目的是______________________ 。
(3)氯、溴、碘单质氧化性逐渐减弱的原因:同主族元素,最外层电子数相同,从上到下,_________ ,得电子能力逐渐减弱。
(1)实验记录(
| 实验步骤 | 实验现象 | 离子方程式 |
 | ①溶液分层 ②下层呈橙色。 | |
 | ①溶液分层 ② | Br2+2I-=I2+2Br- |
(2)该实验的目的是
(3)氯、溴、碘单质氧化性逐渐减弱的原因:同主族元素,最外层电子数相同,从上到下,
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】工业以浓缩海水为原料提取溴的部分过程如图:
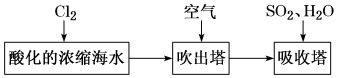
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):
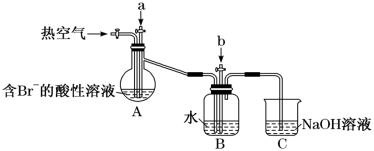
实验开始时,A装置中不通热空气,先通入氯气。
(1)反应过程中,B装置中Br2与SO2反应的化学方程式:_______ 。
(2)C装置的作用是_______ 。
(3)该小组同学向反应后B装置的溶液中通入氯气,充分反应得到混合液。
①一位同学根据溴的沸点是59℃,提出采用_______ 方法从该混合液中分离出溴单质。
②另一位同学向该混合液中加入四氯化碳,充分振荡、静置后放出下层液体,这种方法是_______ 。
(4)(CN)2与Cl2性质相似,则(CN)2分子中含有的化学键有_______ (填“离子键”、“极性键”或“非极性键”);(CN)2的制备原理同实验室制取Cl2类似,在酸性条件下用MnO2氧化对应的阴离子得到。写出制取(CN)2的离子方程式:_______ 。

某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):

实验开始时,A装置中不通热空气,先通入氯气。
(1)反应过程中,B装置中Br2与SO2反应的化学方程式:
(2)C装置的作用是
(3)该小组同学向反应后B装置的溶液中通入氯气,充分反应得到混合液。
①一位同学根据溴的沸点是59℃,提出采用
②另一位同学向该混合液中加入四氯化碳,充分振荡、静置后放出下层液体,这种方法是
(4)(CN)2与Cl2性质相似,则(CN)2分子中含有的化学键有
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐1】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
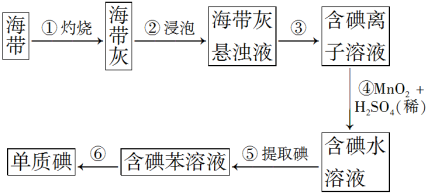
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是_______ (从下列仪器中选出所需的仪器,将标号字母填写在空白处)。
A.烧杯 B.表面皿 C.坩埚 D.酒精灯 E.干燥器
(2)步骤④一定发生的化学反应类型是_______ 。
A.化合反应 B.分解反应 C.氧化还原反应
(3)步骤⑤所用的主要仪器是_______ 。步骤③的实验操作名称是_______ 。
(4)①~⑥操作中,使用玻璃棒的是_______ (填序号)。
(5)请设计简单实验,验证⑤提取碘后的水溶液中是否含有碘单质_______ 。

请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是
A.烧杯 B.表面皿 C.坩埚 D.酒精灯 E.干燥器
(2)步骤④一定发生的化学反应类型是
A.化合反应 B.分解反应 C.氧化还原反应
(3)步骤⑤所用的主要仪器是
(4)①~⑥操作中,使用玻璃棒的是
(5)请设计简单实验,验证⑤提取碘后的水溶液中是否含有碘单质
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】碘化钠可用作甲状腺肿瘤防治剂、祛痰剂和利尿剂等。某探究小组利用NaOH、单质碘和水合肼(N2H4•H2O)为原料可制备碘化钠。
资料显示:水合肼有还原性,能消除水中溶解的氧气;NaIO3是一种氧化剂。
回答下列问题:
[实验一]制备NaClO溶液
实验装置如图所示:

(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有__ (填序号)。
A.烧杯 B.容量瓶 C.烧瓶 D.玻璃棒
(2)锥形瓶中发生反应的离子方程式是___ 。
[实验二]制取水合肼。
制备原理:CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl
实验装置如图所示:
控制反应温度,将分液漏斗中的溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108℃~114℃馏分。
(3)分液漏斗中的溶液是__ (填序号)。选择的理由是__ 。
A.NaOH和NaClO混合溶液
B.CO(NH2)2溶液
[实验三]制备碘化钠
探究小组用NaOH、单质碘和水合肼(N2H4•H2O)为原料可制备碘化钠。其步骤如下:
(4)步骤一:向三颈烧瓶中加入过量的NaOH及水,搅拌、冷却,再加入碘单质,打开恒温磁力搅拌器,保持60℃~70℃至反应完全;观察到的现象是___ 。
(5)步骤二:继续加入稍过量的N2H4•H2O,还原NaIO和NaIO3,得NaI溶液粗品;向上述反应液中加入活性炭,煮沸半小时,然后将溶液与活性炭分离,分离的方法是___ 。
(6)步骤三:将步骤二中分离出的溶液__ 、__ 、过滤、洗涤、干燥,得产品。
(7)某同学检验产品NaI中是否混有NaIO3杂质。取少量固体样品于试管中,加水溶解,滴加少量淀粉溶液后再滴加适量稀硫酸,片刻后溶液变蓝,由此得出NaI中含有NaIO3杂质。请评价该实验结论的合理性:___ (填“合理”或“不合理”)。
资料显示:水合肼有还原性,能消除水中溶解的氧气;NaIO3是一种氧化剂。
回答下列问题:
[实验一]制备NaClO溶液
实验装置如图所示:

(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有
A.烧杯 B.容量瓶 C.烧瓶 D.玻璃棒
(2)锥形瓶中发生反应的离子方程式是
[实验二]制取水合肼。
制备原理:CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl
实验装置如图所示:

控制反应温度,将分液漏斗中的溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108℃~114℃馏分。
(3)分液漏斗中的溶液是
A.NaOH和NaClO混合溶液
B.CO(NH2)2溶液
[实验三]制备碘化钠
探究小组用NaOH、单质碘和水合肼(N2H4•H2O)为原料可制备碘化钠。其步骤如下:
(4)步骤一:向三颈烧瓶中加入过量的NaOH及水,搅拌、冷却,再加入碘单质,打开恒温磁力搅拌器,保持60℃~70℃至反应完全;观察到的现象是
(5)步骤二:继续加入稍过量的N2H4•H2O,还原NaIO和NaIO3,得NaI溶液粗品;向上述反应液中加入活性炭,煮沸半小时,然后将溶液与活性炭分离,分离的方法是
(6)步骤三:将步骤二中分离出的溶液
(7)某同学检验产品NaI中是否混有NaIO3杂质。取少量固体样品于试管中,加水溶解,滴加少量淀粉溶液后再滴加适量稀硫酸,片刻后溶液变蓝,由此得出NaI中含有NaIO3杂质。请评价该实验结论的合理性:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】海带含有丰富的碘,为了从海带中提取碘,设计并进行以下实验:
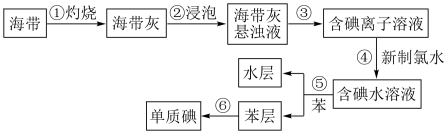
完成下列填空:
(1)步骤①灼烧海带时,不需要用到的仪器是_______ (选填编号)
(2)步骤③的操作名称是_______ ;步骤⑤的操作名称是_______ 。
(3)步骤②加速溶解的方法_______ 。(写出一种合理的措施)
(4)步骤⑤中不能用酒精代替苯的理由是_______ 。
(5)步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作是_______ 。

完成下列填空:
(1)步骤①灼烧海带时,不需要用到的仪器是
A. | B. | C. | D. |
(3)步骤②加速溶解的方法
(4)步骤⑤中不能用酒精代替苯的理由是
(5)步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】海洋植物如海带和海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋中提取碘的流程如下:
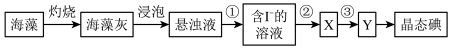
某化学兴趣小组将上述流程②、③设计成如下图所示操作。
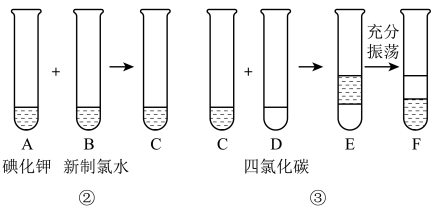
已知过程②发生反应的化学方程式为Cl2+2KI=2KCl+I2,回答下列问题:
(1)写出提取过程①、③中实验操作的名称:①___________ ,③___________ 。
(2)步骤③中充分振荡后的现象是___________ 。
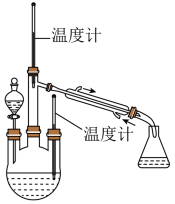
(3)从F中提取碘和回收有机溶剂,需要经过蒸馏,指出下面蒸馏装置图中的错误之处。

①___________ ;
②___________ ;

某化学兴趣小组将上述流程②、③设计成如下图所示操作。

已知过程②发生反应的化学方程式为Cl2+2KI=2KCl+I2,回答下列问题:
(1)写出提取过程①、③中实验操作的名称:①
(2)步骤③中充分振荡后的现象是
(3)从F中提取碘和回收有机溶剂,需要经过蒸馏,指出下面蒸馏装置图中的错误之处。

①
②
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】海带含有丰富的碘。为了从海带中提取碘,某学习小组设计并进行了以下实验:
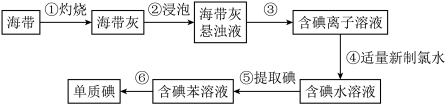
(1)海带提碘实验中不需要的仪器是_________ (选填编号)。
A. B.
B. C.
C. D.
D. 
(2)步骤③的实验操作名称是____________ ;用到的玻璃仪器有(写仪器名称)_____________________________________ 。
(3)步骤④反应的离子方程式是__________________________________ 。
(4)步骤⑤是用有机溶剂将碘从水中提取出来,此过程包含的实验操作是_______________ 、_______________ 。不能用酒精代替苯的理由是_________________________ (用文字简述)。
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法(用文字简述):_________________________________ 。

(1)海带提碘实验中不需要的仪器是
A.
 B.
B. C.
C. D.
D. 
(2)步骤③的实验操作名称是
(3)步骤④反应的离子方程式是
(4)步骤⑤是用有机溶剂将碘从水中提取出来,此过程包含的实验操作是
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法(用文字简述):
您最近一年使用:0次

 、
、 、
、 、
、 溶液,请根据有关物质的性质,设计实验将其区分开来。
溶液,请根据有关物质的性质,设计实验将其区分开来。

