原子序数为114号的稳定同位素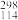 X预测。
X预测。
(1)114X元素位于元素周期表第________ 周期____ 族,为________ 元素(“金属”、“非金属”)。
(2)其最高价氧化物及其对应水化物的分子式分别是____ 、____ (用含X的式子表示),并估计后者为_______ 性(酸碱、两性)。
(3)它与氯生成化合物的分子式________ 、________ (用含X的式子表示)。
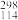 X预测。
X预测。(1)114X元素位于元素周期表第
(2)其最高价氧化物及其对应水化物的分子式分别是
(3)它与氯生成化合物的分子式
更新时间:2020-02-10 15:24:45
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。请依据元素周期表回答问题。
(1)填写下表
(2)丙的原子结构示意图是__________ ,该元素与同周期ⅦA族元素组成的化合物类型是_________ 。
(1)填写下表
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 原子序数 | 6 | 13 | ||
| 元素周期表中的位置 | 第二周期第ⅥA族 | 第三周期第IA族 |
(2)丙的原子结构示意图是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】2006年,科学家以钙离子撞击锎(Cf)靶,产生了一种超重元素——  (Og),其反应可表示为:
(Og),其反应可表示为: 。请判断
。请判断 在周期表中的位置
在周期表中的位置_________ ,并推测其可能与哪类元素性质相似_________ 。
 (Og),其反应可表示为:
(Og),其反应可表示为: 。请判断
。请判断 在周期表中的位置
在周期表中的位置
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(1)基态 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为___________ 。
(2)基态 原子的核外电子排布式为
原子的核外电子排布式为___________ 。
(3) 位于元素周期表中第四周期第
位于元素周期表中第四周期第___________ 族,基态 原子核外未成对电子有
原子核外未成对电子有___________ 个。
(4)基态 原子价电子的电子排布图(轨道表达式)为
原子价电子的电子排布图(轨道表达式)为___________ ,基态S原子电子占据最高能级的电子云轮廓图为___________ 形。
(5) 原子核外电子排布式为
原子核外电子排布式为___________ 。
(6)氮原子价层电子的轨道表达式(电子排布图)为___________ 。
(7) 基态原子核外电子排布式为
基态原子核外电子排布式为___________ 。
 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为(2)基态
 原子的核外电子排布式为
原子的核外电子排布式为(3)
 位于元素周期表中第四周期第
位于元素周期表中第四周期第 原子核外未成对电子有
原子核外未成对电子有(4)基态
 原子价电子的电子排布图(轨道表达式)为
原子价电子的电子排布图(轨道表达式)为(5)
 原子核外电子排布式为
原子核外电子排布式为(6)氮原子价层电子的轨道表达式(电子排布图)为
(7)
 基态原子核外电子排布式为
基态原子核外电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】下列曲线分别表示元素的某种性质与核电荷数的关系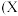 为核电荷数,Y为元素的有关性质
为核电荷数,Y为元素的有关性质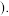 把与下面元素有关的性质相符的曲线标号填入相应的横线中:
把与下面元素有关的性质相符的曲线标号填入相应的横线中:
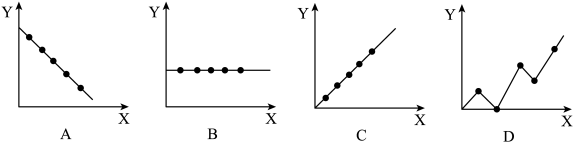
(1)第VIA族元素的最外层电子数是______
(2)第三周期元素的最高化合价是______
(3) 、
、 、
、 、
、 、
、 的离子半径是
的离子半径是 ______ .
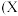 为核电荷数,Y为元素的有关性质
为核电荷数,Y为元素的有关性质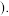 把与下面元素有关的性质相符的曲线标号填入相应的横线中:
把与下面元素有关的性质相符的曲线标号填入相应的横线中: 
(1)第VIA族元素的最外层电子数是
(2)第三周期元素的最高化合价是
(3)
 、
、 、
、 、
、 、
、 的离子半径是
的离子半径是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】归纳整理是科学学习的重要方法之一。在学习了卤族元素的各种性质后,可归纳整理出如下所示的表格:
请根据表回答下列问题:
(1)溴单质的熔点范围可能是_______ 。
(2)碘元素的化合价可能有_______ 。
(3)氯、溴、碘的最高价氧化物对应水化物的酸性由强到弱的顺序是_______ (填化学式)。
(4) 与金刚石互为同素异形体,两者的物理性质差异较大。下列关于
与金刚石互为同素异形体,两者的物理性质差异较大。下列关于 的说法中,正确的是_______。
的说法中,正确的是_______。
(5)在打开原子结构大门的过程中,科学家运用了许多科学方法,除模型方法外,请从下列方法中选择出人们在认识原子结构过程中所运用的科学方法_______ (多项选择,填写序号)。
①实验方法 ②假说方法 ③类比方法 ④推理方法
 | 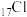 | 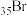 | 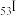 | |
| 单质熔点(℃) | ﹣219.6 | ﹣101 | 113.5 | |
| 单质沸点(℃) | ﹣188.1 | ﹣34.6 | 58.8 | 184.4 |
| 主要化合价 | ﹣1 | ﹣1,+1,+3,+5,+7, | ﹣1,+1,+3,+5,+7 | |
| 原子半径 |  | |||
单质与 反应情况 反应情况 | 喑处剧烈化合并爆炸 | 光照或点燃反应 | 加热至一定温度反应 | 不断加热才缓慢反应 |
请根据表回答下列问题:
(1)溴单质的熔点范围可能是
(2)碘元素的化合价可能有
(3)氯、溴、碘的最高价氧化物对应水化物的酸性由强到弱的顺序是
(4)
 与金刚石互为同素异形体,两者的物理性质差异较大。下列关于
与金刚石互为同素异形体,两者的物理性质差异较大。下列关于 的说法中,正确的是_______。
的说法中,正确的是_______。| A.易溶于水 | B.易溶于氯化钠溶液 |
| C.可溶于苯等有机溶剂 | D.易溶于氨水 |
①实验方法 ②假说方法 ③类比方法 ④推理方法
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】1999年俄、美科学家联合小组合成了第114号元素的一种同位素,该核素原子的质量数为298,则这种同位素原子的核内中子数为________ ,核内质子数为________ ,近似相对原子质量为________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】现有下列9种微粒: 、
、 、
、 、
、 、
、 、
、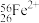 、
、 、
、 、
、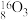 。按要求完成以下各题:
。按要求完成以下各题:
(1) 、
、 分别是氢元素的一种
分别是氢元素的一种______ ,它们互为______ 。
(2)互为同素异形体的微粒是______ 。
(3)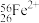 的中子数为
的中子数为______ ,核外电子数为______ 。
(4)形成上述9种微粒的核素有______ 种、元素有______ 种。
 、
、 、
、 、
、 、
、 、
、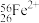 、
、 、
、 、
、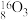 。按要求完成以下各题:
。按要求完成以下各题:(1)
 、
、 分别是氢元素的一种
分别是氢元素的一种(2)互为同素异形体的微粒是
(3)
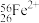 的中子数为
的中子数为(4)形成上述9种微粒的核素有
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】放射性原子在人类的生活中的很多地方有着特殊的作用,对人类的科学研究有很大的帮助,其中最主要的作用是作为示踪原子。最近医学界通过用放射性14C的羧酸衍生物在特定条件下通过断裂DNA来杀死细胞,从而抑制艾滋病。
(1)下面有关14C的叙述正确的是_______ 。
A、14C与14N含有相同的中子数 B、14C与C60是同分异构体
C、14C与C60中普通碳原子的化学性质不同 D、14C与12C互为同位素
(2)自然界中存在很多像14C的放射性原子,这些天然放射现象的发现说明了什么问题____ 。
A、原子不可以再分 B、原子的核式结构
C、原子核还可以再分 D、原子核是由质子和中子构成
(1)下面有关14C的叙述正确的是
A、14C与14N含有相同的中子数 B、14C与C60是同分异构体
C、14C与C60中普通碳原子的化学性质不同 D、14C与12C互为同位素
(2)自然界中存在很多像14C的放射性原子,这些天然放射现象的发现说明了什么问题
A、原子不可以再分 B、原子的核式结构
C、原子核还可以再分 D、原子核是由质子和中子构成
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】有下列各组物质:① 和
和 ;②石墨和足球烯;③CH3-CH2-CH2-CH3和CH3-CH(CH3)CH3④正丁烷和异庚烷;⑤
;②石墨和足球烯;③CH3-CH2-CH2-CH3和CH3-CH(CH3)CH3④正丁烷和异庚烷;⑤ 和
和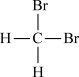 。用序号填空:
。用序号填空:
(1)_______ 组两者互为同位素。
(2)_______ 组两者互为同素异形体。
(3)_______ 组两者属于同系物。
(4)_______ 组两者互为同分异构体。
(5)_______ 组两者是同一物质。
 和
和 ;②石墨和足球烯;③CH3-CH2-CH2-CH3和CH3-CH(CH3)CH3④正丁烷和异庚烷;⑤
;②石墨和足球烯;③CH3-CH2-CH2-CH3和CH3-CH(CH3)CH3④正丁烷和异庚烷;⑤ 和
和 。用序号填空:
。用序号填空:(1)
(2)
(3)
(4)
(5)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】请按要求填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的核组成符号:________ ;
(2)CO2的电子式是________ ,NH4Cl的电子式是________ ;
(3)物质在下列变化过程中克服的是:①共价键②离子键。(填序号)
HCl溶于水____ ;电解熔融NaCl制Na____ ;电解水分解生成O2和H2______ 。
(4)下列物质中:互为同分异构体的有_________ ;互为同素异形体的有________ ;
属于同位素的有________ ; 属于同一种物质的有________ 。(填序号)
①液氯 ②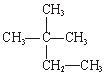 ③白磷 ④氯气 ⑤
③白磷 ④氯气 ⑤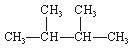 ⑥
⑥ Cl ⑦
Cl ⑦ Cl ⑧红磷
Cl ⑧红磷
(1)写出表示含有8个质子、10个中子的原子的核组成符号:
(2)CO2的电子式是
(3)物质在下列变化过程中克服的是:①共价键②离子键。(填序号)
HCl溶于水
(4)下列物质中:互为同分异构体的有
属于同位素的有
①液氯 ②
 ③白磷 ④氯气 ⑤
③白磷 ④氯气 ⑤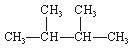 ⑥
⑥ Cl ⑦
Cl ⑦ Cl ⑧红磷
Cl ⑧红磷
您最近一年使用:0次

 、
、 、
、 ;②H2、D2、T2;③石墨、金刚石;④
;②H2、D2、T2;③石墨、金刚石;④ 、
、 、
、 ,以上四组微粒或物质中:
,以上四组微粒或物质中:

